Règlement (UE) 2017/746 relatif aux dispositifs médicaux de diagnostic in vitro (DMDIV)
Union Européenne
Cette page reproduit le Règlement (UE) 2017/746 relatif aux dispositifs médicaux de diagnostic in vitro (DMDIV) avec une table des matières et des hyperliens dans le corps du texte.
Aucune modification n'a été apportée au texte original diffusé par EUR-Lex sous licence Creative Commons Attribution 4.0 International.
CHAPITRE I — DISPOSITIONS LIMINAIRES
-
SECTION 1 — Champ d'application et définitions
-
SECTION 2 — Statut des produits au regard de la réglementation et conseils
CHAPITRE II — MISE À DISPOSITION SUR LE MARCHÉ ET MISE EN SERVICE DES DISPOSITIFS, OBLIGATIONS DES OPÉRATEURS ÉCONOMIQUES, MARQUAGE CE ET LIBRE CIRCULATION
- Article 5 - Mise sur le marché et mise en service
- Article 6 - Ventes à distance
- Article 7 - Allégations
- Article 8 - Application de normes harmonisées
- Article 9 - Spécifications communes
- Article 10 - Obligations générales des fabricants
- Article 11 - Mandataire
- Article 12 - Changement de mandataire
- Article 13 - Obligations générales des importateurs
- Article 14 - Obligations générales des distributeurs
- Article 15 - Personne chargée de veiller au respect de la réglementation
- Article 16 - Cas dans lesquels les obligations des fabricants s'appliquent aux importateurs, aux distributeurs ou à d'autres personnes
- Article 17 - Déclaration de conformité UE
- Article 18 - Marquage de conformité CE
- Article 19 - Dispositifs destinés à des usages particuliers
- Article 20 - Parties et éléments
- Article 21 - Libre circulation
CHAPITRE III — IDENTIFICATION ET TRAÇABILITÉ DES DISPOSITIFS, ENREGISTREMENT DES DISPOSITIFS ET DES OPÉRATEURS ÉCONOMIQUES, RÉSUMÉ DES CARACTÉRISTIQUES DE SÉCURITÉ ET DES PERFORMANCES CLINIQUES ET BASE DE DONNÉES EUROPÉENNE SUR LES DISPOSITIFS MÉDICAUX
- Article 22 - Identification dans la chaîne d'approvisionnement
- Article 23 - Nomenclature des dispositifs médicaux
- Article 24 - Système d'identification unique des dispositifs
- Article 25 - Base de données IUD
- Article 26 - Enregistrement des dispositifs
- Article 27 - Système électronique d'enregistrement des opérateurs économiques
- Article 28 - Enregistrement des fabricants, mandataires et importateurs
- Article 29 - Résumé des caractéristiques de sécurité et des performances
- Article 30 - Base de données européenne sur les dispositifs médicaux
CHAPITRE IV — ORGANISMES NOTIFIÉS
- Article 31 - Autorités responsables des organismes notifiés
- Article 32 - Exigences applicables aux organismes notifiés
- Article 33 - Filiales et sous-traitance
- Article 34 - Demande de désignation d'organismes d'évaluation de la conformité
- Article 35 - Évaluation de la demande
- Article 36 - Nomination d'experts pour l'évaluation conjointe des demandes de notification
- Article 37 - Exigences linguistiques
- Article 38 - Procédure de désignation et de notification
- Article 39 - Numéro d'identification et liste des organismes notifiés
- Article 40 - Surveillance et réévaluation des organismes notifiés
- Article 41 - Examen de l'évaluation de la documentation technique et de la documentation relative à l'évaluation des performances effectuée par l'organisme notifié
- Article 42 - Modifications des désignations et des notifications
- Article 43 - Contestation de la compétence des organismes notifiés
- Article 44 - Évaluation par les pairs et échange d'expérience entre les autorités responsables des organismes notifiés
- Article 45 - Coordination des organismes notifiés
- Article 46 - Listes de redevances standard
CHAPITRE V — CLASSIFICATION ET ÉVALUATION DE LA CONFORMITÉ
-
SECTION 1 - Classification
-
SECTION 2 - Évaluation de la conformité
- Article 48 - Procédures d'évaluation de la conformité
- Article 49 - Intervention des organismes notifiés dans les procédures d'évaluation de la conformité
- Article 50 - Mécanisme de contrôle des évaluations de la conformité des dispositifs de classe D
- Article 51 - Certificats de conformité
- Article 52 - Système électronique relatif aux organismes notifiés et aux certificats de conformité
- Article 53 - Changement volontaire d'organisme notifié
- Article 54 - Dérogation aux procédures d'évaluation de la conformité
- Article 55 - Certificat de libre vente
CHAPITRE VI — PREUVE CLINIQUE, ÉVALUATION DES PERFORMANCES ET ÉTUDES DES PERFORMANCES
- Article 56 - Évaluation des performances et preuve clinique
- Article 57 - Exigences générales relatives aux études des performances
- Article 58 - Exigences supplémentaires pour certaines études des performances
- Article 59 - Consentement éclairé
- Article 60 - Études des performances sur des participants incapables
- Article 61 - Études des performances sur des mineurs
- Article 62 - Études des performances sur des femmes enceintes ou allaitantes
- Article 63 - Mesures nationales supplémentaires
- Article 64 - Études des performances en situation d'urgence
- Article 65 - Compensation de dommages
- Article 66 - Demande relative aux études des performances
- Article 67 - Évaluation par les États membres
- Article 68 - Réalisation d'une étude des performances
- Article 69 - Système électronique relatif aux études des performances
- Article 70 - Études des performances concernant les dispositifs munis du marquage CE
- Article 71 - Modifications substantielles d'études des performances
- Article 72 - Mesures correctives à prendre par les États membres et échange d'informations entre les États membres concernant les études des performances
- Article 73 - Information par le promoteur à la fin d'une étude des performances ou en cas d'interruption temporaire ou d'arrêt anticipé
- Article 74 - Procédure d'évaluation coordonnée concernant les études des performances
- Article 75 - Réexamen de la procédure d'évaluation coordonnée
- Article 76 - Enregistrement et notification des événements indésirables survenant pendant les études des performances
- Article 77 - Actes d'exécution
CHAPITRE VII — SURVEILLANCE APRÈS COMMERCIALISATION, VIGILANCE ET SURVEILLANCE DU MARCHÉ
-
SECTION 1 - Surveillance après commercialisation
-
SECTION 2 - Vigilance
- Article 82 - Notification des incidents graves et des mesures correctives de sécurité
- Article 83 - Rapport de tendances
- Article 84 - Analyse des incidents graves et des mesures correctives de sécurité
- Article 85 - Analyse des données issues de la vigilance
- Article 86 - Actes d'exécution
- Article 87 - Système électronique relatif à la vigilance et à la surveillance après commercialisation
-
SECTION 3 - Surveillance du marché
- Article 88 - Activités de surveillance du marché
- Article 89 - Évaluation des dispositifs dont on suspecte qu'ils présentent un risque inacceptable ou une autre non-conformité
- Article 90 - Procédure applicable aux dispositifs présentant un risque inacceptable pour la santé et la sécurité
- Article 91 - Procédure d'évaluation des mesures nationales au niveau de l'Union
- Article 92 - Autre non-conformité
- Article 93 - Mesures préventives de protection de la santé
- Article 94 - Bonnes pratiques administratives
- Article 95 - Système électronique relatif à la surveillance du marché
CHAPITRE VIII — COOPÉRATION ENTRE LES ÉTATS MEMBRES, LE GROUPE DE COORDINATION EN MATIÈRE DE DISPOSITIFS MÉDICAUX, LES LABORATOIRES DE RÉFÉRENCE DE L'UE ET LES REGISTRES DE DISPOSITIFS
- Article 96 - Autorités compétentes
- Article 97 - Coopération
- Article 98 - Groupe de coordination en matière de dispositifs médicaux
- Article 99 - Tâches du GCDM
- Article 100 - Les laboratoires de référence de l'Union européenne
- Article 101 - Registres de dispositifs et banques de données
CHAPITRE IX — CONFIDENTIALITÉ, PROTECTION DES DONNÉES, FINANCEMENT ET SANCTIONS
- Article 102 - Confidentialité
- Article 103 - Protection des données
- Article 104 - Perception de redevances
- Article 105 - Financement des activités liées à la désignation et au contrôle des organismes notifiés
- Article 106 - Sanctions
CHAPITRE X — DISPOSITIONS FINALES
- Article 107 - Comité
- Article 108 - Exercice de la délégation
- Article 109 - Actes délégués distincts pour chaque délégation de pouvoir
- Article 110 - Dispositions transitoires
- Article 111 - Évaluation
- Article 112 - Abrogation
- Article 113 - Entrée en vigueur et date d'application
ANNEXES
- Annexe I - Exigences générales en matière de sécurité et de performances
- Annexe II - Documentation technique
- Annexe III - Documentation technique relative à la surveillance après commercialisation
- Annexe IV - Déclaration de conformité UE
- Annexe V - Marquage de conformité CE
- Annexe VI - Informations à fournir pour l'enregistrement des dispositifs et des opérateurs économiques conformément à l'article 26, paragraphe 3, et à l'article 28, principaux éléments de données à fournir à la base de données IUD avec l'IUD-ID conformément aux articles 25 et 26 et système d'IUD
- Annexe VII - Exigences auxquelles doivent satisfaire les organismes notifiés
- Annexe VIII - Règles de classification
- Annexe IX - Évaluation de la conformité sur la base d'un système de gestion de la qualité et de l'évaluation de la documentation technique
- Annexe X - Évaluation de la conformité sur la base de l'examen de type
- Annexe XI - Évaluation de la conformité sur la base de l'assurance de la qualité de la production
- Annexe XII - Certificats délivrés par un organisme notifié
- Annexe XIII - Évaluation des performances, études des performances et suivi des performances après commercialisation
- Annexe XIV - Études interventionnelles des performances cliniques et certaines autres études des performances
- Annexe XV - Tableau de correspondance
RÈGLEMENT (UE) 2017/746 DU PARLEMENT EUROPÉEN ET DU CONSEIL du 5 avril 2017 relatif aux dispositifs médicaux de diagnostic in vitro et abrogeant la directive 98/79/CE et la décision 2010/227/UE de la Commission
(Texte présentant de l'intérêt pour l'EEE)
Inclut les rectifications introduites par :
- le Rectificatif, JO L 117 du 3.5.2019, p. 11 (2017/746) et
- le Rectificatif, JO L 334 du 27.12.2019, p. 167 (2017/746)
LE PARLEMENT EUROPÉEN ET LE CONSEIL DE L'UNION EUROPÉENNE,
vu le traité sur le fonctionnement de l'Union européenne, et notamment son article 114 et son article 168, paragraphe 4, point c),
vu la proposition de la Commission européenne,
après transmission du projet d'acte législatif aux parlements nationaux,
vu l'avis du Comité économique et social européen,
après consultation du Comité des régions,
statuant conformément à la procédure législative ordinaire,
considérant ce qui suit:
(1) |
La directive 98/79/CE du Parlement européen et du Conseil forme le cadre réglementaire de l'Union régissant les dispositifs médicaux de diagnostic in vitro. Toutefois, il est nécessaire de procéder à une révision de fond de cette directive de manière à établir un cadre réglementaire rigoureux, transparent, prévisible et durable pour les dispositifs médicaux de diagnostic in vitro, qui garantisse un niveau élevé de sécurité et de protection de la santé tout en favorisant l'innovation. |
(2) |
Le présent règlement vise à garantir le bon fonctionnement du marché intérieur des dispositifs médicaux de diagnostic in vitro, sur la base d'un niveau élevé de protection de la santé pour les patients et les utilisateurs et compte tenu des petites et moyennes entreprises qui sont actives dans ce secteur. Dans le même temps, il fixe des normes élevées de qualité et de sécurité des dispositifs médicaux de diagnostic in vitro afin de faire face aux enjeux communs de sécurité relatifs à ces produits. Les deux objectifs sont poursuivis simultanément et sont indissociables, sans que l'un ne l'emporte sur l'autre. En ce qui concerne l'article 114 du traité sur le fonctionnement de l'Union européenne, le présent règlement harmonise les dispositions régissant la mise sur le marché et la mise en service sur le marché de l'Union de dispositifs médicaux de diagnostic in vitro et de leurs accessoires, qui peuvent alors bénéficier du principe de libre circulation des marchandises. En ce qui concerne l'article 168, paragraphe 4, point c), du traité sur le fonctionnement de l'Union européenne, le présent règlement fixe des normes élevées de qualité et de sécurité applicables aux dispositifs médicaux de diagnostic in vitro en garantissant, entre autres, que les données issues des études des performances sont fiables et robustes et que la sécurité des participants à ces études est préservée. |
(3) |
Le présent règlement n'entend pas harmoniser les dispositions régissant la remise à disposition sur le marché de dispositifs médicaux de diagnostic in vitro après qu'ils aient déjà été mis en service, dans le cadre notamment de ventes de seconde main. |
(4) |
Il convient, pour améliorer la santé et la sécurité, de renforcer considérablement certains aspects essentiels de l'approche réglementaire en vigueur, tels que la supervision des organismes notifiés, la classification en fonction des risques, les procédures d'évaluation de la conformité, l'évaluation des performances et les études des performances, la vigilance et la surveillance du marché, et d'introduire des dispositions garantissant la transparence et la traçabilité des dispositifs médicaux de diagnostic in vitro. |
(5) |
Pour favoriser la convergence de la réglementation à l'échelle internationale afin de contribuer à instaurer un niveau élevé de sécurité dans le monde entier et de faciliter les échanges commerciaux, il convient de tenir compte, dans la mesure du possible, des lignes directrices élaborées au niveau international relatives aux dispositifs médicaux de diagnostic in vitro, notamment dans le cadre du Groupe de travail sur l'harmonisation mondiale et du Forum international des autorités de réglementation des dispositifs médicaux (IMDRF) qui lui a succédé, et ce notamment dans les dispositions relatives à l'identification unique des dispositifs, aux exigences générales en matière de sécurité et de performances, à la documentation technique, aux règles de classification, aux procédures d'évaluation de la conformité et aux preuves cliniques. |
(6) |
Certaines caractéristiques des dispositifs médicaux de diagnostic in vitro, en particulier concernant la classification en fonction des risques, les procédures d'évaluation de la conformité et les preuves cliniques, et du secteur de ces dispositifs requièrent l'adoption d'une législation spécifique, distincte de la législation régissant les autres dispositifs médicaux, tandis que les aspects horizontaux communs aux deux secteurs devraient être alignés. |
(7) |
Il convient de dissocier clairement le champ d'application du présent règlement de celui des autres actes législatifs relatifs aux produits tels que les dispositifs médicaux, les produits destinés à des usages généraux en laboratoire et les produits destinés exclusivement à la recherche. |
(8) |
Il devrait appartenir aux États membres de trancher au cas par cas la question de savoir si un produit relève ou non du champ d'application du présent règlement. Afin de garantir la cohérence des décisions de qualification à cet égard dans l'ensemble des États membres, notamment en ce qui concerne les cas limites, la Commission devrait être autorisée, de sa propre initiative ou à la demande dûment justifiée d'un État membre, après avoir consulté le groupe de coordination en matière de dispositifs médicaux (GCDM), à trancher au cas par cas la question de savoir si un produit, une catégorie ou un groupe de produit donné relève ou non du champ d'application du présent règlement. Lorsqu'elle examine le statut des produits au regard de la réglementation dans les cas limites impliquant des médicaments, des tissus et cellules humains, des produits biocides ou des produits alimentaires, la Commission devrait veiller à dûment consulter l'Agence européenne des médicaments (EMA), l'Agence européenne des produits chimiques (ECHA) et l'Autorité européenne de sécurité des aliments. |
(9) |
Il apparait que des règles nationales divergentes en ce qui concerne la communication d'informations et de conseils en matière de tests génétiques pourraient n'avoir qu'une incidence limitée sur le bon fonctionnement du marché intérieur. Il convient donc de n'établir dans le présent règlement que des exigences limitées à cet égard, en veillant à respecter en permanence les principes de proportionnalité et de subsidiarité. |
(10) |
Il convient de préciser que tous les essais qui renseignent sur la prédisposition à une affection ou à une maladie, tels que les tests génétiques, et tous les essais fournissant des informations permettant de prévoir la réponse ou les réactions à un traitement, tels que les diagnostics compagnons, sont des dispositifs médicaux de diagnostic in vitro. |
(11) |
Les diagnostics compagnons sont essentiels pour recenser les patients pouvant bénéficier d'un traitement médicamenteux spécifique par la détermination quantitative ou qualitative de marqueurs spécifiques identifiant les participants qui risquent davantage de développer des effets indésirables en réaction au médicament spécifique en question ou, au sein de la population, les patients pour lesquels le produit thérapeutique a fait l'objet d'une étude appropriée et a été jugé sûr et efficace. Les biomarqueurs de ce type peuvent être présents chez des personnes en bonne santé et/ou des patients. |
(12) |
Les dispositifs utilisés en vue d'assurer le suivi d'un traitement médicamenteux afin de veiller à ce que la concentration des substances concernées dans le corps humain soit comprise dans l'intervalle thérapeutique, ne sont pas considérés comme des diagnostics compagnons. |
(13) |
L'exigence prévoyant qu'il convient de réduire les risques autant que possible devrait être respectée compte tenu de l'état de l'art généralement admis dans le domaine de la médecine. |
(14) |
Les aspects liés à la sécurité faisant l'objet de la directive 2014/30/UE du Parlement européen et du Conseil font partie intégrante des exigences générales en matière de sécurité et de performances fixées par le présent règlement pour les dispositifs médicaux de diagnostic in vitro. Le présent règlement devrait dès lors être considéré comme une lex specialis par rapport à la directive 2014/30/UE. |
(15) |
Il convient que le présent règlement contienne des dispositions relatives à la conception et à la fabrication de dispositifs médicaux émettant des rayonnements ionisants sans faire obstacle à l'application de la directive 2013/59/Euratom du Conseil, qui poursuit d'autres objectifs. |
(16) |
Le présent règlement devrait comporter des dispositions quant aux caractéristiques de sécurité et de performances des dispositifs qui sont conçus de manière à prévenir les lésions professionnelles, y compris pour ce qui est de la protection contre les rayonnements. |
(17) |
Il est nécessaire de préciser que les logiciels, spécifiquement destinés par le fabricant à une ou plusieurs des fins médicales visées dans la définition d'un dispositif médical de diagnostic in vitro, constituent, en soi, des dispositifs médicaux de diagnostic in vitro, tandis que les logiciels à usage général, même lorsqu'ils sont utilisés dans un environnement médical, ou les logiciels destinés à des fins ayant trait au bien-être ne constituent pas des dispositifs médicaux de diagnostic in vitro. Le fait qu'un logiciel soit considéré comme un dispositif ou comme un accessoire est indépendant de la localisation du logiciel ou du type d'interconnexion entre le logiciel et un dispositif. |
(18) |
Afin d'accroître la sécurité juridique, il est nécessaire d'aligner sur les pratiques européennes et internationales bien établies dans ce domaine les définitions contenues dans le présent règlement en ce qui concerne les dispositifs proprement dits, la mise à disposition de dispositifs, les opérateurs économiques, les utilisateurs et des processus donnés, l'évaluation de la conformité, les preuves cliniques, la surveillance après commercialisation, la vigilance et la surveillance du marché, les normes et les autres spécifications techniques. |
(19) |
Il convient de préciser qu'il est essentiel que les dispositifs proposés à des personnes dans l'Union au moyen de services de la société de l'information au sens de la directive (UE) 2015/1535 du Parlement européen et du Conseil ainsi que les dispositifs utilisés dans le contexte d'une activité commerciale pour fournir une prestation diagnostique ou thérapeutique à des personnes dans l'Union soient conformes aux exigences du présent règlement lors de la mise sur le marché du produit en question ou de la fourniture de la prestation dans l'Union. |
(20) |
Compte tenu du rôle important de la normalisation dans le domaine des dispositifs médicaux de diagnostic in vitro, le respect des normes harmonisées définies dans le règlement (UE) no 1025/2012 du Parlement européen et du Conseil devrait être un moyen pour les fabricants de prouver qu'ils respectent les exigences générales en matière de sécurité et de performances et les autres exigences légales, notamment celles relatives à la gestion de la qualité et des risques, énoncées dans le présent règlement. |
(21) |
La directive 98/79/CE permet à la Commission d'adopter des spécifications techniques communes pour certaines catégories de dispositifs médicaux de diagnostic in vitro. Dans les domaines dans lesquels il n'existe pas de normes harmonisées ou dans lesquels les normes harmonisées sont insuffisantes, il convient de conférer à la Commission le pouvoir de définir des spécifications communes permettant de garantir la conformité avec les exigences générales en matière de sécurité et de performances et avec les exigences applicables aux études des performances et à l'évaluation des performances et/ou au suivi après commercialisation, telles qu'elles sont énoncées dans le présent règlement. |
(22) |
Des spécifications communes devraient être élaborées après consultation des parties prenantes concernées et compte tenu des normes européennes et internationales. |
(23) |
La réglementation régissant les dispositifs devrait, s'il y a lieu, être alignée sur le nouveau cadre législatif applicable à la commercialisation des produits, lequel se compose du règlement (CE) no 765/2008 du Parlement européen et du Conseil et de la décision no 768/2008/CE du Parlement européen et du Conseil. |
(24) |
Les modalités de surveillance du marché de l'Union et de contrôle des produits entrant sur le marché de l'Union établies par le règlement (CE) no 765/2008 s'appliquent aux dispositifs relevant du présent règlement, ce qui n'empêche pas les États membres de confier ces tâches aux autorités compétentes de leur choix. |
(25) |
Il convient d'énoncer clairement les obligations générales des différents opérateurs économiques, dont les importateurs et les distributeurs, en s'inspirant du nouveau cadre législatif applicable à la commercialisation des produits, sans préjudice des obligations particulières énoncées dans les différentes parties du présent règlement, de manière à permettre aux opérateurs concernés de mieux comprendre les exigences énoncées dans le présent règlement et donc de mieux s'y conformer. |
(26) |
Aux fins du présent règlement, les activités des distributeurs sont censées comprendre l'acquisition, la détention et l'offre de dispositifs. |
(27) |
Plusieurs des obligations incombant aux fabricants, comme l'évaluation des performances ou les notifications dans le cadre de la vigilance, qui n'étaient établies que dans les annexes de la directive 98/79/CE, devraient être intégrées aux dispositions du présent règlement afin d'en faciliter l'application. |
(28) |
Il convient, pour garantir un niveau de protection de la santé le plus élevé possible, de clarifier et de renforcer les dispositions régissant les dispositifs médicaux de diagnostic in vitro qui sont à la fois fabriqués et utilisés dans un seul et même établissement de santé. Cette utilisation devrait être entendue comme comprenant les mesures et les résultats produits. |
(29) |
Les établissements de santé devraient avoir la possibilité, sans faire l'objet de toutes les exigences du présent règlement, de fabriquer, de modifier et d'utiliser des dispositifs en interne et de répondre ainsi, à une échelle non industrielle, aux besoins spécifiques des groupes cibles de patients qui ne peuvent pas être satisfaits au niveau de performances approprié par un dispositif équivalent disponible sur le marché. Dans ce contexte, il convient de prévoir que certaines règles du présent règlement concernant les dispositifs fabriqués et utilisés uniquement dans les établissements de santé, notamment des hôpitaux ainsi que des établissements tels que des laboratoires et des instituts de santé publique qui contribuent au système de soins de santé et/ou répondent aux besoins des patients, sans assurer directement leur traitement ou leur prise en charge, ne devraient pas s'appliquer, étant donné que les objectifs du présent règlement continueraient d'être atteints de manière proportionnée. Aux fins du présent règlement, il convient de noter que le concept d'établissement de santé ne couvre pas les établissements dont l'objet principal est d'encourager la santé et des modes de vie sains, tels que les centres de gymnastique, de remise en forme, de bienêtre ou de culture physique. Par conséquent, l'exemption prévue pour les établissements de santé ne s'applique pas aux établissements susmentionnés. |
(30) |
Étant donné que les personnes physiques ou morales peuvent demander réparation pour des dommages causés par un dispositif défectueux conformément à la législation de l'Union et à la législation nationale applicables, il convient d'exiger des fabricants qu'ils aient pris des mesures pour disposer d'une couverture financière suffisante au regard de leur éventuelle responsabilité en application de la directive 85/374/CEE du Conseil. Les mesures en question devraient être proportionnées à la classe de risque, au type de dispositif et à la taille de l'entreprise. Dans ce contexte, il convient également d'établir des règles permettant à une autorité compétente de faciliter la fourniture d'informations aux personnes qui pourraient avoir subi des dommages du fait d'un dispositif défectueux. |
(31) |
Pour garantir que les dispositifs fabriqués en série demeurent conformes aux exigences du présent règlement et que l'expérience tirée de leur utilisation est prise en compte dans le procédé de production, il convient que tous les fabricants disposent d'un système de gestion de la qualité et d'un système de surveillance après commercialisation proportionnés à la classe de risque et au type de dispositif en question. En outre, afin de minimiser les risques ou de prévenir les incidents impliquant des dispositifs, les fabricants devraient mettre en place un système de gestion des risques ainsi qu'un système de notification des incidents et des mesures correctives de sécurité. |
(32) |
Le système de gestion des risques devrait être soigneusement aligné sur le processus d'évaluation des performances pour le dispositif, et pris en compte dans celui-ci, y compris en ce qui concerne les risques cliniques à prendre en considération dans le cadre des études des performances, de l'évaluation des performances et du suivi après commercialisation. Le processus de gestion des risques et le processus d'évaluation des performances devraient être interdépendants et être mis à jour régulièrement. |
(33) |
Il convient de faire en sorte que la surveillance et le contrôle de la fabrication des dispositifs ainsi que la surveillance consécutive à leur commercialisation et les activités de vigilance les concernant soient assurés par un membre du personnel du fabricant chargé de veiller au respect de la règlementation et répondant à des conditions minimales de qualification. |
(34) |
Pour les fabricants qui ne sont pas établis dans l'Union, le mandataire joue un rôle capital en ce sens qu'il veille à la conformité des dispositifs produits par ces fabricants et sert à ces derniers de point de contact dans l'Union. Compte tenu de ce rôle capital, il convient, aux fins de l'application des règles, que le mandataire soit juridiquement responsable des dispositifs défectueux au cas où un fabricant établi en dehors de l'Union n'a pas satisfait à ses obligations générales. La responsabilité du mandataire prévue dans le présent règlement est sans préjudice des dispositions de la directive 85/374/CEE et, par conséquent, le mandataire, l'importateur et le fabricant devraient être solidairement responsables. Les tâches du mandataire devraient être définies dans un mandat écrit. Compte tenu du rôle des mandataires, il y a lieu de définir clairement les obligations minimales auxquelles ils doivent satisfaire, entre autres l'obligation de disposer d'une personne remplissant des conditions de qualification minimales qui devraient être similaires à celles applicables au membre du personnel du fabricant chargé de veiller au respect de la règlementation. |
(35) |
Pour garantir la sécurité juridique en ce qui concerne les obligations incombant aux opérateurs économiques, il est nécessaire de préciser dans quels cas un distributeur, un importateur ou un tiers doit être considéré comme le fabricant d'un dispositif. |
(36) |
Le commerce parallèle de produits déjà mis sur le marché est une forme légale de commerce au sein du marché intérieur sur le fondement de l'article 34 du traité sur le fonctionnement de l'Union européenne, sous réserve des limites découlant de la nécessité de protéger la santé et la sécurité et de protéger les droits de propriété intellectuelle prévues à l'article 36 du traité sur le fonctionnement de l'Union européenne. L'application de ce principe de commerce parallèle fait toutefois l'objet d'interprétations différentes dans les États membres. Il convient dès lors de préciser dans le présent règlement les conditions, et notamment les exigences en matière de réétiquetage et de reconditionnement, compte tenu de la jurisprudence de la Cour de justice dans d'autres secteurs concernés et des bonnes pratiques appliquées dans le domaine des dispositifs médicaux de diagnostic in vitro. |
(37) |
D'une manière générale, le marquage CE devrait être apposé sur les dispositifs pour indiquer leur conformité avec le présent règlement afin qu'ils puissent circuler librement dans l'Union et être mis en service conformément à leur destination. Les États membres devraient s'abstenir de créer des entraves à la mise sur le marché ou à la mise en service de dispositifs conformes aux exigences du présent règlement. Néanmoins, les États membres devraient être autorisés à décider s'il y a lieu de restreindre l'utilisation de tout type particulier de dispositif en ce qui concerne des aspects ne relevant pas du présent règlement. |
(38) |
La traçabilité des dispositifs au moyen d'un système d'identification unique des dispositifs (ci-après dénommé «système IUD») fondé sur des lignes directrices internationales devrait accroître considérablement l'efficacité des activités liées à la sécurité après commercialisation pour les dispositifs, grâce à une meilleure notification des incidents, à des mesures correctives de sécurité ciblées et à un meilleur contrôle par les autorités compétentes. Elle devrait aussi contribuer à réduire le nombre d'erreurs médicales et à lutter contre les dispositifs falsifiés. L'utilisation du système IUD devrait également améliorer les politiques d'achat et d'élimination des déchets ainsi que la gestion des stocks par les établissements de santé et d'autres opérateurs économiques et, si possible, être compatible avec d'autres systèmes d'authentification déjà présents dans ces lieux. |
(39) |
Le système IUD devrait s'appliquer à tous les dispositifs mis sur le marché, à l'exception des dispositifs devant faire l'objet d'une étude des performances, et s'appuyer sur des principes internationalement reconnus, y compris des définitions compatibles avec celles qui sont utilisées par les principaux partenaires commerciaux. Afin que le système IUD devienne opérationnel en temps utile pour l'application du présent règlement, il convient d'établir des modalités détaillées dans le présent règlement et dans le règlement (UE) 2017/745 du Parlement européen et du Conseil. |
(40) |
La transparence et un accès approprié à l'information, présentée de manière adéquate à l'utilisateur auquel le dispositif est destiné, sont essentiels dans l'intérêt général, pour protéger la santé publique, pour donner davantage d'autonomie aux patients et aux professionnels de la santé et leur permettre de prendre des décisions en connaissance de cause, pour fournir une base robuste à la prise de décisions en matière de réglementation et pour faire en sorte que le système de réglementation inspire confiance. |
(41) |
Un aspect primordial de la réalisation des objectifs du présent règlement est la création d'une base de données européenne sur les dispositifs médicaux (Eudamed) qui devrait intégrer plusieurs systèmes électroniques pour rassembler et traiter les informations relatives aux dispositifs présents sur le marché et aux opérateurs économiques concernés, à certains aspects de l'évaluation de la conformité, aux organismes notifiés, aux certificats, aux études des performances, à la vigilance et à la surveillance du marché. La base de données devrait permettre d'accroître la transparence générale, notamment grâce à un meilleur accès à l'information pour le public et les professionnels de la santé, d'éviter les obligations de notification multiples, de renforcer la coordination entre les États membres et de rationaliser et de faciliter l'échange d'informations entre les opérateurs économiques, les organismes notifiés ou les promoteurs et les États membres, ainsi qu'entre les États membres et entre eux et la Commission. Étant donné que, sur le marché intérieur, cette démarche ne peut être menée efficacement qu'à l'échelle de l'Union, la Commission devrait étoffer et gérer la banque de données européenne sur les dispositifs médicaux instituée par la décision 2010/227/UE de la Commission. |
(42) |
Afin de faciliter le fonctionnement de la banque de données européenne sur les dispositifs médicaux (Eudamed), une nomenclature des dispositifs médicaux qui soit internationalement reconnue devrait être mise gratuitement à la disposition des fabricants et des autres personnes physiques ou morales qui sont tenues par le présent règlement d'utiliser cette nomenclature. En outre, cette nomenclature devrait également être mise à disposition gratuitement, dans la mesure où cela est raisonnablement possible, aux autres intervenants. |
(43) |
Il convient que les systèmes électroniques d'Eudamed relatifs aux dispositifs présents sur le marché, aux opérateurs économiques concernés et aux certificats permettent au public d'être bien informé des dispositifs présents sur le marché de l'Union. Le système électronique relatif aux études des performances devrait servir d'outil de coopération entre les États membres et permettre aux promoteurs d'introduire, volontairement, une demande unique pour plusieurs États membres et de notifier les événements indésirables graves, les défectuosités de dispositifs et les mises à jour y afférentes. Le système électronique relatif à la vigilance devrait permettre aux fabricants de notifier les incidents graves et autres événements à signaler, et faciliter la coordination de l'évaluation de ceux-ci par les autorités compétentes. Le système électronique relatif à la surveillance du marché devrait servir à l'échange d'informations entre les autorités compétentes. |
(44) |
En ce qui concerne les données rassemblées et traitées par les systèmes électroniques d'Eudamed, la directive 95/46/CE13 du Parlement européen et du Conseil régit le traitement de données à caractère personnel effectué dans les États membres, sous la surveillance des autorités compétentes de ceux-ci, en particulier les autorités publiques indépendantes qu'ils ont désignées. Le règlement (CE) no 45/2001 du Parlement européen et du Conseil régit le traitement de données à caractère personnel effectué par la Commission dans le cadre du présent règlement, sous la surveillance du Contrôleur européen de la protection des données. Conformément au règlement (CE) no 45/2001, la Commission devrait être désignée comme responsable du traitement des données pour Eudamed et ses systèmes électroniques. |
(45) |
Pour les dispositifs de classe C et D, il convient que les fabricants résument les principaux aspects liés à la sécurité et aux performances de ces dispositifs et les résultats de l'évaluation des performances dans un document destiné à être rendu public. |
(46) |
Le bon fonctionnement des organismes notifiés est indispensable pour garantir un niveau élevé de protection de la santé et de la sécurité ainsi que la confiance des citoyens dans le système. La désignation et le contrôle des organismes notifiés par les États membres, selon des critères précis et stricts, devraient dès lors être supervisés à l'échelle de l'Union. |
(47) |
Les évaluations de la documentation technique des fabricants, en particulier de la documentation concernant l'évaluation des performances, réalisées par les organismes notifiés devraient faire l'objet d'une évaluation critique par l'autorité responsable des organismes notifiés. Cette évaluation devrait s'inscrire dans le cadre de l'approche fondée sur les risques appliquée pour la surveillance et le contrôle des activités des organismes notifiés et devrait être fondée sur un échantillonnage de la documentation concernée. |
(48) |
Il convient de renforcer la position des organismes notifiés par rapport aux fabricants, notamment pour ce qui est du droit et de l'obligation qui sont les leurs d'effectuer des audits sur place inopinés et de soumettre les dispositifs à des essais physiques ou en laboratoire pour s'assurer que les fabricants continuent de respecter la réglementation après réception du certificat initial. |
(49) |
Afin que la surveillance des organismes notifiés exercée par les autorités nationales soit plus transparente, les autorités responsables des organismes notifiés devraient publier des informations sur les mesures nationales régissant l'évaluation, la désignation et le contrôle des organismes notifiés. Conformément aux bonnes pratiques administratives, ces autorités devraient tenir ces informations à jour, en particulier pour prendre en compte les modifications pertinentes, marquantes ou substantielles apportées aux procédures en question. |
(50) |
L'État membre dans lequel est établi un organisme notifié devrait être responsable du respect des exigences du présent règlement pour ce qui concerne cet organisme notifié. |
(51) |
Compte tenu, en particulier, de la responsabilité qui leur incombe en matière d'organisation et de fourniture des services de santé et des soins médicaux, les États membres devraient être autorisés à imposer aux organismes notifiés désignés pour évaluer la conformité des dispositifs qui sont établis sur leur territoire des exigences supplémentaires concernant les questions qui ne sont pas régies par le présent règlement. Toute exigence supplémentaire de ce type ne saurait avoir une incidence sur des textes législatifs horizontaux de l'Union plus spécifiques concernant les organismes notifiés et l'égalité de traitement desdits organismes. |
(52) |
Pour les dispositifs de classe D, il convient que les autorités compétentes soient informées des certificats délivrés par les organismes notifiés et aient le droit de contrôler l'évaluation réalisée par les organismes notifiés. |
(53) |
Pour les dispositifs de classe D pour lesquels il n'existe pas de spécifications communes, il convient de prévoir, lorsqu'il s'agit de la première certification pour ce type spécifique de dispositif et qu'il n'existe pas de dispositif similaire sur le marché ayant la même destination et reposant sur une technologie similaire, les organismes notifiés devraient, en plus de la vérification par des laboratoires de référence de l'UE, au moyen d'essais de laboratoire, des performances alléguées par le fabricant et de la conformité des dispositifs, être tenus de demander à des groupes d'experts de contrôler leurs rapports d'évaluation sur l'évaluation des performances. La consultation de groupes d'experts en ce qui concerne l'évaluation des performances devrait permettre une évaluation harmonisée des dispositifs médicaux de diagnostic in vitro à haut risque grâce au partage de l'expertise sur les aspects liés aux performances cliniques et à l'élaboration de spécifications communes concernant les catégories de dispositifs ayant fait l'objet de cette procédure de consultation. |
(54) |
Pour accroître la sécurité des patients et tenir dûment compte des progrès technologiques, il convient de modifier fondamentalement le système actuel de classification des dispositifs établi dans la directive 98/79/CE, de manière à l'aligner sur les pratiques internationales, et d'adapter en conséquence les procédures d'évaluation de la conformité correspondantes. |
(55) |
Il est nécessaire, en particulier aux fins des procédures d'évaluation de la conformité, de répertorier les dispositifs en quatre classes de risque et d'établir un ensemble de règles de classification robustes fondées sur les risques, conformément aux pratiques internationales. |
(56) |
En règle générale, la procédure d'évaluation de la conformité des dispositifs de classe A devrait relever de la seule responsabilité des fabricants, vu le faible risque que ces dispositifs présentent pour les patients. Pour les dispositifs des classes B, C et D, il y a lieu d'imposer un degré approprié d'intervention d'un organisme notifié. |
(57) |
Il convient de renforcer et de rationaliser davantage les procédures d'évaluation de la conformité des dispositifs et de définir clairement les modalités d'évaluation que les organismes notifiés sont tenus d'appliquer, de manière à garantir des conditions équitables. |
(58) |
Il convient que les certificats de libre vente contiennent des informations permettant d'utiliser Eudamed afin d'obtenir des informations sur le dispositif concerné, en particulier de savoir s'il est sur le marché, s'il a été retiré du marché ou s'il a été rappelé, ainsi que sur tout certificat de conformité le concernant. |
(59) |
Il est nécessaire de clarifier les obligations en matière de vérification de la libération de lots de dispositifs de la classe de risque la plus élevée. |
(60) |
Il convient de permettre aux laboratoires de référence de l'UE de vérifier par essai en laboratoire les performances alléguées par le fabricant et la conformité des dispositifs présentant le risque le plus élevé aux spécifications communes applicables, dès lors qu'il en existe, ou aux autres solutions retenues par les fabricants pour garantir un niveau de sécurité et de performances au moins équivalent. |
(61) |
Pour garantir un niveau élevé de sécurité et de performances, il convient que le respect des exigences générales en matière de sécurité et de performances énoncées dans le présent règlement soit démontré sur la base de preuves cliniques. Il est nécessaire de clarifier les modalités de démonstration de ces preuves cliniques, qui repose sur des données concernant la validité scientifique ainsi que sur les performances analytiques et les performances cliniques du dispositif. Pour que le processus puisse être structuré et transparent et qu'il livre des données fiables et robustes, l'obtention et l'évaluation des informations scientifiques disponibles ainsi que des données fournies par les études des performances devraient être fondées sur un plan d'évaluation des performances. |
(62) |
En règle générale, les preuves cliniques devraient provenir d'études des performances réalisées sous la responsabilité d'un promoteur. Le fabricant et une autre personne physique ou morale devraient pouvoir être le promoteur qui assume la responsabilité de l'étude des performances. |
(63) |
Il est nécessaire de veiller à ce que les preuves cliniques des dispositifs soient mises à jour tout au long du cycle de vie des dispositifs. Cela suppose que le fabricant planifie un suivi des progrès scientifiques et de l'évolution des pratiques médicales. Toute nouvelle information pertinente devrait alors donner lieu à une réévaluation des preuves cliniques du dispositif afin d'en garantir la sécurité et les performances au moyen d'un processus continu d'évaluation des performances. |
(64) |
Il convient d'être conscient du fait que, pour les dispositifs médicaux de diagnostic in vitro, la notion de bénéfices cliniques est fondamentalement différente de celle qui s'applique dans le cas des médicaments ou des dispositifs médicaux thérapeutiques, car les bénéfices des dispositifs médicaux de diagnostic in vitro résident dans la communication d'informations médicales précises concernant les patients, évaluées le cas échéant par rapport à des informations médicales obtenues au moyen d'autres solutions et technologies de diagnostic, le résultat clinique définitif pour le patient dépendant d'autres solutions diagnostiques et/ou thérapeutiques qui pourraient être disponibles. |
(65) |
Lorsqu'il n'existe pas de performance analytique ou clinique pour des dispositifs spécifiques ou lorsqu'aucune exigence spécifique ne s'applique en matière de performances, il y a lieu de justifier dans le plan d'évaluation des performances, ainsi que dans les rapports connexes, les omissions concernant ces exigences. |
(66) |
Les dispositions régissant les études des performances devraient être conformes aux lignes directrices internationales bien établies dans ce domaine, telles que la norme internationale ISO 14155:2011 sur les bonnes pratiques cliniques en matière d'investigation clinique des dispositifs médicaux pour sujets humains, afin que les résultats des études des performances menées dans l'Union puissent être plus facilement acceptés ailleurs comme documentation et que les résultats des études des performances menées hors de l'Union conformément aux lignes directrices internationales puissent être plus facilement acceptés dans l'Union. En outre, ces dispositions devraient être alignées sur la dernière version de la déclaration d'Helsinki de l'Association médicale mondiale sur les principes éthiques applicables à la recherche médicale impliquant des êtres humains. |
(67) |
Il convient de laisser à l'État membre dans lequel une étude des performances doit être réalisée, le soin de désigner l'autorité appropriée participant à l'évaluation de la demande de conduite d'une étude des performances ainsi que d'organiser la participation de comités d'éthique dans les délais fixés par le présent règlement pour l'autorisation d'une étude des performances. De telles décisions relèvent de l'organisation interne de chaque État membre. À cet égard, les États membres devraient garantir la participation de profanes, en particulier de patients ou d'organisations de patients. Ils devraient également veiller à ce que l'expertise nécessaire soit disponible. |
(68) |
Il convient de mettre en place un système électronique à l'échelle de l'Union pour que toute étude interventionnelle des performances cliniques et toute autre étude des performances présentant des risques pour les participants aux études soit enregistrée et notifiée dans une base de données rendue publique. Dans un souci de préservation du droit à la protection des données à caractère personnel, consacré à l'article 8 de la Charte des droits fondamentaux de l'Union européenne (ci-après dénommée «Charte»), les données à caractère personnel des participants à une étude des performances ne devraient pas être enregistrées dans le système électronique. Pour créer des synergies avec les essais cliniques de médicaments, le système électronique relatif aux études des performances et la base de données de l'UE qui doit être établie pour les essais cliniques sur les médicaments à usage humain devraient être interopérables. |
(69) |
Lorsqu'une étude interventionnelle des performances cliniques ou une autre étude des performances présentant des risques pour les participants doit être réalisée dans plusieurs États membres, le promoteur devrait avoir la possibilité d'introduire une demande unique de manière à réduire la charge administrative. Pour permettre le partage des ressources et garantir la cohérence de l'évaluation des éléments liés à la santé et à la sécurité que présente le dispositif faisant l'objet d'une étude des performances ainsi que du modèle scientifique sur lequel repose cette étude des performances, la procédure d'évaluation de cette demande unique devrait être coordonnée entre les États membres sous la direction d'un État membre coordonnateur. Cette évaluation coordonnée ne devrait pas englober l'évaluation des aspects intrinsèquement nationaux, locaux et éthiques de l'étude des performances, comme le consentement éclairé. Pendant une période initiale de sept ans à compter de la date d'application du présent règlement, les États membres devraient être en mesure de participer à l'évaluation coordonnée sur une base volontaire. À l'issue de cette période, tous les États membres devraient être tenus de participer à l'évaluation coordonnée. La Commission, sur la base des enseignements tirés de cette coordination volontaire entre les États membres, devrait établir un rapport sur l'application des dispositions pertinentes relatives à la procédure d'évaluation coordonnée. Si les conclusions du rapport sont négatives, la Commission devrait présenter une proposition en vue de prolonger la période de participation volontaire à la procédure d'évaluation coordonnée. |
(70) |
Il convient que les promoteurs notifient aux États membres dans lesquels sont en cours des études interventionnelles des performances cliniques et autres études des performances présentant des risques pour les participants, certains événements indésirables et défectuosités de dispositifs survenant durant ces études. Les États membres devraient avoir la possibilité d'arrêter ou de suspendre les études ou de révoquer l'autorisation relative auxdites études s'ils le jugent nécessaire pour garantir un niveau élevé de protection des participants à celles-ci. Ces informations devraient être communiquées aux autres États membres. |
(71) |
Le promoteur d'une étude des performances devrait transmettre un résumé des résultats de l'étude des performances qui soit aisément compréhensible par l'utilisateur auquel le dispositif est destiné en même temps que le rapport sur l'étude des performances, le cas échéant, dans les délais prévus par le présent règlement. Lorsqu'il n'est pas possible, pour des raisons scientifiques, de transmettre le résumé des résultats dans les délais prévus, le promoteur devrait le justifier et préciser quand les résultats seront transmis. |
(72) |
À l'exception de certaines exigences générales, le présent règlement ne devrait porter que sur les études des performances destinées à recueillir des données scientifiques aux fins de démontrer la conformité d'un dispositif. |
(73) |
Il est nécessaire de préciser que les études des performances utilisant des échantillons restants ne sont pas soumises à autorisation. Néanmoins, il convient que les exigences générales et autres exigences supplémentaires concernant la protection des données et les exigences applicables aux procédures établies conformément à la législation nationale, telles que l'examen éthique, continuent de s'appliquer à toutes les études des performances, y compris celles utilisant des échantillons restants. |
(74) |
Il y a lieu d'observer les principes de remplacement, de réduction et de raffinement dans le domaine de l'expérimentation animale énoncés dans la directive 2010/63/UE du Parlement européen et du Conseil. En particulier, il convient d'éviter de répéter inutilement des essais et des études. |
(75) |
Les fabricants devraient jouer un rôle actif durant la phase après commercialisation en collectant systématiquement et activement des informations concernant l'utilisation de leurs dispositifs après leur commercialisation, afin de mettre à jour leur documentation technique et de coopérer avec les autorités nationales compétentes chargées des activités de vigilance et de surveillance du marché. À cette fin, les fabricants devraient établir un système global de surveillance après commercialisation, mis en place dans le cadre de leur système de gestion de la qualité et fondé sur un plan de surveillance après commercialisation. Les données et les informations pertinentes collectées grâce à la surveillance après commercialisation, ainsi que les enseignements tirés des mesures préventives et/ou correctives mises en œuvre, devraient être utilisés pour mettre à jour toute partie pertinente de la documentation technique, concernant par exemple l'évaluation des risques et l'évaluation des performances, et devraient également servir l'objectif de transparence. |
(76) |
Pour mieux protéger la santé et mieux préserver la sécurité des dispositifs présents sur le marché, il convient d'améliorer l'efficacité du système électronique de vigilance relatif aux dispositifs en créant un portail centralisé au niveau de l'Union permettant de notifier les incidents graves et les mesures correctives de sécurité. |
(77) |
Les États membres devraient prendre des mesures appropriées pour sensibiliser les professionnels de la santé, les utilisateurs et les patients à l'importance de notifier les incidents. Il y a lieu d'encourager les professionnels de la santé, les utilisateurs et les patients et de leur permettre de notifier les incidents graves supposés au niveau national selon des modalités harmonisées. Les autorités nationales compétentes devraient informer les fabricants de tout incident grave supposé et, lorsqu'un fabricant confirme la survenance dudit incident, les autorités concernées devraient veiller au suivi approprié, de manière à réduire au minimum la récurrence de ces incidents. |
(78) |
L'évaluation des incidents graves et des mesures correctives de sécurité notifiés devraient être menée au niveau national mais il faudrait assurer une coordination lorsque des incidents similaires sont survenus ou que des mesures correctives de sécurité doivent être mises en œuvre dans plusieurs États membres, avec pour objectif de partager les ressources et de garantir la cohérence des mesures correctives. |
(79) |
Dans le cadre de l'investigation des incidents, les autorités compétentes devraient tenir compte, le cas échéant, des informations et des avis émanant des parties prenantes concernées, y compris les organisations de patients et de professionnels de la santé et les associations de fabricants. |
(80) |
Il y a lieu de bien faire la distinction entre la notification d'événements indésirables graves ou de défectuosités de dispositifs survenant pendant les études interventionnelles des performances cliniques et autres études des performances présentant des risques pour les participants et la notification d'incidents graves postérieurs à la mise sur le marché d'un dispositif, afin d'éviter les doubles notifications. |
(81) |
Il convient que le présent règlement prévoie des règles en matière de surveillance du marché pour renforcer les droits et obligations des autorités nationales compétentes, garantir la coordination effective de leurs activités en matière de surveillance du marché et clarifier les procédures applicables. |
(82) |
Toute progression statistiquement significative du nombre ou de la sévérité des incidents qui ne sont pas des incidents graves ou des résultats erronés attendus susceptibles d'avoir une incidence significative sur l'analyse du rapport bénéfice/risque et d'entraîner des risques inacceptables devrait être notifiée aux autorités compétentes afin d'en permettre l'évaluation ainsi que l'adoption de mesures appropriées. |
(83) |
Il convient d'instituer un comité d'experts, le GCDM, composé de personnes désignées par les États membres pour leur fonction et leur expertise dans le domaine des dispositifs médicaux, y compris des dispositifs médicaux de diagnostic in vitro, conformément aux conditions et modalités définies dans le règlement (UE) 2017/745, afin qu'il s'acquitte des tâches qui lui sont confiées par le présent règlement et par le règlement (UE) 2017/745, qu'il conseille la Commission et qu'il aide celle-ci et les États membres à assurer une application harmonisée du présent règlement. Le GCDM devrait être en mesure de créer des sous-groupes afin d'avoir accès à l'expertise technique approfondie nécessaire dans le domaine des dispositifs médicaux, y compris des dispositifs médicaux de diagnostic in vitro. Lors de la création de sous-groupes, il convient d'envisager la possibilité d'associer des groupes actifs au niveau de l'Union dans le domaine des dispositifs médicaux. |
(84) |
Une coordination plus étroite entre les autorités nationales compétentes grâce à l'échange d'informations et à des évaluations coordonnées sous la direction d'une autorité coordonnatrice est essentielle pour que la protection de la santé et la sécurité soient constamment à un niveau élevé dans le marché intérieur, notamment dans les domaines des études des performances et de la vigilance. Le principe consistant à coordonner les échanges et les évaluations devrait également s'appliquer à d'autres activités des autorités décrites dans le présent règlement, notamment la désignation des organismes notifiés, et devrait être encouragé dans le domaine de la surveillance des dispositifs présents sur le marché. Travailler ensemble, se coordonner et communiquer au sujet des activités devrait également permettre d'utiliser plus efficacement les ressources et l'expertise au niveau national. |
(85) |
Il convient que la Commission fournisse une aide scientifique, technique et logistique aux autorités nationales coordonnatrices et fasse en sorte que le système de réglementation des dispositifs soit effectivement et uniformément appliqué à l'échelle de l'Union sur la base de données scientifiques rigoureuses. |
(86) |
Il y a lieu que l'Union et, le cas échéant, les États membres participent activement à la coopération internationale en matière de réglementation des dispositifs afin de faciliter l'échange d'informations sur la sécurité des dispositifs et de contribuer à l'élaboration de lignes directrices internationales en matière de réglementation qui inciteront d'autres juridictions à adopter des règles garantissant un niveau de protection de la santé et de sécurité équivalent à celui établi par le présent règlement. |
(87) |
Les États membres devraient prendre toutes les mesures nécessaires pour veiller à ce que les dispositions du présent règlement soient mises en œuvre et, notamment, prévoir des sanctions effectives, proportionnées et dissuasives en cas de violation de ces dispositions. |
(88) |
Même si le présent règlement devrait être sans effet sur le droit qu'ont les États membres de percevoir des redevances pour les activités menées au niveau national, il convient, pour des raisons de transparence, que les États membres informent la Commission et les autres États membres avant qu'ils ne décident du montant et de la structure de ces redevances. Afin d'accroître encore la transparence, la structure et le montant des redevances devraient être rendus publics sur demande. |
(89) |
Le présent règlement respecte les droits fondamentaux et les principes reconnus en particulier par la Charte et, spécialement, la dignité humaine, l'intégrité de la personne, la protection des données à caractère personnel, la liberté des arts et des sciences, la liberté d'entreprise et le droit de propriété. Il convient que le présent règlement soit appliqué par les États membres conformément à ces droits et principes. |
(90) |
Il convient de déléguer à la Commission le pouvoir d'adopter des actes délégués conformément à l'article 290 du traité sur le fonctionnement de l'Union européenne pour modifier certains éléments non essentiels du présent règlement. Il importe particulièrement que la Commission procède aux consultations appropriées durant son travail préparatoire, y compris au niveau des experts, et que ces consultations soient menées conformément aux principes définis dans l'accord interinstitutionnel du 13 avril 2016«Mieux légiférer». En particulier, pour assurer leur égale participation à la préparation des actes délégués, le Parlement européen et le Conseil reçoivent tous les documents au même moment que les experts des États membres, et leurs experts ont systématiquement accès aux réunions des groupes d'experts de la Commission traitant de la préparation des actes délégués. |
(91) |
Afin d'assurer des conditions uniformes d'exécution du présent règlement, il convient de conférer des compétences d'exécution à la Commission. Ces compétences devraient être exercées en conformité avec le règlement (UE) no 182/2011 du Parlement européen et du Conseil. |
(92) |
Il convient d'avoir recours à la procédure consultative pour les actes d'exécution qui définissent la forme et la présentation des données devant figurer dans les résumés des caractéristiques de sécurité et des performances établis par le fabricant et qui déterminent le modèle pour les certificats de libre vente, étant donné que ces actes d'exécution sont de nature procédurale et n'ont pas d'incidence directe sur la santé et la sécurité dans l'Union. |
(93) |
La Commission devrait adopter des actes d'exécution immédiatement applicables lorsque, dans des cas dûment justifiés liés à l'extension au territoire de l'Union d'une dérogation nationale aux procédures d'évaluation de la conformité, des raisons d'urgence impérieuses le requièrent. |
(94) |
Afin de lui permettre de désigner les entités d'attribution et les laboratoires de référence de l'UE, il convient de conférer à la Commission des compétences d'exécution. |
(95) |
Pour permettre aux opérateurs économiques, en particulier les PME, aux organismes notifiés, aux États membres et à la Commission de s'adapter aux modifications introduites par le présent règlement et pour veiller à la bonne application de celui-ci, il convient de prévoir une période de transition suffisante pour leur donner le temps de s'adapter et de prendre les mesures d'organisation nécessaires. Néanmoins, certaines parties du règlement qui concernent directement les États membres et la Commission devraient être mises en œuvre dès que possible. Il importe aussi tout particulièrement qu'un nombre suffisant d'organismes notifiés soit désigné conformément aux nouvelles dispositions au moment de la mise en application du présent règlement afin d'éviter toute pénurie de dispositifs sur le marché. Néanmoins, il faut que toute désignation d'un organisme notifié conformément aux dispositions du présent règlement avant la date de sa mise en application soit sans préjudice de la validité de la désignation de ces organismes au titre de la directive 98/79/CE et de leur capacité à continuer à délivrer des certificats valides au titre de ladite directive jusqu'à la date d'application du présent règlement. |
(96) |
Pour que la transition vers de nouvelles règles en matière d'enregistrement des dispositifs et des certificats se fasse sans heurts, il convient, si les systèmes informatiques correspondants sont développés conformément au calendrier prévu, que les obligations de transmission des informations pertinentes aux systèmes électroniques mis en place au niveau de l'Union conformément au présent règlement ne prennent pleinement effet que dix-huit mois après la date d'application du présent règlement. Durant cette période transitoire, certaines dispositions de la directive 98/79/CE devraient rester en vigueur. Toutefois, afin d'éviter les enregistrements multiples, les opérateurs économiques et les organismes notifiés qui s'enregistrent dans les systèmes électroniques pertinents mis en place au niveau de l'Union conformément au présent règlement devraient être réputés satisfaire aux obligations d'enregistrement imposées par les États membres en application de ces dispositions. |
(97) |
Afin de permettre une introduction harmonieuse du système IUD, la date d'application de l'obligation d'apposer le support IUD sur l'étiquette du dispositif devrait varier de un à cinq ans à compter de la date d'application du présent règlement, en fonction de la classe à laquelle appartient le dispositif concerné. |
(98) |
Il y a lieu d'abroger la directive 98/79/CE de manière à ce qu'un seul et même ensemble de règles régisse la mise sur le marché de dispositifs médicaux de diagnostic in vitro et les aspects connexes faisant l'objet du présent règlement. Néanmoins, il convient de continuer d'appliquer les obligations des fabricants concernant la mise à disposition de la documentation relative aux dispositifs qu'ils ont mis sur le marché ainsi que les obligations des fabricants et des États membres concernant les activités de vigilance pour les dispositifs mis sur le marché au titre de la directive susmentionnée. Bien qu'il convienne de laisser aux États membres le soin de décider de la manière d'organiser les activités de vigilance, il est souhaitable qu'ils aient la possibilité de notifier les incidents indésirables liés aux dispositifs mis sur le marché au titre de ladite directive en ayant recours aux mêmes outils que pour la communication relative aux dispositifs mis sur le marché au titre du présent règlement. Cependant, la décision 2010/227/UE adoptée en exécution de la directive susmentionnée et des directives 90/385/CEE et 93/42/CEE du Conseil devrait également être abrogée à compter de la date à laquelle Eudamed deviendra pleinement opérationnelle. |
(99) |
Les exigences du présent règlement devraient s'appliquer à l'ensemble des dispositifs mis sur le marché ou mis en service à compter de sa date d'application. Toutefois, afin de garantir une transition harmonieuse, les dispositifs devraient, pendant une période limitée après cette date, pouvoir être mis sur le marché ou mis en service en vertu d'un certificat valide délivré conformément à la directive 98/79/CE. |
(100) |
Le Contrôleur européen de la protection des données a rendu un avis conformément à l'article 28, paragraphe 2, du règlement (CE) no 45/2001. |
(101) |
Étant donné que les objectifs du présent règlement, à savoir assurer le bon fonctionnement du marché intérieur en ce qui concerne les dispositifs médicaux et garantir des normes de qualité et de sécurité élevées pour les dispositifs médicaux, et donc un niveau élevé de protection de la santé et de la sécurité des patients, des utilisateurs et des autres personnes, ne peuvent pas être atteints de manière suffisante par les États membres mais peuvent, en raison de leur ampleur et de leurs effets, l'être mieux au niveau de l'Union, celle-ci peut prendre des mesures, conformément au principe de subsidiarité consacré à l'article 5 du traité sur l'Union européenne. Conformément au principe de proportionnalité tel qu'énoncé audit article, le présent règlement n'excède pas ce qui est nécessaire pour atteindre ces objectifs, |
ONT ADOPTÉ LE PRÉSENT RÈGLEMENT:
CHAPITRE I
DISPOSITIONS LIMINAIRES
Section I
Champ d'application et définitions
Article premier
Objet et champ d'application
1. Le présent règlement établit des règles concernant la mise sur le marché, la mise à disposition sur le marché ou la mise en service de dispositifs médicaux de diagnostic in vitro à usage humain et de leurs accessoires dans l'Union. Il s'applique également aux études des performances concernant ces dispositifs et leurs accessoires effectuées dans l'Union.
2. Aux fins du présent règlement, les dispositifs médicaux de diagnostic in vitro et leurs accessoires sont dénommés ci-après «dispositifs».
3. Le présent règlement ne régit:
a) |
ni les produits destinés à des usages généraux en laboratoire ni les produits destinés exclusivement à la recherche, à moins que, eu égard à leurs caractéristiques, ces produits soient spécifiquement destinés par leur fabricant à des examens de diagnostic in vitro; |
b) |
ni les produits invasifs destinés à prélever des échantillons ni les produits placés en contact direct avec le corps humain dans le but d'obtenir un échantillon; |
c) |
ni les matériaux de référence certifiés au niveau international; |
d) |
ni les matériaux utilisés dans les programmes d'évaluation externe de la qualité. |
4. Tout dispositif qui, lors de sa mise sur le marché ou de sa mise en service, incorpore comme partie intégrante un dispositif médical au sens de l'article 2, point 1), du règlement (UE) 2017/745 est régi par ledit règlement. Les exigences du présent règlement s'appliquent à la partie constituant le dispositif médical de diagnostic in vitro.
5. Le présent règlement est un acte législatif particulier de l'Union au sens de l'article 2, paragraphe 3, de la directive 2014/30/UE.
6. Les dispositifs qui sont aussi des machines au sens de l'article 2, point a), de la directive 2006/42/CE du Parlement européen et du Conseil sont, en cas de risque au sens de ladite directive, également conformes aux exigences essentielles de santé et de sécurité figurant à l'annexe I de ladite directive, dans la mesure où ces exigences sont plus spécifiques que les exigences générales en matière de sécurité et de performances énoncées à l'annexe I, section II, du présent règlement.
7. Le présent règlement n'a aucune incidence sur l'application de la directive 2013/59/Euratom.
8. Le présent règlement n'a aucune incidence sur le droit d'un État membre de restreindre l'utilisation de tout type particulier de dispositif en ce qui concerne des aspects ne relevant pas du présent règlement.
9. Le présent règlement n'a aucune incidence sur la législation nationale comportant des exigences relatives à l'organisation, à la fourniture et au financement des services de santé et des soins médicaux, prévoyant que certains dispositifs ne peuvent être fournis que sur prescription médicale, que seuls certains professionnels de la santé ou établissements de santé peuvent fournir ou utiliser certains dispositifs ou que leur utilisation doit être accompagnée de conseils professionnels spécifiques.
10. Aucune disposition du présent règlement ne restreint la liberté de la presse ou la liberté d'expression dans les médias dès lors que ces libertés sont garanties dans l'Union et dans les États membres, en particulier en vertu de l'article 11 de la Charte des droits fondamentaux de l'Union européenne.
Article 2
Définitions
Aux fins du présent règlement, on entend par:
1) «dispositif médical», un dispositif médical au sens de l'article 2, point 1), du règlement (UE) 2017/745;
2) «dispositif médical de diagnostic in vitro», tout dispositif médical qui consiste en un réactif, un produit réactif, un matériau d'étalonnage, un matériau de contrôle, une trousse, un instrument, un appareil, un équipement, un logiciel ou un système, utilisé seul ou en association, destiné par le fabricant à être utilisé in vitro dans l'examen d'échantillons provenant du corps humain, y compris les dons de sang et de tissus, uniquement ou principalement dans le but de fournir des informations sur un ou plusieurs des éléments suivants:
a) |
concernant un processus ou état physiologique ou pathologique; |
b) |
concernant des déficiences congénitales physiques ou mentales; |
c) |
concernant la prédisposition à une affection ou à une maladie; |
d) |
permettant de déterminer si un traitement donné est sûr pour des receveurs potentiels et compatible avec eux; |
e) |
permettant de prévoir la réponse ou les réactions à un traitement; |
f) |
permettant de définir ou de contrôler des mesures thérapeutiques. |
Les récipients pour échantillons sont également réputés être des dispositifs médicaux de diagnostic in vitro.
3) «récipient pour échantillons», un dispositif, qu'il soit sous vide ou non, spécifiquement destiné par son fabricant à recevoir directement l'échantillon provenant du corps humain et à le conserver en vue d'un examen de diagnostic in vitro;
4) «accessoire de dispositif médical de diagnostic in vitro», tout article qui, sans être lui-même un dispositif médical de diagnostic in vitro, est destiné par son fabricant à être utilisé avec un ou plusieurs dispositifs médicaux de diagnostic in vitro donnés pour permettre spécifiquement une utilisation de ce ou ces derniers conforme à sa ou leur destination ou pour aider spécifiquement et directement au fonctionnement médical du ou des dispositifs médicaux de diagnostic in vitro selon sa ou leur destination;
5) «dispositif d'autodiagnostic», tout dispositif que le fabricant destine à être utilisé par des profanes, y compris des dispositifs utilisés pour des services de diagnostic fournis à des profanes au moyen de services de la société de l'information;
6) «dispositif de diagnostic près du patient», tout dispositif qui n'est pas destiné à un autodiagnostic mais est destiné à un diagnostic par un professionnel de la santé hors d'un environnement de laboratoire, généralement à proximité ou près du patient;
7) «diagnostic compagnon», tout dispositif essentiel pour une utilisation sûre et efficace d'un médicament donné visant à:
a) |
identifier, avant et/ou pendant le traitement, les patients les plus susceptibles de bénéficier du médicament en question; ou |
b) |
identifier, avant et/ou pendant le traitement, les patients susceptibles de présenter un risque accru d'effets indésirables graves en réaction au traitement par le médicament en question; |
8) «groupe générique de dispositifs», un ensemble de dispositifs destinés à une utilisation identique ou similaire, ou possédant une technologie commune permettant une classification générique de ces dispositifs sans prise en compte de leurs caractéristiques particulières;
9) «dispositif à usage unique», tout dispositif destiné à être utilisé au cours d'une procédure unique;
10) «dispositif falsifié», tout dispositif comportant une fausse présentation de son identité et/ou de sa source et/ou de ses certificats de marquage CE ou des documents relatifs aux procédures de marquage CE. La présente définition n'inclut pas les cas de non-respect non intentionnels et s'entend sans préjudice des violations des droits de propriété intellectuelle;
11) «trousse», un ensemble de composants conditionnés ensemble et destinés à être utilisés pour réaliser un examen de diagnostic in vitro spécifique, ou une partie d'un tel examen;
12) «destination», l'utilisation à laquelle un dispositif est destiné d'après les indications fournies par le fabricant sur l'étiquette, dans la notice d'utilisation ou dans les documents ou indications publicitaires ou de vente, ou celles présentées par le fabricant dans l'évaluation des performances;
13) «étiquette», les informations écrites, imprimées ou graphiques figurant soit sur le dispositif proprement dit, soit sur le conditionnement de chaque unité ou sur le conditionnement de dispositifs multiples;
14) «notice d'utilisation», les indications fournies par le fabricant pour informer l'utilisateur de la destination et de la bonne utilisation d'un dispositif et des précautions à prendre;
15) «identifiant unique des dispositifs» (IUD), une série de chiffres ou de lettres créée selon des normes d'identification et de codification internationales et qui permet l'identification formelle de dispositifs donnés sur le marché;
16) «risque», la combinaison de la probabilité d'un préjudice et de la sévérité de celui-ci;
17) «détermination du rapport bénéfice/risque», l'analyse de toutes les évaluations du bénéfice et du risque susceptibles d'être pertinentes pour l'utilisation du dispositif conformément à la destination donnée par le fabricant;
18) «compatibilité», la capacité d'un dispositif, y compris un logiciel, lorsqu'il est utilisé avec un ou plusieurs autres dispositifs conformément à sa destination, à:
a) |
fonctionner sans perte ni altération de sa capacité à fonctionner comme prévu; et/ou |
b) |
intégrer une modification ou une adaptation de toute composante des dispositifs combinés et/ou fonctionner sans nécessiter une telle modification ou adaptation; et/ou |
c) |
être utilisé avec un autre dispositif sans conflit/interférence ni effet indésirable; |
19) «interopérabilité», la capacité de deux dispositifs médicaux ou plus, y compris des logiciels, du même fabricant ou de fabricants différents, à:
a) |
échanger des informations et utiliser les informations qui ont été échangées aux fins de l'exécution correcte d'une fonction particulière sans modifier le contenu des données; et/ou |
b) |
communiquer l'un avec l'autre; et/ou |
c) |
fonctionner ensemble comme prévu; |
20) «mise à disposition sur le marché», toute fourniture d'un dispositif, autre qu'un dispositif devant faire l'objet d'une étude des performances, destiné à être distribué, consommé ou utilisé sur le marché de l'Union dans le cadre d'une activité commerciale, à titre onéreux ou gratuit;
21) «mise sur le marché», la première mise à disposition d'un dispositif, autre qu'un dispositif devant faire l'objet d'une étude des performances, sur le marché de l'Union;
22) «mise en service», le stade auquel un dispositif, autre qu'un dispositif devant faire l'objet d'une étude des performances, est mis à la disposition de l'utilisateur final, étant prêt à être utilisé pour la première fois sur le marché de l'Union conformément à sa destination;
23) «fabricant», une personne physique ou morale qui fabrique ou remet à neuf un dispositif ou fait concevoir, fabriquer ou remettre à neuf un dispositif, et commercialise ce dispositif sous son nom ou sous sa marque;
24) «remise à neuf», aux fins de la définition du fabricant, la restauration complète d'un dispositif déjà mis sur le marché ou mis en service, ou la confection d'un nouveau dispositif à partir de dispositifs usagés, de manière à le rendre conforme au présent règlement, ainsi que l'attribution d'une nouvelle durée de vie au dispositif remis à neuf;
25) «mandataire», toute personne physique ou morale établie dans l'Union ayant reçu et accepté un mandat écrit d'un fabricant, situé hors de l'Union, pour agir pour le compte du fabricant aux fins de l'accomplissement de tâches déterminées liées aux obligations incombant à ce dernier en vertu du présent règlement;
26) «importateur», toute personne physique ou morale établie dans l'Union qui met un dispositif provenant d'un pays tiers sur le marché de l'Union;
27) «distributeur», toute personne physique ou morale faisant partie de la chaîne d'approvisionnement, autre que le fabricant ou l'importateur, qui met un dispositif à disposition sur le marché, jusqu'au stade de sa mise en service;
28) «opérateur économique», le fabricant, un mandataire, un importateur ou un distributeur;
29) «établissement de santé», une entité ayant pour mission première de prendre en charge ou soigner des patients ou d'œuvrer en faveur de la santé publique;
30) «utilisateur», tout professionnel de la santé ou tout profane qui utilise un dispositif;
31) «profane», une personne physique qui n'est titulaire d'aucun diplôme dans une branche des soins de santé ou dans une discipline médicale;
32) «évaluation de la conformité», la procédure permettant de démontrer le respect ou non des exigences du présent règlement relatives à un dispositif;
33) «organisme d'évaluation de la conformité», un organisme en charge des activités d'évaluation de la conformité par un tiers, y compris l'étalonnage, la mise à l'essai, la certification et l'inspection;
34) «organisme notifié», un organisme d'évaluation de la conformité désigné en application du présent règlement;
35) «marquage de conformité CE» ou «marquage CE», un marquage par lequel le fabricant indique qu'un dispositif est conforme aux dispositions applicables du présent règlement et des autres actes législatifs d'harmonisation de l'Union qui en prévoient l'apposition;
36) «preuve clinique», les données cliniques et les résultats de l'évaluation des performances relatifs à un dispositif, dont le volume et la qualité sont suffisants pour permettre d'évaluer, en connaissance de cause, si le dispositif est sûr et offre le ou les bénéfices cliniques attendus lorsqu'il est utilisé conformément à la destination prévue par le fabricant;
37) «bénéfice clinique», l'effet positif d'un dispositif du fait de sa fonction, telle que le dépistage, la surveillance, le diagnostic ou l'aide au diagnostic des patients, ou un effet positif sur la prise en charge des patients ou en termes de santé publique;
38) «validité scientifique d'un analyte», l'association d'un analyte à une affection clinique ou à un état physiologique;
39) «performances d'un dispositif», la capacité d'un dispositif d'être utilisé conformément à sa destination indiquée par le fabricant. Elles désignent les performances analytiques et, le cas échéant, les performances cliniques associées à cette destination;
40) «performances analytiques», la capacité d'un dispositif de déceler ou mesurer correctement un analyte donné;
41) «performances cliniques», la capacité d'un dispositif de produire des résultats en corrélation avec une affection clinique donnée ou un processus ou état physiologique ou pathologique donné en fonction de la population cible et de l'utilisateur auquel le dispositif est destiné;
42) «étude des performances», une étude destinée à établir ou à confirmer les performances analytiques ou cliniques d'un dispositif;
43) «plan d'étude des performances», un document qui décrit la justification, les objectifs, la conception, les méthodes, le contrôle, les aspects statistiques, l'organisation et la réalisation d'une étude des performances;
44) «évaluation des performances», l'examen et l'analyse des données visant à établir ou vérifier la validité scientifique, les performances analytiques et, le cas échéant, les performances cliniques d'un dispositif;
45) «dispositif devant faire l'objet d'une étude des performances», tout dispositif que le fabricant prévoit de soumettre à une étude des performances.
Un dispositif destiné à la recherche, sans le moindre objectif médical, n'est pas considéré comme un dispositif devant faire l'objet d'une étude des performances;
46) «étude interventionnelle des performances cliniques», une étude des performances cliniques dans laquelle les résultats des essais peuvent influencer les décisions relatives à la prise en charge du patient et/ou être utilisés pour orienter les soins;
47) «participant», une personne physique participant à une étude des performances dont les échantillons font l'objet d'un examen in vitro par un dispositif devant faire l'objet d'une étude des performances et/ou par un dispositif utilisé à des fins de contrôle;
48) «investigateur», une personne physique responsable de la réalisation d'une étude des performances sur un site d'étude des performances;
49) «spécificité diagnostique», la capacité d'un dispositif de reconnaître l'absence d'un marqueur cible associé à une maladie ou affection donnée;
50) «sensibilité diagnostique», la capacité d'un dispositif de déceler la présence d'un marqueur cible associé à une maladie ou affection donnée;
51) «valeur prédictive», la probabilité qu'une personne chez laquelle un dispositif livre des résultats positifs présente une affection donnée recherchée ou qu'une personne chez laquelle un dispositif livre des résultats négatifs ne présente pas une affection donnée;
52) «valeur prédictive positive», la capacité d'un dispositif de distinguer les vrais résultats positifs des faux résultats positifs pour un attribut donné dans une population donnée;
53) «valeur prédictive négative», la capacité d'un dispositif de distinguer les vrais résultats négatifs des faux résultats négatifs pour un attribut donné dans une population donnée;
54) «rapport de vraisemblance», la vraisemblance d'obtenir un résultat donné chez une personne physique présentant l'affection clinique ou l'état physiologique cible rapportée à la vraisemblance d'obtenir le même résultat chez une personne physique ne présentant pas cette affection clinique ou cet état physiologique;
55) «matériau d'étalonnage», matériau de référence de mesure utilisé dans l'étalonnage d'un dispositif;
56) «matériau de contrôle», une substance, un matériau ou un article conçu par le fabricant afin d'être utilisé pour vérifier les performances d'un dispositif;
57) «promoteur», une personne physique, une entreprise, un institut ou une organisation responsable du lancement, de la gestion et de l'organisation du financement de l'étude des performances;
58) «consentement éclairé», l'expression, par un participant, de son plein gré et en toute liberté, de sa volonté de participer à une étude des performances particulière, après avoir pris connaissance de tous les éléments de l'étude des performances qui lui permettent de prendre sa décision ou, dans le cas des mineurs et des personnes incapables, une autorisation ou un accord de leur représentant légal de les faire participer à l'étude des performances;
59) «comité d'éthique», un organisme indépendant instauré dans un État membre conformément à la législation dudit État membre et habilité à émettre des avis aux fins du présent règlement, en tenant compte de l'avis de profanes, notamment des patients ou des associations de patients;
60) «événement indésirable», tout manifestation nocive, toute décision inappropriée relative à la prise en charge du patient, toute maladie ou blessure non intentionnelle ou tout signe clinique malencontreux, y compris un résultat de laboratoire anormal, chez des participants, des utilisateurs ou d'autre personnes, dans le cadre d'une étude des performances, lié ou non au dispositif devant faire l'objet d'une étude des performances;
61) «événement indésirable grave», tout événement indésirable ayant entraîné:
a) |
une décision de prise en charge du patient qui cause la mort de l'individu soumis à l'essai ou met sa vie en danger de manière imminente ou qui cause la mort de sa descendance; |
||||||||||||
b) |
la mort; |
||||||||||||
c) |
une dégradation grave de l'état de santé de l'individu soumis à l'essai ou du destinataire des dons ou des matériaux soumis à l'essai, laquelle est à l'origine:
|
||||||||||||
d) |
une souffrance fœtale, la mort du fœtus, des déficiences physiques ou mentales congénitales ou une malformation congénitale; |
62) «défectuosité d'un dispositif», tout défaut en matière d'identité, de qualité, de durabilité, de fiabilité, de sécurité ou de performances d'un dispositif devant faire l'objet d'une étude des performances, y compris tout dysfonctionnement, toute erreur d'utilisation ou tout défaut dans les informations fournies par le fabricant;
63) «surveillance après commercialisation», l'ensemble des activités réalisées par les fabricants, en collaboration avec d'autres opérateurs économiques, pour élaborer et tenir à jour une procédure systématique de collecte proactive de données sur les dispositifs qu'ils mettent sur le marché, mettent à disposition sur le marché ou mettent en service de manière à dresser le bilan de leur utilisation, dans le but de repérer toute nécessité d'appliquer immédiatement une mesure préventive ou corrective;
64) «surveillance du marché», l'ensemble des activités réalisées et des mesures prises par les pouvoirs publics pour vérifier et garantir que les dispositifs sont conformes aux exigences de la législation d'harmonisation de l'Union applicable et ne compromettent pas la santé, la sécurité ni tout autre aspect de la protection de l'intérêt public;
65) «rappel», toute mesure visant à obtenir le retour d'un dispositif qui a déjà été mis à la disposition de l'utilisateur final;
66) «retrait», toute mesure visant à empêcher qu'un dispositif de la chaîne d'approvisionnement reste mis à disposition sur le marché;
67) «incident», tout dysfonctionnement ou toute altération des caractéristiques ou des performances d'un dispositif mis à disposition sur le marché, y compris une erreur d'utilisation due à des caractéristiques ergonomiques, ainsi que tout défaut dans les informations fournies par le fabricant et tout préjudice résultant d'une décision médicale et des mesures prises ou non sur la base des informations ou du ou des résultats fournis par le dispositif;
68) «incident grave», tout incident ayant entraîné directement ou indirectement, susceptible d'avoir entraîné ou susceptible d'entraîner:
a) |
la mort d'un patient, d'un utilisateur ou de toute autre personne; |
b) |
une grave dégradation, temporaire ou permanente, de l'état de santé d'un patient, d'un utilisateur ou de toute autre personne; |
c) |
une menace grave pour la santé publique; |
69) «menace grave pour la santé publique», un événement susceptible d'entraîner un risque imminent de mort, de grave détérioration de l'état de santé ou de maladie grave pouvant nécessiter une mesure corrective rapide, et susceptible d'entraîner une morbidité ou une mortalité importante chez l'homme ou qui présente un caractère inhabituel ou imprévu au lieu et au moment considérés;
70) «mesure corrective», toute mesure visant à éliminer la cause d'un cas de non-conformité potentielle ou effective ou d'une autre situation indésirable;
71) «mesure corrective de sécurité», toute mesure corrective prise par un fabricant pour des raisons techniques ou médicales afin de prévenir ou d'atténuer le risque d'incident grave en rapport avec un dispositif mis à disposition sur le marché;
72) «avis de sécurité», une communication envoyée par un fabricant aux utilisateurs ou clients en rapport avec une mesure corrective de sécurité;
73) «norme harmonisée», une norme européenne au sens de l'article 2, point 1) c), du règlement (UE) no 1025/2012;
74) «spécifications communes», un ensemble d'exigences techniques et/ou cliniques, autres qu'une norme, offrant un moyen de se conformer aux obligations légales applicables à un dispositif, à un procédé ou à un système.
Section 2
Statut des produits au regard de la réglementation et conseils
Article 3
Statut des produits au regard de la réglementation
1. À la demande dûment justifiée d'un État membre, la Commission, après avoir consulté le groupe de coordination en matière de dispositifs médicaux (GCDM) institué en vertu de l'article 103 du règlement (UE) 2017/745, détermine, au moyen d'actes d'exécution, si un produit donné ou une catégorie donnée ou un groupe donné de produits répond ou non aux définitions de «dispositif médical de diagnostic in vitro» ou d'«accessoire de dispositif médical de diagnostic in vitro». Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3, du présent règlement.
2. La Commission peut aussi, de sa propre initiative, après avoir consulté le GCDM, statuer, au moyen d'actes d'exécution, sur les questions visées au paragraphe 1 du présent article. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
3. La Commission veille à ce que les États membres partagent leur expertise dans les domaines des dispositifs médicaux de diagnostic in vitro, des dispositifs médicaux, des médicaments, des tissus et cellules humains, des cosmétiques, des biocides, des denrées alimentaires et, si nécessaire, d'autres produits, afin de déterminer la réglementation dont relève un produit, ou une catégorie ou un groupe de produits.
4. Lorsqu'elle examine le statut possible, au regard de la réglementation en tant que dispositifs, des produits impliquant des médicaments, des tissus et cellules humains, des biocides ou des produits alimentaires, la Commission veille à dûment consulter l'Agence européenne des médicaments (EMA), l'Agence européenne des produits chimiques et l'Autorité européenne de sécurité des aliments, selon le cas.
Article 4
Informations génétiques, conseils et consentement éclairé
1. Les États membres veillent à ce que, lorsqu'un test génétique est pratiqué sur des personnes physiques dans le cadre de soins de santé au sens de l'article 3, point a), de la directive 2011/24/UE du Parlement européen et du Conseil et à des fins médicales de diagnostic, d'amélioration du traitement, de test prédictif ou prénatal, des informations pertinentes sur la nature, l'importance et les implications du test génétique, le cas échéant, soient communiquées à la personne physique faisant l'objet du test ou à son représentant légal, selon le cas.
2. Dans le cadre des obligations visées au paragraphe 1, les États membres garantissent en particulier un accès approprié à des conseils en cas de recours à des tests génétiques fournissant des informations sur la prédisposition génétique à des affections et/ou des maladies généralement considérées comme incurables dans l'état actuel de la science et de la technologie.
3. Le paragraphe 2 ne s'applique pas dans les cas où le diagnostic d'une affection et/ou d'une maladie dont la personne physique qui fait l'objet du test se sait déjà atteinte est confirmé par un test génétique ou en cas de recours à un diagnostic compagnon.
4. Aucun élément du présent article n'empêche les États membres d'adopter ou de maintenir au niveau national des mesures plus protectrices pour le patient, plus spécifiques ou concernant le consentement éclairé.
CHAPITRE II
MISE À DISPOSITION SUR LE MARCHÉ ET MISE EN SERVICE DES DISPOSITIFS, OBLIGATIONS DES OPÉRATEURS ÉCONOMIQUES, MARQUAGE CE ET LIBRE CIRCULATION
Article 5
Mise sur le marché et mise en service
1. Un dispositif ne peut être mis sur le marché ou mis en service que s'il est conforme au présent règlement au moment où il est dûment fourni et dès lors qu'il est correctement installé, entretenu et utilisé conformément à sa destination.
2. Un dispositif est conforme aux exigences générales en matière de sécurité et de performances fixées à l'annexe I qui lui sont applicables, compte tenu de sa destination.
3. La démonstration de la conformité avec les exigences générales en matière de sécurité et de performances passe par une évaluation des performances telle qu'elle est prévue à l'article 56.
4. Les dispositifs fabriqués et utilisés dans les établissements de santé, à l'exception des dispositifs devant faire l'objet d'une étude des performances, sont considérés comme ayant été mis en service.
5. À l'exception des exigences générales en matière de sécurité et de performances fixées à l'annexe I, les dispositions du présent règlement ne s'appliquent pas aux dispositifs fabriqués et utilisés exclusivement dans les établissements de santé établis dans l'Union, si toutes les conditions suivantes sont remplies:
a) |
les dispositifs ne sont pas transférés vers une autre entité juridique; |
||||||
b) |
la fabrication et l'utilisation des dispositifs s'effectuent dans le cadre de systèmes de gestion de la qualité appropriés; |
||||||
c) |
le laboratoire de l'établissement de santé respecte la norme EN ISO 15189 ou, le cas échéant, les dispositions nationales, notamment les dispositions nationales en matière d'accréditation; |
||||||
d) |
l'établissement de santé justifie dans sa documentation que les besoins spécifiques du groupe cible de patients ne peuvent pas être satisfaits ou ne peuvent pas être satisfaits au niveau de performances approprié par un dispositif équivalent disponible sur le marché; |
||||||
e) |
l'établissement de santé fournit, sur demande, à son autorité compétente des informations concernant l'utilisation de ces dispositifs, qui comportent une justification de leur fabrication, de leur modification et de leur utilisation; |
||||||
f) |
l'établissement de santé établit une déclaration, qu'il rend publique, comprenant:
|
||||||
g) |
en ce qui concerne les dispositifs relevant de la classe D, conformément aux règles établies à l'annexe VIII, l'établissement de santé établit une documentation permettant de comprendre les installations de fabrication, le procédé de fabrication, la conception et les données sur les performances des dispositifs, y compris leur destination, et de manière suffisamment détaillée pour que l'autorité compétente puisse s'assurer que les exigences générales en matière de sécurité et de performances énoncées à l'annexe I sont remplies. Les États membres peuvent appliquer la présente disposition également aux dispositifs relevant des classes A, B ou C, conformément aux règles établies à l'annexe VIII; |
||||||
h) |
l'établissement de santé prend toutes les mesures nécessaires pour garantir que l'ensemble des dispositifs sont fabriqués conformément à la documentation visée au point g); et |
||||||
i) |
l'établissement de santé examine l'expérience issue de l'utilisation clinique des dispositifs et prend toutes les mesures correctives nécessaires. |
Les États membres peuvent exiger de ces établissements de santé qu'ils transmettent à l'autorité compétente toute autre information pertinente concernant les dispositifs de ce type qui ont été fabriqués et sont utilisés sur leur territoire. Les États membres conservent le droit de restreindre la fabrication et l'utilisation de tout type particulier de dispositif et ont en outre le droit de contrôler les activités des établissements de santé.
Le présent paragraphe ne s'applique pas aux dispositifs qui sont fabriqués à l'échelle industrielle.
6. Afin d'assurer l'application uniforme de l'annexe I, la Commission peut adopter des actes d'exécution dans la mesure nécessaire pour résoudre les problèmes liés à des différences d'interprétation et à l'application pratique. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
Article 6
Ventes à distance
1. Un dispositif proposé au moyen de services de la société de l'information, au sens de l'article 1er, paragraphe 1, point b), de la directive (UE) 2015/1535, à une personne physique ou morale établie dans l'Union est conforme au présent règlement.
2. Sans préjudice des dispositions de droit national relatives à l'exercice de la profession médicale, un dispositif qui n'est pas mis sur le marché mais utilisé dans le cadre d'une activité commerciale, à titre onéreux ou gratuit, aux fins d'une prestation diagnostique ou thérapeutique fournie au moyen de services de la société de l'information au sens de l'article 1er, paragraphe 1, point b), de la directive (UE) 2015/1535 ou par d'autres moyens de communication, directement ou via des intermédiaires, à une personne physique ou morale établie dans l'Union doit être conforme au présent règlement.
3. À la demande d'une autorité compétente, toute personne physique ou morale proposant un dispositif conformément au paragraphe 1 ou assurant une prestation conformément au paragraphe 2 met à disposition une copie de la déclaration de conformité UE du dispositif concerné.
4. Un État membre peut, pour des motifs liés à la protection de la santé publique, exiger d'un fournisseur de services de la société de l'information au sens de l'article 1er, paragraphe 1, point b), de la directive (UE) 2015/1535 qu'il mette fin à son activité.
Article 7
Allégations
Au niveau de l'étiquetage, de la notice d'utilisation, de la mise à disposition et de la mise en service des dispositifs ainsi que de la publicité les concernant, il est interdit d'utiliser du texte, des noms, des marques, des images et des signes figuratifs ou autres susceptibles d'induire l'utilisateur ou le patient en erreur en ce qui concerne la destination, la sécurité et les performances du dispositif:
a) |
en attribuant au dispositif des fonctions et des propriétés qu'il n'a pas; |
b) |
en donnant une impression trompeuse sur le traitement ou le diagnostic, ou sur des fonctions ou des propriétés qui ne sont pas celles du dispositif en question; |
c) |
en omettant d'informer l'utilisateur ou le patient d'un risque probable lié à l'utilisation du dispositif conformément à sa destination; |
d) |
en suggérant d'autres utilisations du dispositif que celles déclarées relever de la destination pour laquelle l'évaluation de la conformité a été réalisée. |
Article 8
Application de normes harmonisées
1. Les dispositifs conformes aux normes harmonisées applicables, ou à des parties pertinentes de ces normes, dont les références ont été publiées au Journal officiel de l'Union européenne, sont présumés conformes aux exigences du présent règlement relevant de ces normes ou de parties de celles-ci.
Le premier alinéa s'applique également aux mesures imposées par le présent règlement aux opérateurs économiques ou aux promoteurs en matière de systèmes ou de procédures, y compris celles relatives aux systèmes de gestion de la qualité, à la gestion des risques, aux systèmes de surveillance après commercialisation, aux études des performances, aux preuves cliniques et au suivi des performances après commercialisation (SPAC).
Les références faites dans le présent règlement à des normes harmonisées s'entendent comme les références à des normes harmonisées qui ont été publiées au Journal officiel de l'Union européenne.
2. Les références faites dans le présent règlement à des normes harmonisées incluent aussi les monographies de la pharmacopée européenne adoptées en vertu de la convention relative à l'élaboration d'une pharmacopée européenne, pour autant que les références auxdites monographies aient été publiées au Journal officiel de l'Union européenne.
Article 9
Spécifications communes
1. La Commission, après avoir consulté le GCDM, peut, au moyen d'actes d'exécution, adopter des spécifications communes, lorsqu'il n'existe pas de normes harmonisées, lorsque les normes harmonisées applicables ne suffisent pas, ou lorsqu'il y a lieu de répondre à des préoccupations de santé publique, en ce qui concerne les exigences générales en matière de sécurité et de performances énoncées à l'annexe I, la documentation technique prévue aux annexes II et III, l'évaluation des performances et le SPAC prévus à l'annexe XIII ou les exigences relatives aux études des performances énoncées à l'annexe XIII. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
2. Les dispositifs conformes aux spécifications communes visées au paragraphe 1 sont présumés conformes aux exigences du présent règlement relevant de ces spécifications ou de parties pertinentes de celles-ci.
3. Les fabricants se conforment aux spécifications communes visées au paragraphe 1 à moins qu'ils puissent dûment justifier avoir adopté des solutions qui garantissent un niveau de sécurité et de performances au moins équivalent à celui prévu par ces spécifications.
Article 10
Obligations générales des fabricants
1. Lorsqu'ils mettent leurs dispositifs sur le marché ou en service, les fabricants veillent à ce que ceux-ci aient été conçus et fabriqués conformément aux exigences du présent règlement.
2. Les fabricants établissent, documentent, mettent en œuvre et maintiennent un système de gestion des risques tel qu'il est décrit à l'annexe I, section 3.
3. Les fabricants réalisent une évaluation des performances conformément aux exigences énoncées à l'article 56 et à l'annexe XIII, notamment un SPAC.
4. Les fabricants élaborent et tiennent à jour la documentation technique relative à ces dispositifs. La documentation technique doit être de nature à permettre l'évaluation de la conformité du dispositif avec les exigences du présent règlement. La documentation technique contient les éléments prévus aux annexes II et III.
La Commission est habilitée à adopter des actes délégués conformément à l'article 108 pour modifier, eu égard aux progrès techniques, les annexes II et III.
5. Lorsque la conformité avec les exigences applicables est démontrée à l'issue de la procédure d'évaluation de la conformité applicable, les fabricants de dispositifs, autres que les dispositifs devant faire l'objet d'une étude des performances, établissent une déclaration de conformité UE conformément à l'article 17 et apposent le marquage de conformité CE conformément à l'article 18.
6. Les fabricants se conforment aux obligations concernant le système IUD visées à l'article 24 et aux obligations liées à l'enregistrement visées aux articles 26 et 28.
7. Les fabricants tiennent la documentation technique, la déclaration de conformité UE et, le cas échéant, une copie du certificat applicable délivré conformément à l'article 51, y compris toute modification et tout document complémentaire, à la disposition des autorités compétentes pour une durée d'au moins dix ans à partir de la mise sur le marché du dernier dispositif visé par la déclaration de conformité UE.
À la demande d'une autorité compétente, le fabricant présente, comme indiqué dans cette demande, l'ensemble de la documentation technique ou un résumé de celle-ci.
Afin que son mandataire puisse s'acquitter des tâches prévues à l'article 11, paragraphe 3, le fabricant dont le siège social se situe en dehors de l'Union fait en sorte que le mandataire ait en permanence à sa disposition la documentation nécessaire.
8. Les fabricants veillent à ce que des procédures existent pour maintenir la production en série conforme aux exigences du présent règlement. Il est dûment tenu compte, en temps opportun, des modifications de la conception ou des caractéristiques du produit et des modifications des normes harmonisées ou des spécifications communes sur la base desquelles la conformité d'un produit est déclarée. Les fabricants de dispositifs, autres que les dispositifs devant faire l'objet d'une étude des performances, établissent, documentent, appliquent, maintiennent, mettent à jour et améliorent en permanence un système de gestion de la qualité qui garantit la conformité avec les dispositions du présent règlement et ce, de la façon la plus efficace possible et d'une manière qui soit proportionnée à la classe de risque et au type de dispositif.
Le système de gestion de la qualité englobe toutes les parties et éléments de l'organisation d'un fabricant en rapport avec la qualité des processus, des procédures et des dispositifs. Il régit les ressources requises en matière de structure, de responsabilités, de procédures, de processus et de gestion pour appliquer les principes et les mesures nécessaires pour garantir la conformité avec les dispositions du présent règlement.
Le système de gestion de la qualité porte au moins sur les aspects suivants:
a) |
une stratégie de respect de la réglementation, notamment le respect des procédures d'évaluation de la conformité et des procédures de gestion des modifications apportées aux dispositifs concernés par le système; |
b) |
l'identification des exigences générales applicables en matière de sécurité et de performances et la recherche de solutions pour les respecter; |
c) |
la responsabilité de la gestion; |
d) |
la gestion des ressources, et notamment la sélection et le contrôle des fournisseurs et sous-traitants; |
e) |
la gestion des risques visée à l'annexe I, section 3; |
f) |
l'évaluation des performances conformément à l'article 56 et à l'annexe XIII, y compris le SPAC; |
g) |
la réalisation du produit, y compris la planification, la conception, l'élaboration, la production et la fourniture de services; |
h) |
la vérification des attributions d'IUD conformément à l'article 24, paragraphe 3, à l'ensemble des dispositifs concernés, en veillant à la cohérence et à la validité des informations fournies conformément à l'article 26; |
i) |
l'élaboration, la mise en œuvre et le maintien d'un système de surveillance après commercialisation conformément à l'article 78; |
j) |
la gestion de la communication avec les autorités compétentes, les organismes notifiés, les autres opérateurs économiques, les clients et/ou d'autres parties prenantes; |
k) |
les processus de notification des incidents graves et des mesures correctives de sécurité dans un contexte de vigilance; |
l) |
la gestion des mesures correctives et préventives et la vérification de leur efficacité; |
m) |
les procédures de contrôle et de mesure des résultats, d'analyse des données et d'amélioration des produits. |
9. Les fabricants de dispositifs appliquent et mettent à jour le système de surveillance après commercialisation conformément à l'article 78.
10. Les fabricants veillent à ce que le dispositif soit accompagné des informations figurant à l'annexe I, section 20, dans une ou des langues officielles de l'Union définies par l'État membre dans lequel le dispositif est mis à la disposition de l'utilisateur ou du patient. Les indications figurant sur l'étiquette sont indélébiles, facilement lisibles et clairement compréhensibles pour le patient ou l'utilisateur auquel le dispositif est destiné.
Les informations fournies conformément à l'annexe I, section 20, avec les dispositifs d'autodiagnostic ou les dispositifs de diagnostic près du patient sont facilement compréhensibles et communiquées dans la ou les langues officielles de l'Union définies par l'État membre dans lequel le dispositif est mis à la disposition de l'utilisateur ou du patient.
11. Les fabricants qui considèrent ou ont des raisons de croire qu'un dispositif qu'ils ont mis sur le marché ou mis en service n'est pas conforme au présent règlement prennent immédiatement les mesures correctives nécessaires pour le mettre en conformité, le retirer ou le rappeler, selon le cas. Ils informent les distributeurs du dispositif en question et, le cas échéant, le mandataire et les importateurs en conséquence.
Lorsque le dispositif présente un risque grave, les fabricants informent immédiatement les autorités compétentes des États membres dans lesquels ils ont mis le dispositif à disposition et, le cas échéant, l'organisme notifié ayant délivré un certificat conformément à l'article 51, en particulier, du cas de non-conformité et des éventuelles mesures correctives prises.
12. Les fabricants disposent d'un système d'enregistrement et de notification des incidents graves et des mesures correctives de sécurité décrit aux articles 82 et 83.
13. À la demande d'une autorité compétente, les fabricants lui communiquent toutes les informations et tous les documents nécessaires pour démontrer la conformité du dispositif, dans une langue officielle de l'Union définie par l'État membre concerné. L'autorité compétente de l'État membre dans lequel le fabricant a son siège social peut demander que le fabricant fournisse des échantillons du dispositif gratuitement ou, si c'est impossible, donne accès au dispositif. Les fabricants coopèrent avec une autorité compétente, à sa demande, à toute mesure corrective prise en vue d'éliminer, ou, si ce n'est pas possible, d'atténuer les risques présentés par des dispositifs qu'ils ont mis sur le marché ou mis en service.
Si le fabricant ne coopère pas ou si les informations et documents qu'il a communiqués sont incomplets ou incorrects, l'autorité compétente peut, aux fins de la protection de la santé publique et de la sécurité du patient, prendre toute mesure appropriée pour interdire ou limiter la mise à disposition du dispositif sur son marché national, retirer le dispositif dudit marché ou le rappeler jusqu'à ce que le fabricant coopère ou fournisse des informations complètes et correctes.
Si une autorité compétente considère ou a des raisons de croire qu'un dispositif a causé un dommage, elle facilite la communication, sur demande, des informations et des documents visés au premier alinéa au patient ou à l'utilisateur ayant potentiellement subi un dommage et, le cas échéant, à son ayant-droit, à sa compagnie d'assurance maladie ou à d'autres parties tierces concernées par le dommage causé au patient ou à l'utilisateur, sans préjudice des règles en matière de protection des données et, à moins qu'un intérêt public supérieur ne justifie la divulgation des informations en question, sans préjudice de la protection des droits de propriété intellectuelle.
L'autorité compétente n'est pas tenue de respecter l'obligation prévue au troisième alinéa lorsque la divulgation des informations et de la documentation visées au premier alinéa s'effectue habituellement dans le cadre d'une procédure judiciaire.
14. Lorsque les fabricants font concevoir ou fabriquer leurs dispositifs par une autre personne morale ou physique, les informations sur l'identité de celle-ci font partie des informations à transmettre en application de l'article 26, paragraphe 3.
15. Les personnes physiques ou morales peuvent demander réparation pour des dommages causés par un dispositif défectueux conformément à la législation de l'Union et à la législation nationale applicables.
Les fabricants auront, d'une manière qui soit proportionnée à la classe de risque, au type de dispositif et à la taille de l'entreprise, pris des mesures pour disposer d'une couverture financière suffisante au regard de leur éventuelle responsabilité en application de la directive 85/374/CEE, sans préjudice de mesures plus protectrices en vertu du droit national.
Article 11
Mandataire
1. Lorsque le fabricant d'un dispositif n'est pas établi dans un État membre, le dispositif ne peut être mis sur le marché de l'Union que si le fabricant désigne un mandataire unique.
2. La désignation constitue le mandat du mandataire, elle n'est valable que si elle est acceptée par écrit par le mandataire et vaut au moins pour tous les dispositifs du même groupe générique de dispositifs.
3. Le mandataire s'acquitte des tâches précisées dans le mandat dont il aura convenu avec le fabricant. Il fournit une copie du mandat à l'autorité compétente, sur demande.
Le mandat oblige le mandataire, et le fabricant l'autorise, à s'acquitter au moins des tâches suivantes en rapport avec les dispositifs relevant de son mandat:
a) |
vérifier que la déclaration de conformité UE et la documentation technique ont été établies et, le cas échéant, qu'une procédure d'évaluation de la conformité appropriée a été appliquée par le fabricant; |
b) |
tenir disponible une copie de la documentation technique, de la déclaration de conformité UE et, le cas échéant, du certificat applicable délivré conformément à l'article 51, y compris toute modification et tout document complémentaire, à la disposition des autorités compétentes pour la durée visée à l'article 10, paragraphe 7; |
c) |
se conformer aux obligations liées à l'enregistrement visées à l'article 28 et vérifier que le fabricant s'est conformé aux obligations liées à l'enregistrement visées à l'article 26; |
d) |
sur demande d'une autorité compétente, lui communiquer toutes les informations et tous les documents nécessaires à la démonstration de la conformité d'un dispositif, dans une langue officielle de l'Union définie par l'État membre concerné; |
e) |
transmettre au fabricant toute demande d'échantillons ou d'accès à un dispositif faite par une autorité compétente de l'État membre dans lequel le mandataire a son siège social, et vérifier que l'autorité compétente reçoive les échantillons ou ait accès au dispositif; |
f) |
coopérer avec les autorités compétentes à toute mesure préventive ou corrective prise en vue d'éliminer, ou, si ce n'est pas possible, d'atténuer les risques présentés par des dispositifs; |
g) |
informer immédiatement le fabricant des réclamations et signalements de professionnels de la santé, de patients et d'utilisateurs relatifs à des incidents supposés liés à un dispositif relevant de son mandat; |
h) |
mettre fin au mandat si le fabricant ne respecte pas les obligations qui lui incombent en vertu du présent règlement. |
4. Le mandat visé au paragraphe 3 du présent article ne délègue pas les obligations du fabricant prévues par l'article 10, paragraphes 1, 2, 3, 4, 5, 6, 8, 9, 10 et 11.
5. Sans préjudice du paragraphe 4 du présent article, lorsque le fabricant n'est pas établi dans un État membre et n'a pas satisfait aux obligations visées à l'article 10, le mandataire et le fabricant sont solidairement responsables des dispositifs défectueux, selon des modalités identiques.
6. Un mandataire qui met fin à son mandat sur la base du paragraphe 3, point h), informe immédiatement de la fin du mandat et des raisons de cette décision l'autorité compétente de l'État membre dans lequel il est établi et, le cas échéant, l'organisme notifié qui est intervenu dans l'évaluation de la conformité du dispositif.
7. Toute référence dans le présent règlement à l'autorité compétente de l'État membre dans lequel est situé le siège social du fabricant s'entend comme faite à l'autorité compétente de l'État membre dans lequel est situé le siège social du mandataire désigné par un fabricant visé au paragraphe 1.
Article 12
Changement de mandataire
Les modalités de changement de mandataire sont clairement définies dans un accord entre le fabricant, si possible le mandataire sortant et le nouveau mandataire. Cet accord précise au moins les informations suivantes:
a) |
la date de fin du mandat du mandataire sortant et la date de début du mandat du nouveau mandataire; |
b) |
la date jusqu'à laquelle le mandataire sortant peut être indiqué dans les informations fournies par le fabricant, y compris tout document publicitaire; |
c) |
les modalités de transfert des documents, y compris les questions de confidentialité et de droits de propriété; |
d) |
l'obligation du mandataire sortant de transmettre au fabricant ou au nouveau mandataire, après la fin du mandat, toute réclamation ou tout signalement de professionnels de la santé, de patients ou d'utilisateurs relatifs à des incidents supposés liés à un dispositif qui relevait de son mandat. |
Article 13
Obligations générales des importateurs
1. Les importateurs ne mettent sur le marché de l'Union que des dispositifs conformes au présent règlement.
2. Pour mettre un dispositif sur le marché, les importateurs vérifient que:
a) |
le dispositif porte le marquage CE et la déclaration de conformité UE du dispositif a été établie; |
b) |
le fabricant est identifié et a désigné un mandataire conformément à l'article 11; |
c) |
le dispositif est étiqueté conformément au présent règlement et accompagné de la notice d'utilisation requise; |
d) |
le fabricant a attribué, le cas échéant, un IUD au dispositif conformément à l'article 24. |
Lorsqu'un importateur considère ou a des raisons de croire qu'un dispositif n'est pas conforme aux exigences du présent règlement, il ne met le dispositif sur le marché qu'après la mise en conformité de celui-ci et informe le fabricant et le mandataire de celui-ci. Lorsque l'importateur considère ou a des raisons de croire que le dispositif présente un risque grave ou est un dispositif falsifié, il informe également l'autorité compétente de l'État membre dans lequel l'importateur est établi.
3. Les importateurs indiquent sur le dispositif ou sur son conditionnement ou dans un document accompagnant le dispositif leur nom, leur raison sociale ou leur marque déposée, leur siège social et l'adresse à laquelle ils peuvent être joints afin de pouvoir établir leur emplacement. Ils veillent à ce qu'aucune étiquette supplémentaire ne dissimule les informations figurant sur l'étiquette du fabricant.
4. Les importateurs vérifient que le dispositif est enregistré dans le système électronique conformément à l'article 26. Les importateurs ajoutent leurs coordonnées dans cet enregistrement conformément à l'article 28.
5. Les importateurs veillent à ce que, tant qu'un dispositif est sous leur responsabilité, les conditions de stockage ou de transport ne compromettent pas sa conformité avec les exigences générales en matière de sécurité et de performances énoncées à l'annexe I, et ils se conforment aux conditions éventuellement fixées par le fabricant.
6. Les importateurs tiennent un registre des réclamations, des dispositifs non conformes et des rappels et retraits, et fournissent au fabricant, au mandataire et aux distributeurs toute information que ceux-ci demandent, afin de leur permettre de procéder à l'investigation des réclamations.
7. Les importateurs qui considèrent ou ont des raisons de croire qu'un dispositif qu'ils ont mis sur le marché n'est pas conforme au présent règlement informent immédiatement le fabricant et son mandataire. Les importateurs coopèrent avec le fabricant, le mandataire de celui-ci et les autorités compétentes pour faire en sorte que les mesures correctives nécessaires soient prises pour que ce dispositif soit mis en conformité, retiré ou rappelé. Lorsque le dispositif présente un risque grave, ils informent immédiatement les autorités compétentes des États membres dans lesquels ils ont mis le dispositif à disposition et, le cas échéant, l'organisme notifié ayant délivré un certificat conformément à l'article 51 pour le dispositif en question, et précisent, notamment, le cas de non-conformité et les éventuelles mesures correctives prises.
8. Les importateurs qui ont reçu des réclamations ou des signalements de professionnels de la santé, de patients ou d'utilisateurs relatifs à des incidents supposés liés à un dispositif qu'ils ont mis sur le marché transmettent immédiatement cette information au fabricant et à son mandataire.
9. Les importateurs conservent pour la durée prévue à l'article 10, paragraphe 7, une copie de la déclaration de conformité UE et, le cas échéant, du certificat applicable délivré conformément à l'article 51, y compris toute modification et tout document complémentaire.
10. Les importateurs coopèrent avec les autorités compétentes, à la demande de ces dernières, à toute mesure prise en vue d'éliminer ou, si ce n'est pas possible, d'atténuer les risques présentés par des produits qu'ils ont mis sur le marché. À la demande d'une autorité compétente de l'État membre dans lequel l'importateur a son siège social, ils fournissent des échantillons du dispositif gratuitement ou, si c'est impossible, donnent accès au dispositif.
Article 14
Obligations générales des distributeurs
1. Lorsqu'ils mettent un dispositif à disposition sur le marché, les distributeurs agissent, dans le cadre de leurs activités, avec la diligence requise pour respecter les exigences applicables.
2. Avant de mettre un dispositif à disposition sur le marché, les distributeurs vérifient que les conditions suivantes sont remplies:
a) |
le dispositif porte le marquage CE et la déclaration de conformité UE du dispositif a été établie; |
b) |
le dispositif est accompagné des informations que le fabricant est tenu de fournir conformément à l'article 10, paragraphe 10; |
c) |
dans le cas de dispositifs importés, l'importateur s'est conformé aux exigences visées à l'article 13, paragraphe 3; |
d) |
le fabricant a attribué un IUD, le cas échéant. |
Afin de respecter les exigences visées au premier alinéa, points a), b) et d), le distributeur peut appliquer une méthode d'échantillonnage représentative des dispositifs fournis par ledit distributeur.
Lorsqu'un distributeur considère ou a des raisons de croire qu'un dispositif n'est pas conforme aux exigences du présent règlement, il ne met le dispositif à disposition sur le marché qu'après la mise en conformité de celui-ci et informe le fabricant et, le cas échéant, le mandataire de ce dernier et l'importateur. Lorsque le distributeur considère ou a des raisons de croire que le dispositif présente un risque grave ou est un dispositif falsifié, il informe également l'autorité compétente de l'État membre dans lequel il est établi.
3. Les distributeurs veillent à ce que, tant que le dispositif est sous leur responsabilité, les conditions de stockage ou de transport soient conformes aux conditions fixées par le fabricant.
4. Les distributeurs qui considèrent ou ont des raisons de croire qu'un dispositif qu'ils ont mis à disposition sur le marché n'est pas conforme au présent règlement informent immédiatement le fabricant et, le cas échéant, le mandataire de ce dernier et l'importateur. Les distributeurs coopèrent avec le fabricant et, le cas échéant, le mandataire de ce dernier et l'importateur, ainsi qu'avec les autorités compétentes, pour faire en sorte que les mesures correctives nécessaires soient prises pour que ce dispositif soit mis en conformité, retiré ou rappelé, selon le cas. Lorsque le distributeur considère ou à des raisons de croire que le dispositif présente un risque grave, il informe aussi immédiatement les autorités compétentes des États membres dans lesquels il a mis le dispositif à disposition et précise, notamment, le cas de non-conformité et les éventuelles mesures correctives prises.
5. Les distributeurs qui ont reçu des réclamations ou des signalements de professionnels de la santé, de patients ou d'utilisateurs relatifs à des incidents supposés liés à un dispositif qu'ils ont mis à disposition transmettent immédiatement cette information au fabricant et, le cas échéant, au mandataire de ce dernier et à l'importateur. Ils tiennent un registre des réclamations, des dispositifs non conformes et des rappels et retraits, et tiennent le fabricant et, le cas échéant, le mandataire et l'importateur informés de ces activités de suivi et leur fournissent toute information sur demande.
6. À la demande d'une autorité compétente, les distributeurs lui communiquent toutes les informations et tous les documents dont ils disposent et qui sont nécessaires à la démonstration de la conformité d'un dispositif.
Les distributeurs sont réputés avoir rempli l'obligation visée au premier alinéa lorsque le fabricant ou, le cas échéant, le mandataire pour le dispositif en question fournit les informations requises. Les distributeurs coopèrent avec les autorités compétentes, à leur demande, à toute mesure prise pour éliminer les risques présentés par des dispositifs qu'ils ont mis à disposition sur le marché. À la demande d'une autorité compétente, les distributeurs fournissent des échantillons gratuits du dispositif ou, si c'est impossible, donnent accès au dispositif.
Article 15
Personne chargée de veiller au respect de la réglementation
1. Les fabricants disposent au sein de leur organisation d'au moins une personne chargée de veiller au respect de la réglementation possédant l'expertise requise dans le domaine des dispositifs médicaux de diagnostic in vitro. Cette expertise est attestée par l'une des qualifications suivantes:
a) |
un diplôme, un certificat ou un autre document de certification formelle sanctionnant des études universitaires en droit, en médecine, en pharmacie, en ingénierie ou dans une autre discipline scientifique pertinente, ou un cycle de cours reconnu équivalent par l'État membre concerné, et une expérience professionnelle d'au moins un an dans le domaine de la réglementation ou des systèmes de gestion de la qualité en rapport avec les dispositifs médicaux de diagnostic in vitro; |
b) |
une expérience professionnelle de quatre ans dans le domaine de la réglementation ou des systèmes de gestion de la qualité en rapport avec les dispositifs médicaux de diagnostic in vitro. |
2. Les micro et petites entreprises au sens de la recommandation 2003/361/CE de la Commission ne sont pas tenues de disposer, au sein de leur organisation, d'une personne chargée de veiller au respect de la réglementation mais une telle personne est en permanence et sans interruption à leur disposition.
3. La personne chargée de veiller au respect de la réglementation a au moins pour mission de faire en sorte que:
a) |
la conformité des dispositifs soit correctement vérifiée, conformément au système de gestion de la qualité dans le cadre duquel les dispositifs concernés sont fabriqués, avant la libération d'un dispositif; |
b) |
la documentation technique et la déclaration de conformité UE soient établies et tenues à jour; |
c) |
les obligations en matière de surveillance après commercialisation soient remplies, conformément à l'article 10, paragraphe 9; |
d) |
les obligations en matière de notification visées aux articles 82 à 86 soient remplies; |
e) |
dans le cas de dispositifs devant faire l'objet d'une étude des performances en vue d'une utilisation dans le cadre d'études interventionnelles des performances cliniques ou d'autres études des performances présentant des risques pour les sujets, la déclaration visée à l'annexe XIV, section 4.1, soit délivrée. |
4. Si plusieurs personnes sont solidairement responsables du respect de la réglementation conformément aux paragraphes 1, 2 et 3, leurs domaines de responsabilité respectifs sont précisés par écrit.
5. La personne chargée de veiller au respect de la réglementation ne subit, au sein de l'organisation du fabricant, aucun désavantage en relation avec la bonne exécution de ses tâches, qu'elle soit ou non employée par l'organisation.
6. Les mandataires disposent en permanence et sans interruption d'au moins une personne chargée de veiller au respect de la réglementation et possédant l'expertise requise dans le domaine de la réglementation des dispositifs médicaux de diagnostic in vitro dans l'Union. Cette expertise est attestée par l'une des qualifications suivantes:
a) |
un diplôme, un certificat ou un autre document de certification formelle sanctionnant des études universitaires en droit, en médecine, en pharmacie, en ingénierie ou dans une autre discipline scientifique pertinente, ou un cycle de cours reconnu équivalent par l'État membre concerné, et une expérience professionnelle d'au moins un an dans le domaine de la réglementation ou des systèmes de gestion de la qualité en rapport avec les dispositifs médicaux de diagnostic in vitro; |
b) |
une expérience professionnelle de quatre ans dans le domaine de la réglementation ou des systèmes de gestion de la qualité en rapport avec les dispositifs médicaux de diagnostic in vitro. |
Article 16
Cas dans lesquels les obligations des fabricants s'appliquent aux importateurs, aux distributeurs ou à d'autres personnes
1. Un distributeur, un importateur ou une autre personne physique ou morale s'acquitte des obligations incombant aux fabricants en rapport avec l'une des tâches suivantes:
a) |
mettre à disposition sur le marché un dispositif sous son nom propre, sous sa raison sociale ou sous sa marque déposée, sauf si un distributeur ou un importateur conclut avec le fabricant un accord selon lequel ce dernier est mentionné en tant que tel sur l'étiquette et demeure responsable du respect des exigences imposées aux fabricants par le présent règlement; |
b) |
modifier la destination d'un dispositif déjà mis sur le marché ou mis en service; |
c) |
modifier un dispositif déjà mis sur le marché ou mis en service d'une manière telle que cela peut influer sur la conformité avec les exigences applicables. |
Le premier alinéa ne s'applique pas aux personnes qui, sans être considérées comme des fabricants au sens de l'article 2, point 23), assemblent un dispositif déjà sur le marché ou l'adaptent à l'intention d'un patient donné sans en modifier la destination.
2. Aux fins du paragraphe 1, point c), ne sont pas considérées comme des modifications d'un dispositif susceptibles d'influer sur la conformité avec les exigences applicables:
a) |
la fourniture, traduction comprise, des informations fournies par le fabricant en application de l'annexe I, section 20, relatives à un dispositif déjà mis sur le marché, et des informations complémentaires nécessaires à la commercialisation du dispositif dans l'État membre concerné; |
b) |
les modifications apportées au conditionnement extérieur d'un dispositif déjà mis sur le marché, y compris toute modification de la taille du conditionnement, si le reconditionnement est nécessaire à la commercialisation du dispositif dans l'État membre concerné et s'il est effectué dans des conditions telles qu'il n'altère en aucune façon l'état d'origine du dispositif. Dans le cas de dispositifs mis sur le marché à l'état stérile, il est présumé que l'état d'origine du dispositif est altéré si le conditionnement nécessaire pour en préserver l'état stérile est ouvert, endommagé ou altéré de toute autre manière par le reconditionnement. |
3. Un distributeur ou un importateur qui réalise l'une des activités mentionnées au paragraphe 2, points a) et b), indique sur le dispositif ou, si c'est impossible, sur son conditionnement ou dans un document accompagnant le dispositif, l'activité effectuée, ainsi que son nom, sa raison sociale ou sa marque déposée, son siège social et l'adresse à laquelle il peut être joint afin de pouvoir établir son emplacement.
Les distributeurs et les importateurs veillent à disposer d'un système de gestion de la qualité prévoyant des procédures qui garantissent que la traduction des informations est fidèle et à jour, que les activités mentionnées au paragraphe 2, points a) et b), sont réalisées par des moyens et dans des conditions qui préservent l'état d'origine du dispositif et que le conditionnement du dispositif reconditionné n'est ni défectueux, ni de piètre qualité, ni en mauvais état. Le système de gestion de la qualité comporte, entre autres, des procédures garantissant que le distributeur ou l'importateur est informé de toute mesure corrective prise par le fabricant en rapport avec le dispositif en question afin de résoudre des problèmes de sécurité ou de mettre le dispositif en conformité avec le présent règlement.
4. Au moins vingt-huit jours avant la mise à disposition sur le marché du dispositif réétiqueté ou reconditionné, les distributeurs ou importateurs effectuant toute activité visée au paragraphe 2, points a) et b), informent le fabricant et l'autorité compétente de l'État membre dans lequel ils entendent mettre le dispositif à disposition de l'intention mettre le dispositif réétiqueté ou reconditionné à disposition et fournissent, sur demande, au fabricant et à l'autorité compétente, un exemplaire ou une maquette du dispositif réétiqueté ou reconditionné, accompagné de toute étiquette et toute notice d'utilisation traduites. Dans ce même délai de vingt-huit jours, le distributeur ou l'importateur transmet à l'autorité compétente un certificat, délivré par un organisme notifié désigné pour le type de dispositifs faisant l'objet des activités mentionnées au paragraphe 2, points a) et b), attestant que le système de gestion de la qualité du distributeur ou de l'importateur est conforme aux exigences énoncées au paragraphe 3.
Article 17
Déclaration de conformité UE
1. La déclaration de conformité UE atteste que les exigences du présent règlement ont été respectées. Le fabricant met régulièrement à jour la déclaration de conformité UE. La déclaration de conformité UE contient, au minimum, les informations qui figurent à l'annexe IV et est traduite dans une ou des langues officielles de l'Union requises par le ou les États membres dans lesquels le dispositif est mis à disposition.
2. Lorsque, en ce qui concerne des aspects ne relevant pas du présent règlement, des dispositifs font l'objet d'autres actes législatifs de l'Union qui imposent aussi une déclaration de conformité UE du fabricant attestant que le respect des exigences de ces actes législatifs a été démontré, une seule déclaration de conformité UE est établie pour tous les actes de l'Union applicables au dispositif. La déclaration contient toutes les informations nécessaires à l'identification des actes législatifs de l'Union auxquels la déclaration se rapporte.
3. Lors de l'établissement de la déclaration de conformité UE, le fabricant assume la responsabilité du respect des exigences du présent règlement et de tous les autres actes législatifs de l'Union applicables au dispositif.
4. La Commission est habilitée à adopter des actes délégués conformément à l'article 108 pour modifier le contenu minimal de la déclaration de conformité UE prévu à l'annexe IV eu égard aux progrès techniques.
Article 18
Marquage de conformité CE
1. Les dispositifs, autres que les dispositifs devant faire l'objet d'une étude des performances, réputés conformes aux exigences du présent règlement portent le marquage de conformité CE présenté à l'annexe V.
2. Le marquage CE est soumis aux principes généraux énoncés à l'article 30 du règlement (CE) no 765/2008.
3. Le marquage CE est apposé de façon visible, lisible et indélébile sur le dispositif ou sur le conditionnement qui en garantit la stérilité. Si la nature du dispositif ne permet pas cette apposition ou ne le justifie pas, le marquage CE est apposé sur le conditionnement. Le marquage CE figure aussi dans toute notice d'utilisation et sur tout conditionnement commercial.
4. Le marquage CE est apposé avant la mise sur le marché du dispositif. Il peut être suivi d'un pictogramme ou de tout autre marquage indiquant un risque ou un usage particulier.
5. Le cas échéant, le marquage CE est suivi du numéro d'identification de l'organisme notifié responsable des procédures d'évaluation de la conformité prévues à l'article 48. Le numéro d'identification est également indiqué dans tous les documents publicitaires mentionnant qu'un dispositif est conforme aux exigences applicables au marquage CE.
6. Lorsque des dispositifs relèvent d'autres actes législatifs de l'Union qui prévoient aussi l'apposition du marquage CE, le marquage CE indique que les dispositifs satisfont également aux exigences de ces autres actes législatifs.
Article 19
Dispositifs destinés à des usages particuliers
1. Les États membres ne font pas obstacle aux dispositifs devant faire l'objet d'une étude des performances qui sont fournis à cette fin à des laboratoires ou d'autres établissements s'ils remplissent les conditions énoncées aux articles 57 à 76 et dans les actes d'exécution adoptés conformément à l'article 77.
2. Les dispositifs visés au paragraphe 1 ne portent pas le marquage CE, à l'exception des dispositifs visés à l'article 70.
3. Les États membres ne font pas obstacle à la présentation de dispositifs qui ne sont pas conformes au présent règlement lors de foires commerciales, d'expositions, de démonstrations ou d'événements similaires, à la condition qu'une marque visible indique clairement que ces dispositifs sont destinés exclusivement à la présentation ou à la démonstration et ne peuvent être mis à disposition avant d'avoir été mis en conformité avec le présent règlement.
Article 20
Parties et éléments
1. Toute personne physique ou morale qui met à disposition sur le marché un article spécifiquement destiné à remplacer une partie intégrante ou un élément identique ou similaire d'un dispositif défaillant ou usé afin de maintenir ou de rétablir la fonction du dispositif sans en altérer les performances, les caractéristiques de sécurité ou la destination, veille à ce que l'article ne compromette pas la sécurité et les performances du dispositif. Des pièces justificatives sont tenues à la disposition des autorités compétentes des États membres.
2. Un article destiné à remplacer une partie ou un élément d'un dispositif et qui en modifie considérablement les performances, les caractéristiques de sécurité ou la destination est considéré comme un dispositif et respecte les exigences énoncées par le présent règlement.
Article 21
Libre circulation
Sauf indication contraire dans le présent règlement, les États membres ne refusent pas, n'interdisent pas et ne restreignent pas la mise à disposition sur le marché ou la mise en service sur leur territoire de dispositifs conformes aux exigences du présent règlement.
CHAPITRE III
IDENTIFICATION ET TRAÇABILITÉ DES DISPOSITIFS, ENREGISTREMENT DES DISPOSITIFS ET DES OPÉRATEURS ÉCONOMIQUES, RÉSUMÉ DES CARACTÉRISTIQUES DE SÉCURITÉ ET DES PERFORMANCES CLINIQUES ET BASE DE DONNÉES EUROPÉENNE SUR LES DISPOSITIFS MÉDICAUX
Article 22
Identification dans la chaîne d'approvisionnement
1. Les distributeurs et les importateurs coopèrent avec les fabricants ou leurs mandataires pour atteindre un niveau approprié de traçabilité des dispositifs.
2. Les opérateurs économiques sont en mesure d'identifier, pour l'autorité compétente et pour la durée visée à l'article 10, paragraphe 7:
a) |
tout opérateur économique auquel ils ont directement fourni un dispositif; |
b) |
tout opérateur économique qui leur a directement fourni un dispositif; |
c) |
tout établissement de santé ou professionnel de la santé auquel ils ont directement fourni un dispositif. |
Article 23
Nomenclature des dispositifs médicaux
Afin de faciliter le fonctionnement de la base de données européenne sur les dispositifs médicaux (Eudamed) visée à l'article 33 du règlement (UE) 2017/745, la Commission fait en sorte que les fabricants et les autres personnes physiques ou morales tenues par le présent règlement d'utiliser cette nomenclature aient accès gratuitement à une nomenclature des dispositifs médicaux internationalement reconnue. La Commission s'efforce également de faire en sorte que cette nomenclature soit accessible gratuitement à d'autres parties prenantes, dans la mesure où cela est raisonnablement possible.
Article 24
Système d'identification unique des dispositifs
1. Le système d'identification unique des dispositifs (ci-après dénommé «système IUD») décrit à l'annexe VI, partie C, permet l'identification et facilite la traçabilité des dispositifs, autres que les dispositifs devant faire l'objet d'une étude des performances, et prévoit ce qui suit:
a) |
la production d'un IUD comprenant:
|
||||
b) |
l'application de l'IUD sur l'étiquette du dispositif ou sur son conditionnement; |
||||
c) |
l'enregistrement de l'IUD par les opérateurs économiques, les établissements de santé et les professionnels de la santé, conformément aux conditions fixées respectivement aux paragraphes 8 et 9; |
||||
d) |
l'établissement d'un système électronique d'identification unique des dispositifs (ci-après dénommé «base de données IUD») conformément à l'article 28 du règlement (UE) 2017/745. |
2. La Commission désigne, au moyen d'actes d'exécution, une ou plusieurs entités chargées de mettre en œuvre un système d'attribution d'IUD en application du présent règlement (ci-après dénommé «entité d'attribution»). Ces entités satisfont à tous les critères suivants:
a) |
l'entité est une organisation dotée de la personnalité juridique; |
||||||
b) |
son système d'attribution d'IUD permet l'identification d'un dispositif tout au long de sa distribution et son utilisation conformément aux exigences du présent règlement; |
||||||
c) |
son système d'attribution d'IUD est conforme aux normes internationales applicables; |
||||||
d) |
l'entité donne accès à son système d'attribution d'IUD à tous les utilisateurs intéressés selon des modalités et des conditions prédéterminées et transparentes; |
||||||
e) |
l'entité fait en sorte:
|
Lorsqu'elle désigne les entités d'attribution, la Commission s'efforce de veiller à ce que les supports d'IUD définis à l'annexe VI, partie C, soient lisibles en toute circonstance quel que soit le système utilisé par l'entité d'attribution, en vue de réduire le plus possible la charge financière et administrative pour les opérateurs économiques, les établissements de santé et les professionnels de la santé.
3. Avant de mettre sur le marché un dispositif autre qu'un dispositif devant faire l'objet d'une étude des performances, le fabricant attribue au dispositif et, le cas échéant, à tous les niveaux de conditionnement supérieurs, un IUD créé en conformité avec les règles de l'entité d'attribution désignée par la Commission en vertu du paragraphe 2.
Avant de mettre sur le marché un dispositif autre qu'un dispositif devant faire l'objet d'une étude des performances, le fabricant doit assurer que les informations visées à l'annexe V, partie B, concernant le dispositif en question sont correctement présentées et transmises à la base de données IUD visée à l'article 25.
4. Les supports d'IUD sont apposés sur l'étiquette du dispositif et sur tous les niveaux de conditionnement supérieurs. Les niveaux de conditionnement supérieurs n'incluent pas les conteneurs de transport.
5. Les IUD sont utilisés aux fins de la notification d'incidents graves et de mesures correctives de sécurité en application de l'article 82.
6. L'IUD-ID de base, tel qu'il est défini à l'annexe VI, partie C, du dispositif figure sur la déclaration de conformité UE visée à l'article 17.
7. Le fabricant maintient à jour une liste de tous les IUD qu'il a attribués, qui fait partie de la documentation technique visée à l'annexe II.
8. Les opérateurs économiques enregistrent et conservent, de préférence par des moyens électroniques, l'IUD des dispositifs qu'ils ont fournis ou qu'on leur a fournis, si ceux-ci font partie des dispositifs et catégories ou groupes de dispositifs déterminés par un acte adopté conformément au paragraphe 11, point a).
9. Les États membres encouragent les établissements de santé à enregistrer et conserver, de préférence par des moyens électroniques, l'IUD des dispositifs qu'on leur a fournis, et peuvent exiger qu'ils le fassent.
Les États membres encouragent les professionnels de la santé à enregistrer et conserver, de préférence par des moyens électroniques, l'IUD des dispositifs qu'on leur a fournis, et peuvent exiger qu'ils le fassent.
10. La Commission est habilitée à adopter des actes délégués conformément à l'article 108:
a) |
pour modifier la liste des informations établie à l'annexe VI, partie B, eu égard aux progrès techniques; et |
b) |
pour modifier l'annexe VI eu égard aux avancées et aux progrès techniques intervenus sur le plan international dans le domaine de l'identification unique des dispositifs. |
11. La Commission peut, au moyen d'actes d'exécution, préciser les modalités et les aspects procéduraux du système IUD en vue de son application harmonisée pour ce qui concerne les points suivants:
a) |
la détermination des dispositifs et catégories ou groupes de dispositifs auxquels l'obligation visée au paragraphe 8 s'applique; |
b) |
l'indication des données devant figurer dans l'IUD-IP de dispositifs ou groupes de dispositifs particuliers. |
Les actes d'exécution visés au premier alinéa sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
12. Lorsqu'elle adopte les actes visés au paragraphe 11, la Commission tient compte de tous les points suivants:
a) |
la confidentialité et la protection des données visées respectivement aux articles 102 et 103; |
b) |
la méthode fondée sur les risques; |
c) |
le rapport coût-efficacité des actes; |
d) |
la convergence des systèmes IUD mis au point au niveau international; |
e) |
la nécessité d'éviter les doubles emplois dans le système IUD; |
f) |
les besoins des systèmes de soins de santé des États membres et, dans la mesure du possible, la compatibilité avec d'autres systèmes d'identification des dispositifs médicaux utilisés par les parties prenantes. |
Article 25
Base de données IUD
La Commission, après avoir consulté le GCDM, établit et gère une base de données IUD conformément aux conditions et modalités prévues à l'article 28 du règlement (UE) 2017/745.
Article 26
Enregistrement des dispositifs
1. Avant la mise sur le marché d'un dispositif, le fabricant attribue au dispositif, conformément aux règles de l'entité d'attribution visée à l'article 24, paragraphe 2, un IUD-ID de base tel qu'il est défini à l'annexe VI, partie C, et le transmet à la base de données IUD avec les autres principaux éléments de données visés à l'annexe VI, partie B, en rapport avec le dispositif en question.
2. Dans le cas des dispositifs qui font l'objet d'une évaluation de conformité visée à l'article 48, paragraphes 3 et 4, à l'article 48, paragraphe 7, deuxième alinéa, à l'article 48, paragraphe 8, et à l'article 48, paragraphe 9, deuxième alinéa, l'attribution d'un IUD-ID de base visé au paragraphe 1 du présent article s'effectue avant que le fabricant n'introduise une demande auprès d'un organisme notifié en vue de cette évaluation.
Dans le cas des dispositifs visés au premier alinéa, l'organisme notifié fait référence à l'IUD-ID de base sur le certificat délivré conformément à l'annexe XII, section 4, point a), et confirme dans Eudamed que les informations visées à l'annexe VI, partie 1, section 2.2, sont correctes. Après la délivrance du certificat correspondant et avant la mise sur le marché du dispositif, le fabricant transmet l'IUD-ID de base à la base de données IUD, ainsi que les autres principaux éléments de données visés à l'annexe VI, partie B, en rapport avec le dispositif en question.
3. Avant la mise sur le marché d'un dispositif, le fabricant enregistre ou, si elles sont déjà transmises, vérifie dans Eudamed les informations visées à l'annexe VI, partie A, section 2, à l'exception de celles visées en sa section 2.2, et tient, par la suite, ces informations à jour.
Article 27
Système électronique d'enregistrement des opérateurs économiques
1. La Commission, après avoir consulté le GCDM, établit et gère un système électronique afin de créer le numéro d'enregistrement unique visé à l'article 28, paragraphe 2, et de rassembler et traiter les informations utiles et nécessaires à l'identification du fabricant et, le cas échéant, du mandataire et de l'importateur. Les informations précises devant être transmises à ce système électronique par les opérateurs économiques sont énoncées à l'annexe VI, partie A, section 1.
2. Les États membres peuvent maintenir ou introduire des dispositions nationales concernant l'enregistrement des distributeurs des dispositifs qui ont été mis à disposition sur leur territoire.
3. Dans un délai de deux semaines à compter de la mise sur le marché d'un dispositif, les importateurs vérifient que le fabricant ou le mandataire a fourni au système électronique les informations visées au paragraphe 1.
Le cas échéant, les importateurs informent le fabricant ou le mandataire en question si les informations visées au paragraphe 1 sont manquantes ou incorrectes. Les importateurs ajoutent leurs coordonnées à la ou aux rubriques correspondantes.
Article 28
Enregistrement des fabricants, mandataires et importateurs
1. Avant la mise sur le marché d'un dispositif, les fabricants, les mandataires et les importateurs, transmettent au système électronique visé à l'article 27, aux fins de leur enregistrement, les informations visées à l'annexe VI, partie A, section 1, pour autant qu'ils ne se soient pas déjà enregistrés conformément au présent article. Lorsque la procédure d'évaluation de la conformité prévoit l'intervention d'un organisme notifié conformément à l'article 48, les informations visées à l'annexe VI, partie A, section 1, sont transmises à ce système électronique avant qu'une demande ne soit introduite auprès de l'organisme notifié.
2. Après avoir vérifié les données saisies conformément au paragraphe 1 du présent article, l'autorité compétente obtient un numéro d'enregistrement unique à partir du système électronique visé à l'article 27, qu'elle délivre au fabricant, à son mandataire ou à l'importateur.
3. Le fabricant utilise le numéro d'enregistrement unique lorsqu'il introduit une demande auprès d'un organisme notifié pour l'évaluation de conformité et pour accéder à Eudamed afin de s'acquitter de ses obligations au titre de l'article 26.
4. Dans un délai d'une semaine suivant tout changement en rapport avec les informations visées au paragraphe 1 du présent article, l'opérateur économique met à jour les données dans le système électronique visé à l'article 27.
5. Au plus tard un an après la transmission des informations en application du paragraphe 1, puis tous les deux ans, l'opérateur économique confirme l'exactitude des données. En cas de défaut de confirmation dans un délai de six mois suivant l'expiration de ces délais, tout État membre peut prendre des mesures correctives appropriées sur son territoire jusqu'à ce que l'opérateur économique satisfasse à cette obligation.
6. Sans préjudice de la responsabilité de l'opérateur économique à l'égard des données, l'autorité compétente vérifie les données confirmées visées à l'annexe VI, partie A, section 1.
7. Les données saisies dans le système électronique visé à l'article 27 conformément au paragraphe 1 du présent article sont mises à la disposition du public.
8. L'autorité compétence peut utiliser les données pour imposer une redevance au fabricant, au mandataire ou à l'importateur conformément à l'article 104.
Article 29
Résumé des caractéristiques de sécurité et des performances
1. Dans le cas de dispositifs de classe C et D, autres que des dispositifs devant faire l'objet d'une étude des performances, le fabricant produit un résumé des caractéristiques de sécurité et des performances.
Le résumé des caractéristiques de sécurité et des performances est écrit de manière à être clair pour l'utilisateur auquel le dispositif est destiné et, le cas échéant, pour le patient, et il est mis à la disposition du public via Eudamed.
Le projet de ce résumé fait partie de la documentation à fournir à l'organisme notifié intervenant dans l'évaluation de la conformité prévue à l'article 48 et est validé par cet organisme. Après sa validation, l'organisme notifié télécharge le résumé dans Eudamed. Le fabricant mentionne sur l'étiquette ou sur la notice d'utilisation où le résumé est disponible.
2. Le résumé des caractéristiques de sécurité et des performances contient au moins les éléments suivants:
a) |
l'identifiant du dispositif et du fabricant, y compris l'IUD-ID de base et le numéro d'enregistrement unique; |
b) |
la destination du dispositif ainsi que d'éventuelles indication ou contre-indications et les populations cibles; |
c) |
une description du dispositif, y compris une référence à la ou aux générations précédentes et aux variantes, s'il en existe, et une description des différences, ainsi que, le cas échéant, une description des accessoires, et des autres dispositifs et produits destinés à être utilisés en combinaison avec le dispositif; |
d) |
une référence aux normes harmonisées et aux spécifications communes appliquées; |
e) |
le résumé de l'évaluation des performances visée à l'annexe XIII et les informations pertinentes sur le SPAC; |
f) |
la traçabilité métrologique des valeurs assignées; |
g) |
le profil et la formation suggérés pour les utilisateurs; |
h) |
des informations sur les risques résiduels et sur tout effet indésirable, les mises en garde et les précautions. |
3. La Commission peut, au moyen d'actes d'exécution, prescrire la forme et la présentation des données devant figurer dans le résumé des caractéristiques de sécurité et des performances. Ces actes d'exécution sont adoptés en conformité avec la procédure consultative visée à l'article 107, paragraphe 2.
Article 30
Base de données européenne sur les dispositifs médicaux
1. La Commission, après avoir consulté le GCDM, établit, conserve et gère la base de données européenne sur les dispositifs médicaux (Eudamed) conformément aux conditions et modalités prévues aux articles 33 et 34 du règlement (UE) 2017/745.
2. Les systèmes électroniques suivants font partie d'Eudamed:
a) |
le système électronique d'enregistrement des dispositifs visé à l'article 26; |
b) |
la base de données IUD visée à l'article 25; |
c) |
le système électronique d'enregistrement des opérateurs économiques visé à l'article 27; |
d) |
le système électronique relatif aux organismes notifiés et aux certificats visé à l'article 52; |
e) |
le système électronique relatif aux études des performances visé à l'article 69; |
f) |
le système électronique relatif à la vigilance et à la surveillance après commercialisation prévu à l'article 87; |
g) |
le système électronique relatif à la surveillance du marché prévu à l'article 95. |
CHAPITRE IV
ORGANISMES NOTIFIÉS
Article 31
Autorités responsables des organismes notifiés
1. Tout État membre qui entend désigner un organisme d'évaluation de la conformité en tant qu'organisme notifié, ou a désigné un organisme notifié, pour mener des activités d'évaluation de la conformité en application du présent règlement nomme une autorité (ci-après dénommée «autorité responsable des organismes notifiés»), qui peut être composée d'entités constituantes distinctes en vertu de la législation nationale et est chargée de la mise en place et du suivi des procédures nécessaires à l'évaluation, à la désignation et à la notification des organismes d'évaluation de la conformité et du contrôle des organismes notifiés, ainsi que de leurs sous-traitants et filiales.
2. L'autorité responsable des organismes notifiés est établie, organisée et gérée d'une manière telle que l'objectivité et l'impartialité de ses activités sont préservées et que tout conflit d'intérêts avec les organismes d'évaluation de la conformité est évité.
3. L'autorité responsable des organismes notifiés est organisée de telle manière que la désignation ou la notification est décidée par des membres du personnel autres que ceux qui ont procédé à l'évaluation.
4. L'autorité responsable des organismes notifiés ne réalise aucune des activités que les organismes notifiés réalisent à des fins commerciales ou dans un contexte concurrentiel.
5. L'autorité responsable des organismes notifiés préserve les aspects confidentiels des informations qu'elle détient. Toutefois, elle échange des informations sur des organismes notifiés avec les autres États membres, la Commission et, si nécessaire, d'autres autorités chargées de la réglementation.
6. L'autorité responsable des organismes notifiés dispose en permanence d'un personnel compétent en nombre suffisant pour s'acquitter correctement de ses tâches.
Lorsque l'autorité responsable des organismes notifiés est distincte de l'autorité nationale compétente pour les dispositifs médicaux de diagnostic in vitro, elle veille à ce que cette dernière soit consultée sur les questions pertinentes.
7. Les États membres mettent à la disposition du public des informations générales concernant les mesures régissant l'évaluation, la désignation et la notification des organismes d'évaluation de la conformité et concernant le contrôle des organismes notifiés, ainsi que les modifications ayant un impact important sur ces tâches.
8. L'autorité responsable des organismes notifiés participe aux activités d'évaluation par les pairs prévues à l'article 44.
Article 32
Exigences applicables aux organismes notifiés
1. Les organismes notifiés s'acquittent des tâches pour lesquelles ils sont désignés en vertu du présent règlement. Ils se conforment aux exigences organisationnelles et générales et aux exigences en matière de gestion de la qualité, de ressources et de procédures qui sont nécessaires à l'exécution de ces tâches. Les organismes notifiés se conforment notamment aux exigences de l'annexe VII.
Afin de se conformer aux exigences visées au premier alinéa, les organismes notifiés disposent en permanence d'un personnel administratif, technique et scientifique en nombre suffisant conformément à l'annexe VII, section 3.1.1, et d'un personnel possédant une expertise clinique appropriée conformément à l'annexe VII, section 3.2.4, employé si possible par les organismes notifiés eux-mêmes.
Les membres du personnel visé à l'annexe VII, sections 3.2.3 et 3.2.7 sont employés par l'organisme notifié lui-même et ne sont ni des experts externes ni des sous-traitants.
2. Les organismes notifiés mettent à disposition de l'autorité responsable des organismes notifiés et lui soumettent sur demande toute la documentation pertinente, y compris celle du fabricant, afin de lui permettre de réaliser ses activités d'évaluation, de désignation, de notification, de contrôle et de surveillance et pour faciliter les évaluations décrites au présent chapitre.
3. Afin d'assurer l'application uniforme des exigences énoncées à l'annexe VII, la Commission peut adopter des actes d'exécution, dans la mesure nécessaire pour résoudre les problèmes liés à des différences d'interprétation et à l'application pratique. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
Article 33
Filiales et sous-traitance
1. Lorsqu'un organisme notifié sous-traite des tâches particulières relatives à l'évaluation de la conformité ou confie de telles tâches à une filiale, il vérifie que le sous-traitant ou la filiale respecte les exigences applicables énoncées à l'annexe VII et informe l'autorité responsable des organismes notifiés en conséquence.
2. Les organismes notifiés assument l'entière responsabilité des tâches réalisées en leur nom par des sous-traitants ou des filiales.
3. Les organismes notifiés mettent à la disposition du public une liste de leurs filiales.
4. Les activités d'évaluation de la conformité peuvent être sous-traitées ou confiées à une filiale pour autant que la personne morale ou physique ayant demandé l'évaluation de la conformité ait été informée en conséquence.
5. Les organismes notifiés tiennent à la disposition de l'autorité responsable des organismes notifiés tous les documents pertinents concernant la vérification des qualifications du sous-traitant ou de la filiale et des tâches qu'ils réalisent en vertu du présent règlement.
Article 34
Demande de désignation d'organismes d'évaluation de la conformité
1. Les organismes d'évaluation de la conformité introduisent une demande de désignation auprès de l'autorité responsable des organismes notifiés.
2. La demande précise les activités d'évaluation de la conformité telles qu'elles sont définies par le présent règlement et les types de dispositifs pour lesquels l'organisme demande à être désigné, et est accompagnée des documents attestant le respect de l'annexe VII.
En ce qui concerne les exigences organisationnelles et générales et les exigences en matière de gestion de la qualité énoncées à l'annexe VII, sections 1 et 2, un certificat d'accréditation en cours de validité et le rapport d'évaluation correspondant délivrés par un organisme national d'accréditation conformément au règlement (CE) no 765/2008 peuvent être transmis et sont pris en considération lors de l'évaluation décrite à l'article 35. Toutefois, le demandeur met à disposition, sur demande, toute la documentation visée au premier alinéa pour attester le respect de ces exigences.
3. L'organisme notifié met à jour les documents visés au paragraphe 2 dès que des changements pertinents interviennent afin de permettre à l'autorité responsable des organismes notifiés de contrôler et de vérifier que toutes les exigences énoncées à l'annexe VII demeurent observées.
Article 35
Évaluation de la demande
1. L'autorité responsable des organismes notifiés vérifie, dans un délai de trente jours, que la demande visée à l'article 34 est complète et invite le demandeur à fournir toute information manquante. Lorsque la demande est complète, cette autorité nationale l'adresse à la Commission.
L'autorité responsable des organismes notifiés examine la demande et les documents qui l'accompagnent conformément à ses propres procédures et produit un rapport d'évaluation préliminaire.
2. L'autorité responsable des organismes notifiés soumet le rapport d'évaluation préliminaire à la Commission, qui le transmet immédiatement au GCDM.
3. Dans un délai de quatorze jours suivant la transmission du rapport visée au paragraphe 2 du présent article, la Commission, conjointement avec le GCDM, désigne une équipe d'évaluation conjointe composée de trois experts, à moins que des circonstances particulières ne nécessitent un nombre d'experts différent, choisis dans la liste visée à l'article 36. Un de ces experts est un représentant de la Commission qui coordonne les activités de l'équipe d'évaluation conjointe. Les deux autres experts viennent d'États membres autres que celui dans lequel est établi l'organisme d'évaluation de la conformité demandeur.
L'équipe d'évaluation conjointe réunit des experts compétents qualifiés pour évaluer les activités d'évaluation de la conformité et les types de dispositifs qui font l'objet de la demande ou, en particulier lorsque la procédure d'évaluation est engagée conformément à l'article 43, paragraphe 3, pour veiller à ce que le problème spécifique puisse être évalué comme il convient.
4. Dans un délai de 90 jours suivant sa désignation, l'équipe d'évaluation conjointe passe en revue les documents fournis à l'appui de la demande en application de l'article 34. L'équipe d'évaluation conjointe peut fournir en retour à l'autorité responsable des organismes notifiés des informations relatives à la demande et à l'évaluation qui est prévue sur place ou lui demander des précisions à ce sujet.
L'autorité responsable des organismes notifiés ainsi que l'équipe d'évaluation conjointe planifient et réalisent une évaluation sur place de l'organisme d'évaluation de la conformité demandeur et, le cas échéant, de ses filiales ou sous-traitants, situés dans ou hors de l'Union, qui interviendront dans la procédure d'évaluation de la conformité.
L'évaluation sur place de l'organisme demandeur est menée par l'autorité responsable des organismes notifiés.
5. Les cas de non-respect, par un organisme d'évaluation de la conformité demandeur, des exigences énoncées à l'annexe VII sont constatés durant la procédure d'évaluation et sont examinés conjointement par l'autorité responsable des organismes notifiés et l'équipe d'évaluation conjointe en vue de parvenir à un consensus et de résoudre toute divergence d'opinion sur l'évaluation de la demande.
À l'issue de l'évaluation sur place, l'autorité responsable des organismes notifiés transmet à l'organisme d'évaluation de la conformité demandeur une liste des cas de non-respect constatés durant l'évaluation ainsi qu'un résumé de l'évaluation effectuée par l'équipe d'évaluation conjointe.
Dans un délai donné, l'organisme d'évaluation de la conformité demandeur soumet à l'autorité nationale un plan de mesures correctives et préventives en vue de remédier aux cas de non-respect.
6. Dans un délai de trente jours suivant la réalisation de l'évaluation sur place, l'équipe d'évaluation conjointe documente toute divergence d'opinion persistant au sujet de l'évaluation et en fait part à l'autorité responsable des organismes notifiés.
7. L'autorité responsable des organismes notifiés évalue, après avoir reçu un plan de mesures correctives et préventives établi par l'organisme demandeur, s'il a été correctement remédié aux cas de non-respect constatés durant l'évaluation. Ce plan indique la cause essentielle des cas de non-respect constatés et comprend un calendrier de mise en œuvre des mesures qui y sont prévues.
Après avoir confirmé le plan de mesures correctives et préventives, l'autorité responsable des organismes notifiés transmet ce plan et son avis sur celui-ci à l'équipe d'évaluation conjointe. L'équipe d'évaluation conjointe peut demander des précisions supplémentaires et des modifications à l'autorité responsable des organismes notifiés.
L'autorité responsable des organismes notifiés rédige son rapport définitif d'évaluation, qui comprend notamment les éléments suivants:
— |
le résultat de l'évaluation, |
— |
la confirmation que les mesures correctives et préventives ont été correctement prises en compte et, si nécessaire, mises en œuvre, |
— |
toute divergence d'opinion persistant avec l'équipe d'évaluation conjointe et, le cas échéant, |
— |
une recommandation concernant le champ couvert par la désignation. |
8. L'autorité responsable des organismes notifiés soumet son rapport définitif d'évaluation et, s'il y a lieu, le projet de désignation à la Commission, au GCDM et à l'équipe d'évaluation conjointe.
9. L'équipe d'évaluation conjointe communique à la Commission un avis définitif sur le rapport d'évaluation élaboré par l'autorité responsable des organismes notifiés et, s'il y a lieu, le projet de désignation dans un délai de vingt-et-un jours suivant la date de réception de ces documents, avis que la Commission transmet immédiatement au GCDM. Dans un délai de quarante-deux jours suivant la réception de l'avis de l'équipe d'évaluation conjointe, le GCDM émet une recommandation relative au projet de désignation, dont l'autorité responsable des organismes notifiés tient dûment compte lorsqu'elle statue sur la désignation de l'organisme notifié.
10. La Commission peut, au moyen d'actes d'exécution, adopter des mesures fixant les modalités définissant les procédures et les rapports concernant la demande de désignation visée à l'article 34 et l'évaluation de la demande prévue au présent article. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
Article 36
Nomination d'experts pour l'évaluation conjointe des demandes de notification
1. Les États membres et la Commission nomment des experts qualifiés pour évaluer les organismes d'évaluation de la conformité dans le domaine des dispositifs médicaux de diagnostic in vitro en vue de leur participation aux activités visées aux articles 35 et 44.
2. La Commission tient une liste des experts nommés en application du paragraphe 1 du présent article, et des informations sur leur domaine de compétences et leur expertise spécifiques. Cette liste est mise à la disposition des autorités compétentes des États membres via le système électronique visé à l'article 52.
Article 37
Exigences linguistiques
Tous les documents requis au titre des articles 34 et 35 sont rédigés dans une ou des langues définies par l'État membre concerné.
En application du premier alinéa, les États membres envisagent l'adoption et l'utilisation d'une langue couramment comprise dans le domaine médical pour tout ou partie de la documentation concernée.
La Commission fournit les traductions de la documentation ou parties de celle-ci conformément aux articles 34 et 35 dans une langue officielle de l'Union de telle sorte qu'elle puisse être aisément comprise par l'équipe d'évaluation conjointe désignée en application de l'article 35, paragraphe 3.
Article 38
Procédure de désignation et de notification
1. Les États membres ne peuvent désigner que les organismes d'évaluation de la conformité pour lesquels l'évaluation en application de l'article 35 est achevée et qui satisfont à l'annexe VII.
2. Les États membres notifient à la Commission et aux autres États membres les organismes d'évaluation de la conformité qu'ils ont désignés, à l'aide de l'outil de notification électronique de la base de données des organismes notifiés mis en place et géré par la Commission (NANDO).
3. La notification précise clairement, en utilisant les codes visés au paragraphe 13 du présent article, le champ couvert par la désignation et indique les activités d'évaluation de la conformité définies dans le présent règlement et les types de dispositifs que l'organisme notifié est habilité à évaluer et, sans préjudice de l'article 40, toute condition associée à la désignation.
4. La notification est assortie du rapport d'évaluation définitif de l'autorité responsable des organismes notifiés, de l'avis définitif de l'équipe d'évaluation conjointe visé à l'article 35, paragraphe 9, et de la recommandation du GCDM. Lorsque l'État membre notifiant ne suit pas la recommandation du GCDM, sa décision est dûment motivée.
5. Sans préjudice de l'article 40, l'État membre notifiant informe la Commission et les autres États membres de toute condition associée à la désignation et fournit des pièces justificatives relatives aux dispositions prises pour garantir que l'organisme notifié sera contrôlé régulièrement et satisfera sans discontinuer aux exigences énoncées à l'annexe VII.
6. Dans un délai de vingt-huit jours suivant la notification visée au paragraphe 2, un État membre ou la Commission peut formuler des objections écrites, exposant ses arguments, à l'encontre de l'organisme notifié ou de son contrôle par l'autorité responsable des organismes notifiés. En l'absence d'objection, la Commission publie la notification dans NANDO dans un délai de quarante-deux jours après en avoir été informée conformément au paragraphe 2.
7. Lorsqu'un État membre ou la Commission formule des objections en application du paragraphe 6, la Commission saisit le GCDM du dossier dans un délai de dix jours suivant l'expiration du délai visé au paragraphe 6. Après consultation des parties concernées, le GCDM rend son avis dans un délai de quarante jours suivant la date à laquelle il a été saisi du dossier. Si le GCDM est d'avis que la notification est recevable, la Commission la publie dans NANDO dans un délai de quatorze jours.
8. Lorsque, après avoir été consulté conformément au paragraphe 7, le GCDM confirme l'objection ou en formule une autre, l'État membre notifiant répond par écrit à l'avis du GCDM dans un délai de quarante jours suivant sa réception. La réponse concerne les objections soulevées dans l'avis et énonce les raisons pour lesquelles l'État membre notifiant décide de désigner ou non l'organisme d'évaluation de la conformité.
9. Lorsque l'État membre notifiant, ayant énoncé ses raisons conformément au paragraphe 8, décide de confirmer sa décision de désigner l'organisme d'évaluation de la conformité, la Commission publie la notification dans NANDO dans un délai de quatorze jours après en avoir été informée.
10. Lors de la publication de la notification dans NANDO, la Commission ajoute les informations relatives à la notification de l'organisme notifié au système électronique visé à l'article 52, de même que les documents mentionnés au paragraphe 4 du présent article ainsi que l'avis et la réponse visés aux paragraphes 7 et 8 du présent article.
11. La désignation prend effet le jour suivant celui de la publication de la notification dans NANDO. La notification publiée indique le champ des activités légales d'évaluation de la conformité de l'organisme notifié.
12. L'organisme d'évaluation de la conformité concerné ne peut mener les activités d'un organisme notifié qu'après la prise d'effet de la désignation conformément au paragraphe 11.
13. Au plus tard le 26 novembre 2017, la Commission dresse, au moyen d'actes d'exécution, une liste des codes et des types correspondants de dispositifs aux fins de préciser le champ couvert par la désignation des organismes notifiés. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3. Après avoir consulté le GCDM, la Commission peut mettre à jour cette liste, notamment sur la base des informations provenant des activités de coordination visées à l'article 44.
Article 39
Numéro d'identification et liste des organismes notifiés
1. La Commission attribue un numéro d'identification à chaque organisme notifié dont la notification prend effet en application de l'article 38, paragraphe 11. Elle attribue un numéro d'identification unique, même si l'organisme est notifié en application de plusieurs actes législatifs de l'Union. S'ils sont désignés conformément au présent règlement, les organismes notifiés en vertu de la directive 98/79/CE conservent le numéro d'identification qui leur a été attribué au titre de cette directive.
2. La Commission rend publique dans NANDO la liste des organismes notifiés en application du présent règlement, laquelle indique les numéros d'identification qui leur ont été attribués ainsi que les activités d'évaluation de la conformité définies dans le présent règlement et les types de dispositifs pour lesquels ils sont notifiés. Elle met également cette liste à disposition via le système électronique visé à l'article 52. La Commission veille à ce que la liste soit tenue à jour.
Article 40
Surveillance et réévaluation des organismes notifiés
1. Les organismes notifiés informent sans tarder, et au plus tard dans un délai de quinze jours, l'autorité responsable des organismes notifiés des changements pertinents susceptibles d'influer sur le respect des exigences énoncées à l'annexe VII ou sur leur capacité à réaliser les activités d'évaluation de la conformité des dispositifs pour lesquels ils ont été désignés.
2. Les autorités responsables des organismes notifiés contrôlent les organismes notifiés établis sur leur territoire ainsi que leurs filiales et leurs sous-traitants pour veiller à ce que les exigences et obligations qui leur incombent énoncées dans le présent règlement demeurent respectées. Les organismes notifiés fournissent, à la demande de leur autorité responsable des organismes notifiés, toutes les informations et tous les documents nécessaires pour permettre à l'autorité, à la Commission et aux autres États membres de vérifier le respect de ces exigences et obligations.
3. Lorsque la Commission ou l'autorité d'un État membre soumet une demande à un organisme notifié établi sur le territoire d'un autre État membre concernant une évaluation de la conformité réalisée par ledit organisme notifié, elle adresse une copie de cette demande à l'autorité responsable des organismes notifiés de l'État membre en question. L'organisme notifié concerné répond à la demande sans tarder, et au plus tard dans un délai de quinze jours. L'autorité responsable des organismes notifiés de l'État membre dans lequel l'organisme a son siège veille à ce que l'organisme notifié réponde aux demandes des autorités de tout autre État membre ou de la Commission, à moins qu'il y ait une raison légitime de ne pas le faire, auquel cas la question peut être soumise au GCDM.
4. Au moins une fois par an, les autorités responsables des organismes notifiés évaluent une nouvelle fois si les organismes notifiés établis sur leur territoire respectif et, le cas échéant, les filiales et sous-traitants placés sous la responsabilité desdits organismes notifiés respectent toujours les exigences et obligations qui leur incombent énoncées à l'annexe VII. Cet examen prévoit un audit sur place de chacun des organismes notifiés et, si nécessaire, de leurs filiales et sous-traitants.
L'autorité responsable des organismes notifiés réalise ses activités de contrôle et d'évaluation selon un plan d'évaluation annuel visant à garantir qu'elle puisse effectivement contrôler qu'un organisme notifié continue de respecter les exigences du présent règlement. Ce plan contient un calendrier motivé exposant la fréquence d'évaluation de l'organisme notifié et, en particulier, des filiales et sous-traitants associés. L'autorité soumet au GCDM et à la Commission son plan annuel de contrôle ou d'évaluation pour chaque organisme notifié sous sa responsabilité.
5. Le contrôle des organismes notifiés par l'autorité responsable des organismes notifiés comporte des audits du personnel de l'organisme notifié, y compris, si nécessaire, du personnel des filiales et sous-traitants, réalisés en présence d'observateurs au moment où ledit personnel effectue l'évaluation des systèmes de gestion de la qualité des installations d'un fabricant.
6. Le contrôle d'organismes notifiés par l'autorité responsables des organismes notifiés tient compte des données provenant de la surveillance du marché, de la vigilance et de la surveillance après commercialisation en vue d'aider à orienter les activités concernées.
L'autorité responsable des organismes notifiés prévoit un suivi systématique des réclamations et autres informations, notamment celles transmises par d'autres États membres, susceptibles de donner à penser qu'un organisme notifié ne satisfait pas à ses obligations ou s'écarte de la pratique générale ou des pratiques exemplaires.
7. L'autorité responsable des organismes notifiés peut, en plus du contrôle régulier ou d'évaluations sur place, procéder à des examens à préavis limité, inopinés ou dus à une cause spécifique si cela est nécessaire pour traiter une question particulière ou vérifier le respect des exigences.
8. L'autorité responsable des organismes notifiés examine les évaluations de la documentation technique présentée par les fabricants, en particulier de documentations relatives aux évaluations des performances auxquelles ont procédé les organismes notifiés, comme précisé à l'article 41.
9. L'autorité responsable des organismes notifiés documente et documente tout cas de non-respect des exigences énoncées à l'annexe VII par l'organisme notifié et contrôle la mise en œuvre en temps utile des mesures correctives et préventives.
10. Trois ans après la notification d'un organisme notifié, puis tous les quatre ans par la suite, une nouvelle évaluation complète du respect des exigences énoncées à l'annexe VII par l'organisme notifié est réalisée par l'autorité responsable des organismes notifiés de l'État membre dans lequel l'organisme a son siège et par une équipe d'évaluation conjointe désignée aux fins de la procédure décrite aux articles 34 et 35.
11. La Commission est habilitée à adopter des actes délégués conformément à l'article 108 afin de modifier le paragraphe 10 du présent article en vue de modifier la fréquence des nouvelles évaluations complètes visées dans le paragraphe en question.
12. Les États membres adressent à la Commission et au GCDM, au moins une fois par an, un rapport rendant compte de leurs activités de contrôle et d'évaluation sur place à l'égard des organismes notifiés et, le cas échéant, des filiales et sous-traitants. Le rapport fournit les détails du résultat de ces activités, y compris les activités visées au paragraphe 7 et fait l'objet d'un traitement confidentiel par le GCDM et la Commission; il contient toutefois un résumé qui est rendu public.
Le résumé du rapport est transmis au système électronique visé à l'article 52.
Article 41
Examen de l'évaluation de la documentation technique et de la documentation relative à l'évaluation des performances effectuée par l'organisme notifié
1. Dans le cadre du contrôle permanent qu'elle exerce sur les organismes notifiés, l'autorité responsable des organismes notifiés examine un nombre approprié d'évaluations de la documentation technique présentée par les fabricants auxquelles a procédé l'organisme notifié, en particulier de documentations relatives aux évaluations des performances, afin de vérifier les conclusions tirées par cet organisme sur la base des informations fournies par le fabricant. Les évaluations effectuées par l'autorité responsable des organismes notifiés le sont à la fois hors site et sur place.
2. L'échantillonnage de dossiers à examiner conformément au paragraphe 1 fait l'objet d'une planification et est représentatif des types de dispositifs qui sont certifiés par l'organisme notifié, ainsi que des risques correspondants, en particulier les dispositifs à haut risque; il est justifié et documenté comme il convient dans un plan d'échantillonnage mis à la disposition du GCDM par l'autorité responsable des organismes notifiés, sur demande.
3. L'autorité responsable des organismes notifiés examine si l'évaluation à laquelle a procédé l'organisme notifié a été menée comme il convient et elle vérifie les procédures utilisées, la documentation associée et les conclusions tirées par cet organisme. Cette vérification porte notamment sur la documentation technique et la documentation relative aux évaluations des performances présentées par le fabricant, sur lesquelles l'organisme notifié a fondé son évaluation. La réalisation de ces examens s'appuie sur les spécifications communes.
4. Ces examens font également partie de la nouvelle évaluation des organismes notifiés conformément à l'article 40, paragraphe 10, et des activités d'évaluation conjointe visées à l'article 43, paragraphe 3. Ces examens sont réalisés en s'appuyant sur des compétences appropriées.
5. Sur la base des rapports des examens et évaluations réalisés par l'autorité responsable des organismes notifiés ou les équipes d'évaluation conjointe, des résultats des activités de surveillance du marché, de vigilance et de surveillance après commercialisation décrites au chapitre VII, du suivi permanent des progrès techniques, ou de la mise en évidence des préoccupations et des questions qui se font jour en matière de sécurité et de performances des dispositifs, le GCDM peut recommander que l'échantillonnage effectué au titre du présent article porte sur une proportion plus ou moins grande de la documentation technique et de la documentation relative à l'évaluation des performances évaluées par un organisme notifié.
6. La Commission peut, au moyen d'actes d'exécution, adopter des mesures fixant les modalités de l'examen des évaluations de la documentation technique et de la documentation relative à l'évaluation des performances visées au présent article et précisant les documents qui y sont liés et les dispositions en matière de coordination. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
Article 42
Modifications des désignations et des notifications
1. L'autorité responsable des organismes notifiés informe la Commission et les autres États membres de toute modification pertinente apportée à la désignation d'un organisme notifié.
Les procédures décrites aux articles 35 et 38 s'appliquent en cas d'extension du champ couvert par la désignation.
En cas de modification de la désignation autre qu'une extension de son champ, les procédures prévues aux paragraphes ci-après s'appliquent.
2. La Commission publie immédiatement la notification modifiée dans NANDO. La Commission introduit immédiatement les informations concernant la modification de la désignation de l'organisme notifié dans le système électronique visé à l'article 52.
3. Lorsqu'un organisme notifié décide de cesser ses activités d'évaluation de la conformité, il informe l'autorité responsable des organismes notifiés et les fabricants concernés dès que possible et, dans le cas d'un arrêt prévu de ses activités, un an avant de mettre un terme à ses activités. Les certificats peuvent rester valables pendant une période temporaire de neuf mois après l'arrêt des activités de l'organisme notifié, à condition qu'un autre organisme notifié confirme par écrit qu'il assumera la responsabilité des dispositifs concernés par ces certificats. Le nouvel organisme notifié procède à une évaluation complète des dispositifs concernés avant la fin de cette période, avant de délivrer de nouveaux certificats pour les dispositifs en question. Lorsque l'organisme notifié cesse ses activités, l'autorité responsable des organismes notifiés retire la désignation.
4. Lorsqu'une autorité responsable des organismes notifiés a établi qu'un organisme notifié ne satisfait plus aux exigences énoncées à l'annexe VII ou ne s'acquitte pas de ses obligations ou n'a pas mis en œuvre les mesures correctives nécessaires, elle suspend, restreint ou retire en tout ou en partie la désignation, selon la gravité du cas de non-respect de ces exigences ou de ces obligations. La suspension ne peut durer plus d'un an et peut être reconduite une fois pour la même durée.
L'autorité responsable des organismes notifiés informe immédiatement la Commission et les autres États membres de toute suspension, de toute restriction ou de tout retrait d'une désignation.
5. Lorsque sa désignation a été suspendue, restreinte ou retirée en tout ou en partie, l'organisme notifié en informe les fabricants concernés dans un délai maximal de dix jours.
6. En cas de restriction, de suspension ou de retrait d'une désignation, l'autorité responsable des organismes notifiés prend les mesures appropriées pour assurer que les dossiers de l'organisme notifié en question sont conservés et les tient à la disposition des autorités d'autres États membres responsables des organismes notifiés et des autorités responsables de la surveillance du marché, à leur demande.
7. En cas de restriction, de suspension ou de retrait d'une désignation, l'autorité responsable des organismes notifiés:
a) |
évalue l'incidence sur les certificats délivrés par l'organisme notifié; |
b) |
transmet un rapport sur ses conclusions à la Commission et aux autres États membres dans un délai de trois mois après avoir signalé la modification; |
c) |
exige de l'organisme notifié qu'il suspende ou retire, dans un délai raisonnable qu'elle détermine, tous les certificats délivrés à tort afin d'assurer la sécurité des dispositifs présents sur le marché; |
d) |
télécharge dans le système électronique visé à l'article 52 des informations relatives aux certificats dont elle a demandé la suspension ou le retrait; |
e) |
notifie à l'autorité compétente pour les dispositifs médicaux de diagnostic in vitro de l'État membre dans lequel le fabricant a son siège via le système électronique visé à l'article 52 les certificats dont elle a demandé la suspension ou le retrait. Cette autorité compétente prend les mesures appropriées si cela est nécessaire pour éviter un risque potentiel pour la santé ou la sécurité des patients, des utilisateurs ou d'autres personnes. |
8. À l'exception des certificats délivrés à tort, et lorsqu'une désignation a été suspendue ou restreinte, les certificats restent valables dans les cas suivants:
a) |
l'autorité responsable des organismes notifiés a confirmé, dans un délai d'un mois suivant la suspension ou la restriction, qu'il n'y a pas de problème de sécurité en liaison avec les certificats concernés par la suspension ou la restriction, et l'autorité responsable des organismes notifiés a défini un calendrier et les mesures prévues pour remédier à la suspension ou à la restriction; ou |
b) |
l'autorité responsable des organismes notifiés a confirmé qu'aucun certificat ayant trait à la suspension ne sera délivré, modifié ou délivré à nouveau pendant la période de suspension ou de restriction et indique si l'organisme notifié est en mesure de continuer à contrôler les certificats existants délivrés et à en être responsable pour la durée de la suspension ou de la restriction. Si l'autorité responsable des organismes notifiés considère que l'organisme notifié n'est pas en mesure de confirmer les certificats existants délivrés, le fabricant adresse à l'autorité compétente pour les dispositifs médicaux de diagnostic in vitro de l'État membre dans lequel le fabricant du dispositif faisant l'objet du certificat a son siège, dans un délai de trois mois à compter de la suspension ou de la restriction, la confirmation écrite qu'un autre organisme notifié qualifié assume temporairement les fonctions de contrôle de l'organisme notifié et continue d'assumer la responsabilité des certificats pour la durée de la suspension ou de la restriction. |
9. À l'exception des certificats délivrés à tort, et lorsqu'une désignation a été révoquée, les certificats restent valables pendant une durée de neuf mois dans les cas suivants:
a) |
l'autorité compétente pour les dispositifs médicaux de diagnostic in vitro de l'État membre dans lequel le fabricant du dispositif faisant l'objet du certificat a son siège a confirmé qu'il n'y a pas de problème de sécurité pour ce qui est des dispositifs en question; et |
b) |
un autre organisme notifié a confirmé par écrit qu'il assumera la responsabilité immédiate de ces dispositifs et qu'il achèvera leur évaluation dans un délai de douze mois à compter du retrait de la désignation. |
Dans le cas visé au premier alinéa, l'autorité nationale compétente pour les dispositifs médicaux de diagnostic in vitro de l'État membre dans lequel le fabricant du dispositif faisant l'objet du certificat a son siège peut prolonger à plusieurs reprises la durée de validité provisoire des certificats de trois mois supplémentaires, pour une durée totale maximale de douze mois.
L'autorité ou l'organisme notifié qui assume les fonctions de l'organisme notifié concerné par la modification de la désignation en informe immédiatement la Commission, les autres États membres et les autres organismes notifiés.
Article 43
Contestation de la compétence des organismes notifiés
1. La Commission procède, conjointement avec le GCDM, à une enquête à chaque fois qu'elle est avisée que des organismes notifiés, ou une ou plusieurs de leurs filiales ou un ou plusieurs de leurs sous-traitants, sont soupçonnés de ne plus respecter les exigences de l'annexe VII ou les obligations qui leur incombent. Elle veille à ce que l'autorité responsable des organismes notifiés concernée soit informée et ait la possibilité de procéder à une enquête à ce sujet.
2. L'État membre notifiant fournit à la Commission, sur demande, toutes les informations relatives à la désignation de l'organisme notifié concerné.
3. La Commission peut, conjointement avec le GCDM, entamer, le cas échéant, la procédure d'évaluation visée à l'article 35, paragraphes 3 et 5, dès lors qu'il existe des craintes plausibles quant au respect des exigences énoncées à l'annexe VII par un organisme notifié ou par une filiale ou un sous-traitant de l'organisme notifié et lorsque l'enquête de l'autorité responsable des organismes notifiés n'a pas levé tous les doutes, ou à la demande de l'autorité responsable des organismes notifiés. Le rapport et les résultats de cette évaluation suivent les principes fixés à l'article 35. En fonction de la sévérité de la question, la Commission peut aussi, conjointement avec le GCDM, demander que l'autorité responsable des organismes notifiés permette à un maximum deux experts figurant sur la liste établie conformément à l'article 36, de participer à une évaluation sur place dans le cadre des activités de contrôle et d'évaluation planifiées conformément à l'article 40 et selon le plan d'évaluation annuel visé à l'article 40, paragraphe 4.
4. Lorsque la Commission établit qu'un organisme notifié ne satisfait plus aux conditions de sa désignation, elle informe l'État membre notifiant en conséquence et l'invite à prendre les mesures correctives qui s'imposent, dont la suspension, la restriction ou le retrait de la désignation si nécessaire.
Si l'État membre ne prend pas les mesures correctives qui s'imposent, la Commission peut, au moyen d'actes d'exécution, suspendre, restreindre ou retirer la désignation. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3. La Commission notifie sa décision à l'État membre concerné et procède à la mise à jour de NANDO et du système électronique visé à l'article 52.
5. La Commission s'assure que toutes les informations confidentielles obtenues au cours de ses enquêtes sont traitées en conséquence.
Article 44
Évaluation par les pairs et échange d'expérience entre les autorités responsables des organismes notifiés
1. La Commission prévoit l'organisation d'un échange d'expérience et la coordination des pratiques administratives entre les autorités responsables des organismes notifiés. Cet échange porte notamment sur les éléments suivants:
a) |
l'élaboration de documents sur les bonnes pratiques liées aux activités des autorités responsables des organismes notifiés; |
b) |
l'élaboration de documents d'orientation à l'intention des organismes notifiés, en rapport avec l'application du présent règlement; |
c) |
la formation et qualification des experts visés à l'article 36; |
d) |
le suivi des tendances concernant les modifications des désignations et des notifications d'organismes notifiés, les retraits de certificats et les transferts entre organismes notifiés; |
e) |
le contrôle de l'application et du caractère applicable des codes relatifs au champ de la désignation visés à l'article 38, paragraphe 13; |
f) |
la mise en place d'un mécanisme d'évaluations par les pairs entre les autorités et la Commission; |
g) |
des méthodes pour l'information du public sur les activités de contrôle et de surveillance menées par les autorités et la Commission à l'égard des organismes notifiés en ce qui concerne les dispositifs médicaux. |
2. Les autorités responsables des organismes notifiés participent tous les trois ans à une évaluation par les pairs sur la base du mécanisme mis en place en application du paragraphe 1 du présent article. Ces évaluations s'effectuent en principe parallèlement aux évaluations conjointes sur place visées à l'article 35. Mais une autorité nationale peut également décider de les inclure dans ses activités de contrôle visées à l'article 40.
3. La Commission participe à l'organisation et fournit une assistance à la mise en œuvre du mécanisme d'évaluation par les pairs.
4. La Commission établit un rapport de synthèse annuel des activités d'évaluation par les pairs qui est rendu public.
5. La Commission peut, au moyen d'actes d'exécution, adopter des mesures fixant les modalités des mécanismes d'évaluation par les pairs, de la formation et de la qualification, ainsi que les documents qui y sont liés, comme indiqué au paragraphe 1 du présent article. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
Article 45
Coordination des organismes notifiés
La Commission veille à ce que les organismes notifiés coordonnent leurs activités et coopèrent dans le cadre du groupe de coordination des organismes notifiés visé à l'article 49 du règlement (UE) 2017/745.
Les organismes notifiés aux fins du présent règlement participent aux travaux de ce groupe.
Article 46
Listes de redevances standard
Les organismes notifiés établissent des listes de leurs redevances standard concernant les activités d'évaluation de la conformité qu'ils effectuent et rendent ces listes publiques.
CHAPITRE V
CLASSIFICATION ET ÉVALUATION DE LA CONFORMITÉ
Section 1
Classification
Article 47
Classification des dispositifs
1. Les dispositifs sont répartis en classe A, classe B, classe C et classe D en fonction de la destination des dispositifs et des risques qui leur sont inhérents. La classification est effectuée conformément à l'annexe VIII.
2. Tout litige entre le fabricant et l'organisme notifié concerné résultant de l'application de l'annexe VIII, est soumis pour décision à l'autorité compétente de l'État membre dans lequel le fabricant a son siège social. Lorsque le fabricant ne dispose pas d'un siège social dans l'Union et n'a pas encore désigné de mandataire, l'affaire est portée devant l'autorité compétente de l'État membre dans lequel le mandataire visé à l'annexe IX, section 2, deuxième alinéa, point b), dernier tiret, a son siège social. Lorsque l'organisme notifié concerné est établi dans un État membre autre que celui du fabricant, l'autorité compétente arrête sa décision après avoir consulté l'autorité compétente de l'État membre qui a désigné l'organisme notifié.
L'autorité compétente de l'État membre dans lequel le fabricant a son siège notifie sa décision au GCDM et à la Commission. La décision est communiquée sur demande.
3. À la demande d'un État membre, la Commission, après avoir consulté le GCDM, statue, au moyen d'actes d'exécution, sur les éléments suivants:
a) |
l'application de l'annexe VIII à un dispositif ou à une catégorie ou un groupe de dispositifs donné en vue de déterminer la classification des dispositifs en question; |
b) |
la reclassification d'un dispositif ou d'une catégorie ou d'un groupe de dispositifs pour des raisons de santé publique fondées sur de nouvelles données scientifiques, ou sur toute information devenant disponible au cours des activités de vigilance et de surveillance du marché, par dérogation à l'annexe VIII. |
4. La Commission peut aussi, de sa propre initiative et après avoir consulté le GCDM, statuer, au moyen d'actes d'exécution, sur les questions visées au paragraphe 3, points a) et b).
5. Afin d'assurer l'application uniforme de l'annexe VIII, et compte tenu des avis scientifiques pertinents des comités scientifiques concernés, la Commission peut adopter des actes d'exécution dans la mesure nécessaire pour résoudre les problèmes liés à des différences d'interprétation et à l'application pratique.
6. Les actes d'exécution visés aux paragraphes 3, 4 et 5 du présent article sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
Section 2
Évaluation de la conformité
Article 48
Procédures d'évaluation de la conformité
1. Avant la mise sur le marché d'un dispositif, les fabricants en évaluent la conformité, conformément aux procédures d'évaluation de la conformité applicables, définies aux annexes IX à XI.
2 Avant la mise en service d'un dispositif qui n'est pas mis sur le marché, à l'exception des dispositifs fabriqués en interne conformément à l'article 5, paragraphe 5, les fabricants en évaluent la conformité, conformément aux procédures d'évaluation de la conformité applicables, définies aux annexes IX à XI.
3. Les fabricants de dispositifs de classe D, autres que les dispositifs devant faire l'objet d'une étude des performances, sont soumis à une évaluation de la conformité conformément aux chapitres I et II, sauf la section 5, et au chapitre III de l'annexe IX.
Outre les procédures visées au premier alinéa, le fabricant suit, pour les dispositifs d'autodiagnostic et les dispositifs de diagnostic près du patient, la procédure établie pour l'évaluation de la documentation technique à l'annexe IX, section 5.1.
En plus des procédures visées aux premier et deuxième alinéas, pour les diagnostics compagnons, l'organisme notifié consulte une autorité compétente désignée par les États membres conformément à la directive 2001/83/CE du Parlement européen et du Conseil ou l'EMA, le cas échéant, conformément à la procédure exposée à l'annexe IX, point 5.2.
4. Au lieu de la procédure d'évaluation de la conformité applicable au titre du paragraphe 3, les fabricants des dispositifs de classe D, autres que les dispositifs devant faire l'objet d'une étude des performances, peuvent opter pour une évaluation de la conformité au titre de l'annexe X, conjuguée à une évaluation de la conformité au titre de l'annexe XI.
Pour les diagnostiques compagnons, l'organisme notifié consulte, en particulier, une autorité compétente désignée par les États membres conformément à la directive 2001/83/CE ou l'EMA, le cas échéant, conformément à la procédure exposée à l'annexe X, section 3, point k).
5. En particulier et sans préjudice de toutes obligations au titre des autres procédures visées aux paragraphes 3 et 4, pour les dispositifs pour lesquels un ou plusieurs laboratoires de référence de l'UE ont été désignés conformément à l'article 100, l'organisme notifié qui réalise l'évaluation de la conformité demande à l'un de ceux-ci de vérifier, par des essais de laboratoire, les performances alléguées par le fabricant et la conformité du dispositif avec les spécifications communes applicables ou avec d'autres solutions retenues par le fabricant pour garantir un niveau de sécurité et de performances au moins équivalent, conformément à l'annexe IX, section 4.9, et à l'annexe X, section 3, point j). Les essais en laboratoire effectués par un laboratoire de référence de l'UE sont notamment axés sur la sensibilité analytique et la sensibilité diagnostique au moyen des matériaux de référence disponibles les plus performants.
6. Outre la procédure applicable au titre des paragraphes 3 et 4, lorsqu'il n'existe pas de spécification commune pour les dispositifs de classe D et qu'il s'agit en outre de la première certification pour ce type de dispositif, l'organisme notifié consulte le groupe d'experts visé à l'article 106 du règlement (UE) 2017/745 au sujet du rapport sur l'évaluation des performances présenté par le fabricant. À cette fin, l'organisme notifié transmet le rapport sur l'évaluation des performances présenté par le fabricant au groupe d'experts au plus tard cinq jours après l'avoir reçu du fabricant. Le groupe d'experts concerné communique, sous le contrôle de la Commission, conformément à l'annexe IX, section 4.9, ou à l'annexe X, section 3, point j), le cas échéant, ses points de vue à l'organisme notifié dans le délai au cours duquel le laboratoire de référence de l'UE doit rendre son avis scientifique
7. Les fabricants de dispositifs de classe C, autres que les dispositifs devant faire l'objet d'une étude des performances, sont soumis à une évaluation de la conformité conformément à l'annexe IX, chapitres I et III, et, en outre, à une évaluation de la documentation technique visée à la section 4 de ladite annexe pour au moins un dispositif représentatif par groupe générique de dispositifs.
En plus des procédures visées au premier alinéa, le fabricant suit, pour les dispositifs d'autodiagnostic et les dispositifs de diagnostic près du patient, la procédure relative à l'évaluation de la documentation technique établie à l'annexe IX, point 5.1.
En plus des procédures visées aux premier et deuxième alinéas, pour les diagnostics compagnons, l'organisme notifié suit, pour chaque dispositif, la procédure d'évaluation de la documentation technique établie à l'annexe IX, section 5.2, applique la procédure d'évaluation de la documentation technique établie à l'annexe IX, sections 4.1 à 4.8, et consulte une autorité compétente désignée par les États membres conformément à la directive 2001/83/CE ou l'EMA, le cas échéant, conformément à la procédure exposée à l'annexe IX, section 5.2.
8. Les fabricants des dispositifs de classe C, autres que les dispositifs devant faire l'objet d'une étude des performances, peuvent, au lieu d'une procédure d'évaluation de la conformité au titre du paragraphe 7, opter pour une évaluation de la conformité au titre de l'annexe X conjuguée à une évaluation de la conformité au titre de l'annexe XI, à l'exception de la section 5 de ladite annexe.
Pour les diagnostics compagnons, l'organisme notifié consulte, en particulier et pour chaque dispositif, une autorité compétente désignée par les États membres conformément à la directive 2001/83/CE ou l'EMA, le cas échéant, conformément à la procédure exposée à l'annexe X, section 3, point k).
9. Les fabricants de dispositifs de classe B, autres que les dispositifs devant faire l'objet d'une étude des performances, sont soumis à une procédure d'évaluation de la conformité conformément à l'annexe IX, chapitres I et III, et, en outre, à une évaluation de la documentation technique visée à la section 4 de ladite annexe pour au moins un dispositif représentatif par catégorie de dispositifs.
Outre les procédures visées au premier alinéa, le fabricant suit, pour les dispositifs d'autodiagnostic et les dispositifs de diagnostic près du patient, la procédure relative à l'évaluation de la documentation technique établie à l'annexe IX, section 6.1.
10. Les fabricants de dispositifs de classe A, autres que les dispositifs devant faire l'objet d'une étude des performances, attestent la conformité de leurs produits en établissant la déclaration de conformité UE visée à l'article 17, après avoir élaboré la documentation technique prévue aux annexes II et III.
Toutefois, si ces dispositifs sont mis sur le marché à l'état stérile, le fabricant applique les procédures prévues à l'annexe IX ou à l'annexe XI. L'intervention de l'organisme notifié se limite aux aspects liés à l'obtention, à la préservation et au maintien de cet état.
11. Les dispositifs devant faire l'objet d'une étude des performances sont soumis aux exigences énoncées aux articles 57 à 77.
12. L'État membre d'établissement de l'organisme notifié peut exiger que tout ou partie des documents, notamment la documentation technique et les rapports d'audit, d'évaluation et d'inspection, relatifs aux procédures visées aux paragraphes 1 à 10 soient mis à disposition dans une ou des langues officielles de l'Union définies par l'État membre en question. En l'absence d'une telle exigence, ces documents sont disponibles dans toute langue officielle de l'Union acceptée par l'organisme notifié.
13. La Commission peut, au moyen d'actes d'exécution, préciser les modalités et les aspects procéduraux en vue de l'application harmonisée des procédures d'évaluation de la conformité par les organismes notifiés concernant les points suivants:
a) |
la fréquence et la base d'échantillonnage pour l'évaluation d'un échantillon représentatif de la documentation technique, conformément à l'annexe IX, section 3.3, troisième alinéa, et section 3.5, pour les dispositifs de classe C; |
b) |
la fréquence minimale des audits sur place inopinés et des essais pratiqués sur les échantillons par les organismes notifiés conformément à l'annexe IX, section 3.4, compte tenu de la classe de risque et du type de dispositif; |
c) |
la fréquence des prélèvements d'échantillons de dispositifs fabriqués ou de lots de dispositifs de classe D devant être envoyés à un laboratoire de référence de l'UE désigné en vertu de l'article 100, conformément à l'annexe IX, section 4.12, et à l'annexe XI, section 5.1; ou |
d) |
les essais physiques, les essais en laboratoire et les autres essais devant être réalisés par les organismes notifiés dans le contexte des essais pratiqués sur les échantillons, de l'évaluation de la documentation technique et de l'examen de type, conformément à l'annexe IX, sections 3.4 et 4.3, et à l'annexe X, section 3, points f) et g). |
Les actes d'exécution visés au premier alinéa sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
Article 49
Intervention des organismes notifiés dans les procédures d'évaluation de la conformité
1. Lorsque la procédure d'évaluation de la conformité prévoit l'intervention d'un organisme notifié, le fabricant peut introduire une demande auprès de l'organisme notifié de son choix, à condition que l'organisme notifié choisi soit désigné pour les activités d'évaluation de la conformité liées aux types de dispositifs concernés. Le fabricant ne peut introduire une demande en parallèle auprès d'un autre organisme notifié pour la même procédure d'évaluation de la conformité.
2. L'organisme notifié concerné informe, via le système électronique visé à l'article 52, les autres organismes notifiés lorsqu'un fabricant retire sa demande avant que ledit organisme ne soit parvenu à une décision dans le cadre de l'évaluation de la conformité.
3. Lorsqu'ils introduisent une demande auprès d'un organisme notifié comme indiqué au paragraphe 1, les fabricants déclarent s'ils ont retiré une demande introduite auprès d'un autre organisme notifié avant que ledit organisme ne soit parvenu à une décision et communiquent des informations sur toute demande antérieure concernant la même évaluation de la conformité qui a été refusée par un autre organisme notifié.
4. L'organisme notifié peut exiger du fabricant toute information ou donnée nécessaire au bon déroulement de la procédure d'évaluation de la conformité retenue.
5. Les organismes notifiés et leur personnel accomplissent les activités d'évaluation de la conformité avec toute l'intégrité professionnelle et la compétence technique et scientifique requises dans le domaine concerné et ne sont soumis à aucune pression ni incitation, notamment d'ordre financier, susceptibles d'influencer leur jugement ou les résultats de leurs activités d'évaluation de la conformité, en particulier de la part de personnes ou de groupes de personnes ayant un intérêt dans ces résultats.
Article 50
Mécanisme de contrôle des évaluations de la conformité des dispositifs de classe D
1. Un organisme notifié informe l'autorité compétente des certificats qu'il a délivrés pour des dispositifs de classe D, à l'exception des demandes qui visent à compléter ou à renouveler des certificats. Cette notification est effectuée via le système électronique visé à l'article 52 et comprend la notice d'utilisation visée à l'annexe I, section 20.4, le résumé des caractéristiques de sécurité et des performances visé à l'article 29, le rapport d'évaluation de l'organisme notifié, et, le cas échéant, les essais en laboratoires effectués par le laboratoire de référence de l'UE et l'avis scientifique rendu par celui-ci, conformément à l'article 48, paragraphe 3, deuxième alinéa, et, le cas échéant, les points de vue exprimés, conformément à l'article 48, paragraphe 4, par les experts visés à l'article 106 du règlement (UE) 2017/745. Lorsque l'organisme notifié et les experts ont des points de vue différents, une justification exhaustive y figure également.
2. Une autorité compétente et, le cas échéant, la Commission peut, pour des motifs de préoccupation raisonnables, appliquer d'autres procédures conformément aux articles 40, 41, 42, 43 ou 89 et, si nécessaire, prendre des mesures appropriées conformément aux articles 90 et 92.
3. Le GCDM et, le cas échéant, la Commission, peut, pour des motifs de préoccupation raisonnables, demander un avis scientifique aux groupes d'experts en ce qui concerne la sécurité et les performances de tout dispositif.
Article 51
Certificats de conformité
1. Les certificats délivrés par les organismes notifiés conformément aux annexes IX, X et XI sont établis dans une langue officielle de l'Union déterminée par l'État membre d'établissement de l'organisme notifié ou, à défaut, dans une langue officielle de l'Union acceptée par l'organisme notifié. Le contenu minimal des certificats est établi à l'annexe XII.
2. Les certificats sont valables pendant la période indiquée sur ceux-ci, qui n'excède pas cinq ans. À la demande du fabricant, la durée de validité du certificat peut être prolongée d'une durée maximale de cinq ans à chaque fois, sur la base d'une nouvelle évaluation suivant les procédures d'évaluation de la conformité applicables. Tout document complémentaire à un certificat est valable aussi longtemps que l'est le certificat qu'il complète.
3. Les organismes notifiés peuvent imposer à certains groupes de patients ou d'utilisateurs des restrictions à la destination d'un dispositif ou exiger des fabricants qu'ils entreprennent des études spécifiques de SPAC conformément à l'annexe XIII, partie B.
4. Lorsqu'un organisme notifié constate que les exigences énoncées dans le présent règlement ne sont plus respectées par le fabricant, il suspend ou annule le certificat délivré ou l'assortit de restrictions, en tenant compte du principe de proportionnalité, sauf si le fabricant applique, en vue du respect de ces exigences, des mesures correctives appropriées dans le délai imparti à cet effet par l'organisme notifié. L'organisme notifié motive sa décision.
5. L'organisme notifié introduit dans le système électronique visé à l'article 52 les informations concernant les certificats délivrés et les modifications et documents complémentaires y afférents, ainsi que les certificats suspendus, rétablis, annulés ou refusés et les certificats assortis de restrictions. Ces informations sont mises à disposition du public.
6. La Commission est habilitée à adopter des actes délégués conformément à l'article 108 pour modifier, eu égard aux progrès techniques, le contenu minimal des certificats exposés à l'annexe XII.
Article 52
Système électronique relatif aux organismes notifiés et aux certificats de conformité
Aux fins du présent règlement, les informations ci-dessous sont collectées et traitées conformément à l'article 57 du règlement (UE) 2017/745 dans le système électronique établi conformément audit article:
a) |
la liste des filiales visée à l'article 33, paragraphe 2; |
b) |
la liste des experts visée à l'article 36, paragraphe 2; |
c) |
les informations concernant la notification visée à l'article 38, paragraphe 10, et les notifications modifiées visées à l'article 42, paragraphe 2; |
d) |
la liste des organismes notifiés visée à l'article 39, paragraphe 2; |
e) |
le résumé du rapport visé à l'article 40, paragraphe 12; |
f) |
les notifications relatives aux évaluations de la conformité et aux certificats visées à l'article 50, paragraphe 1; |
g) |
le retrait ou les refus de demandes de certificats visés à l'article 49, paragraphe 2, et à l'annexe VII, section 4.3; |
h) |
les informations concernant les certificats visées à l'article 51, paragraphe 5; |
i) |
le résumé des caractéristiques de sécurité et des performances visé à l'article 29. |
Article 53
Changement volontaire d'organisme notifié
1. Lorsqu'un fabricant résilie le contrat qui le lie à un organisme notifié et en conclut un nouveau avec un autre organisme notifié pour l'évaluation de la conformité d'un même dispositif, les modalités du changement d'organisme notifié sont clairement établies dans un accord entre le fabricant, le nouvel organisme notifié et, si possible, l'organisme notifié «sortant». Cet accord porte au moins sur les points suivants:
a) |
la date d'invalidation des certificats délivrés par l'organisme notifié sortant; |
b) |
la date jusqu'à laquelle le numéro d'identification de l'organisme notifié sortant peut figurer dans les informations fournies par le fabricant, y compris sur tout support publicitaire; |
c) |
les modalités de transfert des documents, y compris les questions de confidentialité et de droits de propriété; |
d) |
la date après laquelle le nouvel organisme notifié assume les tâches d'évaluation de la conformité de l'organisme notifié sortant; |
e) |
le dernier numéro de série ou numéro de lot dont l'organisme notifié sortant assume la responsabilité. |
2. L'organisme notifié sortant retire les certificats qu'il a délivrés pour le dispositif concerné à la date d'invalidation fixée.
Article 54
Dérogation aux procédures d'évaluation de la conformité
1. Par dérogation à l'article 48, toute autorité compétente peut, sur demande dûment justifiée, autoriser la mise sur le marché ou la mise en service, sur le territoire de l'État membre concerné, d'un dispositif donné pour lequel les procédures visées à l'article en question n'ont pas été appliquées mais dont l'utilisation est dans l'intérêt de la santé publique ou de la sécurité ou de la santé des patients.
2. L'État membre informe la Commission et les autres États membres de toute décision d'autorisation de mise sur le marché ou de mise en service d'un dispositif en application du paragraphe 1, dès lors que cette autorisation est accordée pour une utilisation concernant plus d'un patient.
3. Après avoir été informée comme le prévoit le paragraphe 2 du présent article, la Commission, dans des cas exceptionnels liés à la santé publique ou à la sécurité ou la santé des patients peut, au moyen d'actes d'exécution, étendre pour une durée limitée la validité d'une autorisation accordée par un État membre en application du paragraphe 1 du présent article au territoire de l'Union et définir les conditions de mise sur le marché ou de mise en service du dispositif concerné. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
Pour des raisons d'urgence impérieuses dûment justifiées liées à la santé et à la sécurité des personnes, la Commission adopte des actes d'exécution immédiatement applicables en conformité avec la procédure visée à l'article 107, paragraphe 4.
Article 55
Certificat de libre vente
1. À des fins d'exportation et à la demande d'un fabricant ou d'un mandataire, l'État membre dans lequel le fabricant ou le mandataire a son siège social délivre un certificat de libre vente attestant que le fabricant ou le mandataire, selon le cas, a son siège social sur son territoire et que le dispositif en question muni du marquage CE conformément au présent règlement peut être commercialisé dans l'Union. Le certificat de libre vente comporte L'IUD-ID de base du dispositif tel qu'il a été transmis à la base de données IUD en application de l'article 26. Lorsqu'un organisme notifié a délivré un certificat conformément à l'article 51, le certificat de libre vente comporte le numéro unique permettant d'identifier le certificat délivré par l'organisme notifié, conformément à l'annexe XII, chapitre II, section 3.
2. La Commission peut, au moyen d'actes d'exécution, établir un modèle pour les certificats de libre vente, en tenant compte des pratiques internationales relatives à l'utilisation de tels certificats. Ces actes d'exécution sont adoptés en conformité avec la procédure consultative visée à l'article 107, paragraphe 2.
CHAPITRE VI
PREUVE CLINIQUE, ÉVALUATION DES PERFORMANCES ET ÉTUDES DES PERFORMANCES
Article 56
Évaluation des performances et preuve clinique
1. La confirmation de la conformité aux exigences générales en matière de sécurité et de performances énoncées à l'annexe I, en particulier celles concernant les caractéristiques de performances visées à l'annexe I, chapitre I et section 9, dans des conditions normales d'utilisation d'un dispositif, ainsi que l'évaluation des interférences et réactions croisées et du caractère acceptable du rapport bénéfice/risque visé à l'annexe I, sections 1 et 8, sont fondées sur la validité scientifique et des données relatives aux performances cliniques et analytiques apportant une preuve clinique suffisante, y compris, le cas échéant, les données pertinentes visées à l'annexe III.
Le fabricant précise et justifie le niveau de preuve clinique nécessaire pour démontrer la conformité aux exigences générales pertinentes en matière de sécurité et de performances. Ce niveau de preuve clinique est approprié, eu égard aux caractéristiques du dispositif et à sa destination.
À cet effet, les fabricants planifient, réalisent et documentent une évaluation des performances conformément au présent article et à l'annexe XIII, partie A.
2. La preuve clinique valide la destination du dispositif, telle qu'elle est alléguée par le fabricant, et repose sur un processus continu d'évaluation des performances, selon un plan d'évaluation des performances.
3. Une évaluation des performances est effectuée selon une procédure définie et méthodologiquement fondée visant à démontrer ce qui suit, conformément au présent article et à l'annexe XIII, partie A:
a) |
la validité scientifique; |
b) |
les performances analytiques; |
c) |
les performances cliniques. |
Les données et conclusions issues de l'évaluation de ces éléments constituent la preuve clinique pour le dispositif. La preuve clinique est de nature à démontrer de manière scientifique, en tenant compte de l'état de l'art dans le domaine médical, que le ou les bénéfices cliniques attendus seront assurés et que le dispositif est sûr. La preuve clinique découlant de l'évaluation des performances donne l'assurance, scientifiquement valable, qu'il est satisfait, dans des conditions normales d'utilisation, aux exigences générales applicables en matière de sécurité et de performances énoncées à l'annexe I.
4. Les études des performances cliniques conformes à l'annexe XIII, partie A, section 2, sont réalisées sauf s'il est dûment justifié de s'en tenir à d'autres sources de données sur les performances cliniques.
5. Les données relatives à la validité scientifique, aux performances analytiques et aux performances cliniques, leur évaluation et la preuve clinique qui en découle sont documentées dans le rapport sur l'évaluation des performances visé à l'annexe XIII, partie A, section 1.3.2. Ce rapport fait partie de la documentation technique visée à l'annexe II relative au dispositif concerné.
6. L'évaluation des performances et la documentation y afférente sont actualisées tout au long du cycle de vie du dispositif concerné à l'aide des données obtenues par le fabricant à la suite de l'application de son plan de SPAC, conformément à l'annexe XIII, partie B, et au plan de surveillance après commercialisation visé à l'article 79.
Le rapport sur l'évaluation des performances des dispositifs des classes C et D est mis à jour selon les besoins, mais au moins annuellement en y ajoutant les données visées au premier alinéa. Le résumé des caractéristiques de sécurité et des performances visé à l'article 29, paragraphe 1, est mis à jour dès que possible, selon les besoins.
7. Si nécessaire afin d'assurer l'application uniforme de l'annexe XIII, la Commission peut, en tenant dûment compte des progrès techniques et scientifiques, adopter des actes d'exécution dans la mesure nécessaire pour résoudre les problèmes liés à des différences d'interprétation et à l'application pratique. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
Article 57
Exigences générales relatives aux études des performances
1. Le fabricant veille à ce que le dispositif devant faire l'objet d'une étude des performances soit, outre les aspects relatifs à l'étude des performances, conforme aux exigences générales en matière de sécurité et de performance énoncées à l'annexe I et, pour ce qui est desdits aspects, à ce que toutes les précautions aient été prises pour protéger la santé et la sécurité du patient, de l'utilisateur et d'autres personnes.
2. Le cas échéant, les études des performances sont réalisées dans des conditions similaires aux conditions normales d'utilisation du dispositif.
3. Les études des performances sont conçues et réalisées de manière à garantir la protection des droits, de la sécurité, de la dignité et du bien-être des personnes y participant, à faire prévaloir ces considérations sur toute autre et à garantir la validité scientifique, la fiabilité et la robustesse des données qu'elles génèrent.
Les études des performances, notamment les études utilisant des échantillons restants, sont réalisées conformément à la législation applicable en matière de protection des données.
Article 58
Exigences supplémentaires pour certaines études des performances
1. Toute étude des performances
a) |
dans le cadre de laquelle des échantillons sont obtenus par prélèvement chirurgical invasif aux seules fins de l'étude des performances; |
b) |
qui constitue une étude interventionnelle des performances cliniques au sens de l'article 2, point 46); ou |
c) |
dont la réalisation suppose des procédures invasives supplémentaires ou d'autres risques pour les participants à l'étude, |
non seulement respecte les exigences énoncées à l'article 57 et à l'annexe XIII, mais est conçue, autorisée, réalisée, documentée et notifiée conformément au présent article et aux articles 59 à 77 et à l'annexe XIV.
2. Les études des performances concernant des diagnostics compagnons sont soumises aux mêmes exigences que les études des performances visées au paragraphe 1. Cela ne s'applique pas aux études des performances concernant des diagnostics compagnons utilisant uniquement des échantillons restants. Ces études sont toutefois notifiées à l'autorité compétente.
3. Les études des performances font l'objet d'un examen scientifique et éthique. L'examen éthique est réalisé par un comité d'éthique conformément à la législation nationale. Les États membres veillent à ce que les procédures pour l'examen effectué par les comités d'éthique soient compatibles avec les procédures établies dans le présent règlement en ce qui concerne l'évaluation de la demande d'autorisation d'une étude des performances. Un profane au moins participe à l'examen éthique.
4. Lorsque le promoteur d'une étude des performances n'est pas établi dans l'Union, il veille à ce qu'une personne physique ou morale y soit établie en qualité de représentant légal. Ce représentant légal est chargé de garantir le respect des obligations incombant au promoteur au titre du présent règlement et est le destinataire de toutes les communications adressées au promoteur conformément au présent règlement. Toute communication avec le représentant légal vaut communication avec le promoteur.
Les États membres peuvent choisir de ne pas appliquer le premier alinéa aux études des performances devant être réalisées uniquement sur leur territoire ou sur leur territoire et sur le territoire d'un pays tiers, à condition qu'ils s'assurent que le promoteur établit au moins une personne de contact sur leur territoire pour l'étude des performances concernée, qui est le destinataire de toutes les communications adressées au promoteur conformément au présent règlement.
5. Une étude des performances telle que visée au paragraphe 1 ne peut être réalisée que si toutes les conditions suivantes sont remplies:
a) |
l'étude des performances fait l'objet d'une autorisation délivrée par le ou les États membres dans lesquels elle doit être réalisée, conformément au présent règlement, sauf dispositions contraires; |
b) |
un comité d'éthique, instauré conformément au droit national, n'a pas émis d'avis défavorable à propos de l'étude des performances, qui est valable pour l'ensemble de cet État membre en vertu de son droit national; |
c) |
le promoteur, ou son représentant légal ou une personne de contact au sens du paragraphe 4, est établi dans l'Union; |
d) |
les populations et participants vulnérables bénéficient d'une protection appropriée, conformément aux articles 59 à 64; |
e) |
les bénéfices attendus pour les participants ou la santé publique justifient les risques et inconvénients prévisibles et le respect de cette condition est contrôlé en permanence; |
f) |
le participant ou, s'il n'est pas en mesure de le faire, son représentant légal a donné son consentement éclairé conformément à l'article 59; |
g) |
le participant ou, s'il n'est pas en mesure de donner son consentement éclairé, son représentant légal a reçu les coordonnées d'une entité auprès de laquelle il peut recevoir de plus amples informations en cas de besoin; |
h) |
les droits du participant à l'intégrité physique et mentale, au respect de la vie privée et à la protection des données le concernant conformément à la directive 95/46/CE sont préservés; |
i) |
l'étude des performances a été conçue pour causer aussi peu de douleur, de désagrément et de peur que possible et pour réduire autant que possible tout autre risque prévisible pour les participants, et tant le seuil de risque que le degré d'angoisse sont définis expressément dans le plan d'étude des performances et contrôlés en permanence; |
j) |
les soins médicaux dispensés aux participants sont de la responsabilité d'un médecin dûment qualifié ou, le cas échéant, de toute autre personne habilitée par le droit national à dispenser les soins concernés aux patients dans des conditions d'étude des performances; |
k) |
aucune incitation indue, y compris de nature financière, n'est exercée sur le participant ou, le cas échéant, son représentant légal, pour qu'il participe à l'étude des performances; |
l) |
le cas échéant, des essais ont été réalisés en matière de sécurité biologique, correspondant aux connaissances scientifiques les plus récentes, ou tout autre essai jugé nécessaire compte tenu de la destination du dispositif; |
m) |
dans le cas d'études des performances cliniques, les performances analytiques ont été démontrées, compte tenu de l'état de l'art; |
n) |
dans le cas d'études interventionnelles des performances cliniques, les performances analytiques et la validité scientifique ont été démontrées, compte tenu de l'état de l'art. Lorsque, dans le cas de diagnostics compagnons, la validité scientifique n'est pas établie, la justification scientifique de l'utilisation du biomarqueur est démontrée; |
o) |
la sécurité technique du dispositif au regard de son utilisation a été démontrée, compte tenu de l'état de l'art et des dispositions en matière de sécurité sur le lieu de travail et de prévention des accidents; |
p) |
les exigences figurant à l'annexe XIV sont respectées. |
6. Tout participant ou, s'il n'est pas en mesure de donner son consentement éclairé, son représentant légal, peut, sans encourir de préjudice et sans devoir se justifier, se retirer de l'étude des performances à tout moment en révoquant son consentement éclairé. Sans préjudice de la directive 95/46/CE, le retrait du consentement éclairé n'a pas d'incidence sur les activités déjà menées ni sur l'utilisation des données obtenues sur la base du consentement éclairé avant que celui-ci ne soit retiré.
7. L'investigateur est une personne dont la profession donne droit, dans l'État membre concerné, à intervenir en tant qu'investigateur en raison des connaissances scientifiques et de l'expérience nécessaires dans le domaine des soins dispensés aux patients ou de la biologie médicale. Toute autre personne participant à la réalisation d'une étude des performances a le niveau d'études, la formation ou l'expérience appropriés dans la discipline médicale concernée et pour ce qui est de la méthode de recherche clinique pour accomplir les tâches qui lui incombent.
8. Le cas échéant, les installations dans lesquelles doit s'effectuer l'étude des performances faisant appel à des participants sont appropriées pour la réalisation de l'étude des performances et sont similaires à celles destinées à l'utilisation prévue du dispositif.
Article 59
Consentement éclairé
1. Le consentement éclairé est écrit, daté et signé par la personne qui effectue l'entretien visée au paragraphe 2, point c), et par le participant ou, si ce dernier n'est pas en mesure de donner son consentement éclairé, par son représentant légal après avoir été dûment informé conformément au paragraphe 2. Si le participant n'est pas en mesure d'écrire, son consentement peut être donné et documenté par d'autres moyens appropriés en présence d'au moins un témoin impartial. Dans ce cas, le témoin signe et date le document relatif au consentement éclairé. Le participant ou, s'il n'est pas en mesure de donner son consentement éclairé, son représentant légal se voit remettre une copie du document ou autre moyen de documentation, selon le cas, par lequel il a donné son consentement éclairé. Le consentement éclairé est documenté. Le participant ou son représentant légal dispose d'un temps de réflexion approprié pour réfléchir à sa décision de participer à l'étude des performances.
2. Les informations communiquées au participant ou, s'il n'est pas en mesure de donner son consentement éclairé, à son représentant légal pour obtenir son consentement éclairé:
a) |
permettent au participant ou à son représentant légal de comprendre:
|
||||||||
b) |
sont complètes, concises, claires, pertinentes et compréhensibles par l'intéressé ou son représentant légal; |
||||||||
c) |
sont fournies lors d'un entretien préalable avec un membre de l'équipe d'investigateurs qui est dûment qualifié en vertu du droit national; et |
||||||||
d) |
comprennent des informations sur le système d'indemnisation des dommages applicable, visé à l'article 65; |
||||||||
e) |
comprennent le numéro d'identification unique, visé à l'article 66, paragraphe 1, valable dans l'ensemble de l'Union attribué à l'étude des performances et des informations sur la disponibilité des résultats de l'étude des performances, conformément au paragraphe 6 du présent article. |
3. Les informations visées au paragraphe 2 sont préparées par écrit et mises à la disposition du participant ou, s'il n'est pas en mesure de donner son consentement éclairé, de son représentant légal.
4. Lors de l'entretien visée au paragraphe 2, point c), une attention particulière est apportée aux besoins d'information des groupes spécifiques de patients et des participants individuels, ainsi qu'aux méthodes employées pour transmettre les informations.
5. Lors de l'entretien visée au paragraphe 2, point c), il est vérifié que le participant a compris les informations.
6. Le participant est informé qu'un rapport sur l'étude des performances et un résumé présenté en des termes compréhensibles pour l'utilisateur auquel le dispositif est destiné seront mis à disposition en application de l'article 73, paragraphe 3, dans le système électronique sur les études de performances visé à l'article 69, quel que soit le résultat de l'étude des performances, et est informé, dans la mesure du possible, au moment de leur mise à disposition.
7. Le présent règlement s'applique sans préjudice de toute disposition du droit national prévoyant que, en plus du consentement éclairé donné par le représentant légal, un mineur en mesure de se forger une opinion et d'évaluer les informations qui lui sont données donne également son accord pour participer à une étude des performances.
Article 60
Études des performances sur des participants incapables
1. Dans le cas de participants incapables qui n'ont pas donné leur consentement éclairé ou qui n'ont pas refusé de le faire avant la survenance de leur incapacité, une étude des performances ne peut être réalisée que si, outre les conditions prévues à l'article 58, paragraphe 5, toutes les conditions suivantes sont remplies:
a) |
le consentement éclairé de leur représentant légal a été obtenu; |
||||
b) |
le participant incapable a reçu les informations visées à l'article 59, paragraphe 2, d'une manière adaptée au regard de leur capacité à les comprendre; |
||||
c) |
le souhait explicite d'un participant incapable, en mesure de se forger une opinion et d'évaluer les informations visées à l'article 59, paragraphe 2, de refuser de participer à l'étude des performances ou de s'en retirer à tout moment, est respecté par l'investigateur; |
||||
d) |
aucune incitation et aucun avantage financier ne sont offerts aux participants ou à leur représentant légal hormis une compensation pour les frais et pertes de revenus directement liés à la participation à l'étude des performances; |
||||
e) |
l'étude des performances est essentielle en ce qui concerne les participants incapables et des données d'une validité comparable ne peuvent être obtenues lors d'études des performances sur des personnes capables de donner leur consentement éclairé ou par d'autres méthodes de recherche; |
||||
f) |
l'étude des performances se rapporte directement à une affection dont est atteint le participant; |
||||
g) |
il existe des raisons scientifiques de penser que la participation à l'étude des performances produira:
|
2. Dans la mesure du possible, le participant prend part à la procédure de consentement éclairé.
3. Le paragraphe 1, point g) ii), s'applique sans préjudice de règles nationales plus strictes interdisant la réalisation de ces études des performances sur des participants incapables lorsqu'il n'y a aucune raison scientifique de penser que la participation à l'étude des performances produira un bénéfice direct pour le participant supérieur aux risques et aux contraintes en jeu.
Article 61
Études des performances sur des mineurs
1. Une étude des performances ne peut être réalisée sur des mineurs que si, outre les conditions prévues à l'article 58, paragraphe 5, toutes les conditions suivantes sont remplies:
a) |
le consentement éclairé de leur représentant légal a été obtenu; |
||||
b) |
les mineurs ont reçu, de la part des investigateurs ou de membres de l'équipe d'investigateurs formés ou rompus au travail avec des enfants, les informations visées à l'article 59, paragraphe 2, d'une façon adaptée à leur âge et à leur maturité mentale; |
||||
c) |
le souhait explicite d'un participant mineur en mesure de se forger une opinion et d'évaluer les informations visées à l'article 59, paragraphe 2, de refuser de participer à l'étude des performances ou de s'en retirer à tout moment, est respecté par l'investigateur; |
||||
d) |
aucune incitation et aucun avantage financier ne sont offerts aux participants ou à leurs représentants désignés légalement hormis une compensation pour les frais et pertes de revenus directement liés à la participation à l'étude des performances; |
||||
e) |
l'étude des performances est destinée à étudier des traitements pour une affection qui ne touche que les mineurs ou l'étude des performances est essentielle en ce qui concerne les mineurs pour valider les données obtenues lors d'études des performances sur des personnes capables de donner leur consentement éclairé ou par d'autres méthodes de recherche; |
||||
f) |
l'étude des performances se rapporte directement à une affection touchant le mineur concerné ou est d'une nature telle qu'elle ne peut être réalisée que sur des mineurs; |
||||
g) |
il existe des raisons scientifiques de penser que la participation à l'étude des performances produira:
|
||||
h) |
le mineur participe à la procédure de consentement éclairé d'une façon adaptée à son âge et à sa maturité mentale; |
||||
i) |
si, au cours d'une étude des performances, le mineur atteint l'âge auquel il est légalement habilité à donner son consentement éclairé tel qu'il est défini par le droit national, son consentement éclairé est obtenu avant que ce participant ne puisse poursuivre sa participation à l'étude des performances. |
2. Le paragraphe 1, point g) ii), s'applique sans préjudice de règles nationales plus strictes interdisant la réalisation de ces études des performances sur des mineurs lorsqu'il n'y a aucune raison scientifique de penser que la participation à l'étude des performances produira un bénéfice direct pour le participant supérieur aux risques et aux contraintes en jeu.
Article 62
Études des performances sur des femmes enceintes ou allaitantes
Une étude des performances ne peut être réalisée sur des femmes enceintes ou allaitantes que si, outre les conditions prévues à l'article 58, paragraphe 5, toutes les conditions suivantes sont remplies:
a) |
l'étude des performances a le potentiel de produire un bénéfice direct pour la femme enceinte ou allaitante concernée ou pour son embryon, son fœtus ou l'enfant après sa naissance, supérieur aux risques et aux contraintes en jeu; |
||||||
b) |
si l'étude des performances ne produit pas de bénéfice direct pour la femme enceinte ou allaitante concernée ou pour son embryon, son fœtus ou l'enfant après sa naissance, elle ne peut avoir lieu que si:
|
||||||
c) |
lorsque des recherches sont menées sur des femmes allaitantes, il convient de veiller en particulier à éviter tout effet indésirable sur la santé de l'enfant; |
||||||
d) |
aucune incitation et aucun avantage financier ne sont offerts aux participantes, hormis une compensation pour les frais et pertes de revenus directement liés à la participation à l'étude des performances. |
Article 63
Mesures nationales supplémentaires
Les États membres peuvent maintenir des mesures supplémentaires concernant les personnes qui accomplissent un service militaire obligatoire, les personnes privées de liberté, les personnes qui, en raison d'une décision de justice, ne peuvent participer à des études des performances ou les personnes placées dans des établissements d'hébergement et de soins.
Article 64
Études des performances en situation d'urgence
1. Par dérogation à l'article 58, paragraphe 5, point f), à l'article 60, paragraphe 1, points a) et b), et à l'article 61, paragraphe 1, points a) et b), le consentement éclairé pour participer à une étude des performances peut être obtenu et des informations sur l'étude des performances peuvent être communiquées après la décision d'inclure le participant dans l'étude des performances à condition que cette décision soit prise au moment de la première intervention sur le participant, conformément au plan d'étude des performances cliniques de cette étude des performances, et que toutes les conditions suivantes soient remplies:
a) |
en raison de l'urgence de la situation, causée par une affection soudaine qui met sa vie en danger ou par toute autre affection grave et soudaine, le participant n'est pas en mesure de donner son consentement éclairé préalable et de recevoir des informations préalables sur l'étude des performances; |
b) |
des raisons scientifiques donnent à penser que la participation à l'étude des performances sera à même de produire un bénéfice direct pertinent sur le plan clinique pour le participant, entraînant une amélioration mesurable sur le plan médical, susceptible d'alléger les souffrances et/ou d'améliorer la santé du participant ou le diagnostic de son affection; |
c) |
il n'est pas possible, dans l'intervalle thérapeutique, de fournir toutes les informations préalables au représentant légal du participant et d'obtenir son consentement éclairé préalable; |
d) |
l'investigateur certifie qu'il n'a pas connaissance d'objections à la participation à l'étude des performances préalablement exprimées par le participant; |
e) |
l'étude des performances se rapporte directement à l'affection du participant en raison de laquelle il n'est pas possible, dans l'intervalle thérapeutique, d'obtenir le consentement éclairé préalable du participant ou de son représentant légal et de communiquer des informations préalables, et l'étude des performances est d'une nature telle qu'elle ne peut avoir lieu qu'en situation d'urgence; |
f) |
l'étude des performances comporte un risque minimal et impose une contrainte minimale pour le participant par rapport au traitement standard de l'affection dont il est atteint. |
2. À la suite d'une intervention conformément au paragraphe 1 du présent article, le consentement éclairé conformément à l'article 59 est sollicité pour poursuivre la participation de l'intéressé à l'étude des performances et les informations sur l'étude des performances sont communiquées conformément aux exigences suivantes:
a) |
en ce qui concerne les participants incapables et les mineurs, l'investigateur sollicite sans retard injustifié le consentement éclairé de leurs représentants désignés légalement et les informations visées à l'article 59, paragraphe 2, sont communiquées dans les plus brefs délais au participant et à son représentant légal; |
b) |
en ce qui concerne les autres participants, l'investigateur sollicite sans retard injustifié le consentement éclairé du participant ou de son représentant légal, selon ce qui peut être le plus rapide, et les informations visées à l'article 59, paragraphe 2, sont communiquées dans les plus brefs délais au participant ou à son représentant légal, selon le cas. |
Aux fins du point b), si le consentement éclairé a été obtenu auprès du représentant légal, il est obtenu, pour la poursuite de la participation à l'étude des performances, auprès du participant dès que celui-ci est en mesure de donner un consentement éclairé.
3. Si le participant ou, le cas échéant, son représentant légal ne donne pas son consentement, il est informé de son droit de s'opposer à l'utilisation des données recueillies dans le cadre de l'étude des performances.
Article 65
Compensation de dommages
1. Les États membres veillent à ce que des systèmes de compensation de tout dommage que subirait un participant en raison de sa participation à une étude des performances conduite sur leur territoire soient en place sous la forme d'une assurance, d'une garantie ou de dispositions similaires, qui sont équivalentes pour ce qui est de leur finalité et adaptées à la nature et à l'ampleur du risque.
2. Le promoteur et l'investigateur ont recours au système visé au paragraphe 1 sous la forme appropriée pour l'État membre dans lequel l'étude des performances est conduite.
Article 66
Demande relative aux études des performances
1. Le promoteur d'une étude des performances visée à l'article 58, paragraphes 1 et 2, introduit et soumet auprès de l'État membre ou des États membres dans lesquels l'étude des performances doit être réalisée (ci-après dénommé «État membre concerné» aux fins du présent article), une demande accompagnée de la documentation visée à l'annexe XIII, sections 2 et 3, et à l'annexe XIV.
La demande est soumise via le système électronique visé à l'article 69 qui génère, pour cette étude des performances, un numéro d'identification unique valable dans l'ensemble de l'Union qui est utilisé pour toute communication ayant trait à cette étude des performances. Dans un délai de dix jours suivant la réception de la demande, l'État membre concerné indique également au promoteur si l'étude des performances relève du champ d'application du présent règlement et si le dossier de demande est complet conformément à l'annexe XIV, chapitre I.
2. Dans un délai d'une semaine suivant tout changement relatif à la documentation visée à l'annexe XIV, chapitre I, le promoteur met à jour les données correspondantes dans le système électronique visé à l'article 69 et rend ce changement relatif à la documentation clairement identifiable. L'État membre concerné est informé de la mise à jour via ce système électronique.
3. Lorsque l'État membre concerné estime que l'étude des performances pour laquelle une demande a été introduite ne relève pas du présent règlement ou que la demande est incomplète, il en informe le promoteur, qui dispose d'un délai maximal de dix jours pour formuler des observations ou compléter la demande via le système électronique visé à l'article 69. L'État membre concerné peut, le cas échéant, prolonger ce délai de vingt jours au maximum.
Lorsque le promoteur ne formule pas d'observations ni ne complète la demande dans le délai visé au premier alinéa, la demande est réputée caduque. Lorsque le promoteur estime que la demande relève du présent règlement et/ou qu'elle est complète mais que l'État membre concerné n'est pas de cet avis, la demande est considérée comme rejetée. L'État membre concerné prévoit une procédure de recours pour un tel refus.
L'État membre concerné indique au promoteur, dans un délai de cinq jours suivant la réception des observations ou des informations complémentaires demandées, si l'étude des performances est réputée relever du présent règlement et si la demande est complète.
4. L'État membre concerné peut également prolonger le délai visé aux paragraphes 1 et 3 de cinq jours supplémentaires.
5. Aux fins du présent chapitre, la date à laquelle le promoteur est informé conformément au paragraphe 1 ou 3 correspond à la date de validation de la demande. Lorsque le promoteur n'est pas informé, la date de validation correspond au dernier jour des délais visés respectivement aux paragraphes 1, 3 et 4.
6. Pendant la période au cours de laquelle la demande est évaluée, l'État membre peut demander des informations complémentaires au promoteur. Le délai visé au paragraphe 7, point b), cesse de courir entre la date de la première demande et la réception des informations complémentaires.
7. Le promoteur peut débuter l'étude des performances:
a) |
dans le cas d'études des performances réalisées en vertu de l'article 58, paragraphe 1, point a), et lorsque le prélèvement d'échantillons ne présente pas un risque clinique majeur pour le participant à l'étude, sauf dispositions contraires du droit national: immédiatement après la date de validation de la demande visée au paragraphe 5 du présent article, pour autant qu'un comité d'éthique dans l'État membre concerné n'ait pas émis d'avis défavorable en ce qui concerne l'étude des performances, valable pour l'ensemble de cet État membre conformément à son droit national; |
b) |
dans le cas d'études des performances réalisées en vertu de l'article 58, paragraphe 1, points b) et c), et de l'article 58, paragraphe 2, ou d'études des performances autres que celles visées au point a) du présent paragraphe: dès que l'État membre concerné a notifié son autorisation au promoteur et pour autant qu'un comité d'éthique dans l'État membre concerné n'ait pas émis d'avis défavorable à l'égard de l'étude des performances, qui est valable pour l'ensemble de cet État membre conformément à son droit national. L'État membre notifie l'autorisation au promoteur dans un délai de quarante-cinq jours suivant la date de validation de la demande visée au paragraphe 45. L'État membre peut prolonger ce délai de vingt jours supplémentaires aux fins de la consultation d'experts. |
8. La Commission est habilitée à adopter des actes délégués conformément à l'article 108 pour modifier, à la lumière du progrès technique et de l'évolution globale de la réglementation, les exigences énoncées à l'annexe XIV, chapitre I.
9. Afin d'assurer l'application uniforme des exigences énoncées à l'annexe XIV, chapitre I, la Commission peut adopter des actes d'exécution, dans la mesure nécessaire pour résoudre les problèmes liés à des différences d'interprétation et à l'application pratique. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
Article 67
Évaluation par les États membres
1. Les États membres veillent à ce que les personnes chargées de valider et d'évaluer la demande, ou de statuer sur celle-ci, soient libres de conflits d'intérêts, soient indépendantes du promoteur, des investigateurs et des personnes physiques ou morales finançant l'étude des performances, et ne soient l'objet d'aucune autre contrainte.
2. Les États membres veillent à ce que l'évaluation soit menée conjointement par un nombre raisonnable de personnes possédant collectivement les qualifications et l'expérience nécessaires.
3. Les États membres évaluent si l'étude des performances est conçue de telle manière que les risques résiduels potentiels pour les participants ou des tiers, après minimisation des risques, sont justifiés au regard des bénéfices cliniques escomptés. Tout en tenant compte des spécifications communes ou des normes harmonisées applicables, ils examinent en particulier:
a) |
s'il a été démontré que le ou les dispositifs devant faire l'objet d'une étude des performances respectent les exigences générales applicables en matière de sécurité et de performances, sauf pour ce qui est des aspects relevant de l'étude des performances, et si, en ce qui concerne ces aspects, toutes les précautions ont été prises pour protéger la santé et la sécurité des participants. Il s'agit notamment, dans le cas d'études des performances, de l'évaluation des performances analytiques et, dans le cas d'études interventionnelles des performances cliniques, de l'évaluation des performances analytiques, des performances cliniques et de la validité scientifique, compte tenu de l'état de l'art; |
b) |
si les solutions retenues par le promoteur pour minimiser les risques sont décrites dans les normes harmonisées et, dans les cas où le promoteur n'applique pas de normes harmonisées, si les solutions pour minimiser les risques assurent un niveau de protection équivalent à celui assuré par les normes harmonisées; |
c) |
si les mesures prévues pour assurer l'installation, la mise en service et la maintenance en toute sécurité du dispositif en vue de l'étude des performances sont adéquates; |
d) |
la fiabilité et la robustesse des données issues de l'étude des performances, au vu des modalités statistiques, de la conception de l'étude des performances et des aspects méthodologiques, y compris la taille de l'échantillon, le dispositif comparateur et les critères d'évaluation; |
e) |
si les exigences figurant à l'annexe XIV sont respectées. |
4. Les États membres refusent l'autorisation de l'étude des performances:
a) |
si le dossier de demande introduit en application de l'article 66, paragraphe 3, demeure incomplète; |
b) |
si le dispositif ou les documents fournis, en particulier le plan d'étude des performances et la brochure pour l'investigateur, ne correspondent pas à l'état des connaissances scientifiques et si l'étude des performances, notamment, n'est pas adaptée pour apporter la preuve de la sécurité ou des caractéristiques de performance du dispositif ou des bénéfices qu'il présente pour les participants ou les patients; |
c) |
si les exigences de l'article 58 ne sont pas respectées; ou |
d) |
si toute évaluation effectuée en vertu du paragraphe 3 est négative. |
Les États membres prévoient une procédure de recours en ce qui concerne un refus en application du premier alinéa.
Article 68
Réalisation d'une étude des performances
1. Le promoteur et l'investigateur veillent à ce que l'étude des performances soit réalisée conformément au plan d'étude des performances qui a été approuvé.
2. Afin de vérifier que les droits, la sécurité et le bien-être des participants sont protégés, que les données notifiées sont fiables et robustes, et que la réalisation de l'étude des performances est conforme aux exigences du présent règlement, le promoteur assure un suivi approprié de la réalisation de l'étude des performances. La portée et la nature du suivi sont définies par le promoteur sur la base d'une évaluation qui tient compte de l'ensemble des caractéristiques de l'étude des performances, y compris des suivantes:
a) |
l'objectif et la méthode de l'étude des performances; et |
b) |
le degré de déviation de l'intervention par rapport à la pratique clinique normale. |
3. Toutes les informations relatives aux études des performances sont enregistrées, traitées, gérées et archivées par le promoteur ou l'investigateur, selon le cas, de manière à pouvoir être notifiées, interprétées et vérifiées avec précision dans le respect de la confidentialité des informations et des données à caractère personnel relatives aux participants, conformément au droit applicable en matière de protection des données à caractère personnel.
4. Des mesures techniques et organisationnelles appropriées sont mises en œuvre afin que les informations et les données à caractère personnel traitées ne puissent pas être consultées, communiquées, diffusées, modifiées sans autorisation ou de manière illicite ou encore détruites ou perdues de façon accidentelle, en particulier lorsque le traitement suppose leur transmission par l'intermédiaire d'un réseau.
5. Les États membres inspectent au niveau approprié le ou les sites d'étude des performances afin de vérifier que l'étude des performances est réalisée dans le respect des exigences du présent règlement et du plan d'étude des performances qui a été approuvé.
6. Le promoteur établit une procédure pour les situations d'urgence qui permet l'identification immédiate et, si nécessaire, le rappel immédiat des dispositifs utilisés dans le cadre de l'étude.
Article 69
Système électronique relatif aux études des performances
1. En collaboration avec les États membres, la Commission met en place, gère et tient à jour un système électronique:
a) |
pour la création des numéros d'identification uniques des études des performances visés à l'article 66, paragraphe 1; |
b) |
pour servir de point d'entrée pour l'introduction de toutes les demandes ou notifications relatives à des études des performances visées aux articles 66, 70, 71 et 74 et pour toute autre communication ou tout autre traitement de données dans ce cadre; |
c) |
pour l'échange d'informations relatives aux études des performances conformément au présent règlement entre les États membres et entre ceux-ci et la Commission, y compris l'échange d'informations visé aux articles 72 et 74; |
d) |
pour les informations qui doivent être communiquées par le promoteur conformément à l'article 73, y compris le rapport sur l'étude des performances et son résumé, comme prévu au paragraphe 5 dudit article; |
e) |
pour la notification d'événements indésirables graves et de défectuosités de dispositifs, ainsi que pour des actualisations y afférents, visés à l'article 76. |
2. Dans le contexte de la mise en place du système électronique visé au paragraphe 1 du présent article, la Commission veille à l'interopérabilité de celui-ci avec la base de données de l'Union sur les essais cliniques de médicaments à usage humain établie en application de l'article 81 du règlement (UE) no 536/2014 du Parlement européen et du Conseil en ce qui concerne les études des performances des diagnostics compagnons.
3. Les informations visées au paragraphe 1, point c), ne sont accessibles qu'aux États membres et à la Commission. Les informations visées aux autres points de ce paragraphe sont accessibles pour le public, sauf s'il est justifié d'en préserver la confidentialité en tout ou partie pour l'un des motifs suivants:
a) |
la protection des données à caractère personnel conformément au règlement (CE) no 45/2001; |
b) |
la protection d'informations confidentielles de nature commerciale, spécialement dans la brochure pour l'investigateur, notamment par la prise en compte du statut de l'évaluation de la conformité pour le dispositif, à moins qu'un intérêt public supérieur ne justifie la divulgation des informations en question; |
c) |
la surveillance effective de la réalisation de l'étude des performances par le ou les États membres concernés. |
4. Aucune donnée à caractère personnel sur les participants n'est mise à la disposition du public.
5. L'interface utilisateur du système électronique visé au paragraphe 1 est disponible dans toutes les langues officielles de l'Union.
Article 70
Études des performances concernant les dispositifs munis du marquage CE
1. Lorsqu'une étude des performances doit être réalisée afin d'approfondir l'évaluation d'un dispositif qui est déjà muni du marquage CE, dans les limites de sa destination prévue, en vertu de l'article 18, paragraphe 1, (ci-après dénommée «étude SPAC») et lorsque l'étude performances impliquerait de soumettre les participations à des procédures additionnelles à celles déjà menées dans des conditions d'utilisation normale du dispositif et que ces procédures supplémentaires sont invasives ou lourdes, le promoteur en informe les États membres concernés au moins trente jours avant que cette étude ne commence via le système électronique visé à l'article 69. Le promoteur y joint la documentation visée à l'annexe XIII, partie A, section 2, et à l'annexe XIV. L'article 58, paragraphe 5, points b) à l) et point p), les articles 71, 72 et 73, l'article 76, paragraphes 5 et 6, et les dispositions pertinentes des annexes XIII et XIV s'appliquent à ces études SPAC.
2. Lorsqu'une étude des performances doit être réalisée afin d'évaluer, en dehors des limites de sa destination prévue, un dispositif déjà muni du marquage CE en vertu de l'article 18, paragraphe 1, les articles 58 à 77 s'appliquent.
Article 71
Modifications substantielles d'études des performances
1. Lorsqu'un promoteur a l'intention d'apporter à une étude des performances des modifications susceptibles d'avoir une incidence substantielle sur la sécurité, la santé ou les droits des participants, ou sur la robustesse ou la fiabilité des données issues de l'étude, il informe, dans un délai d'une semaine, via le système électronique visé à l'article 69, le ou les États membres dans lesquels l'étude des performances est ou doit être réalisée, des raisons et de la nature de ces modifications. Le promoteur y joint une version actualisée de la documentation pertinente visée à l'annexe XIV. Les modifications apportées dans cette documentation sont clairement visibles.
2. L'État membre évalue toute modification substantielle apportée à l'étude des performances conformément à la procédure prévue à l'article 67.
3. Le promoteur peut appliquer les modifications visées au paragraphe 1 au plus tôt trente-huit jours après la notification visée audit paragraphe 1, sauf si:
a) |
l'État membre dans lequel l'étude des performances est ou doit être réalisée a informé le promoteur de son refus sur la base des motifs visés à l'article 67, paragraphe 4, ou pour des raisons liées à la santé publique, à la sécurité ou la santé des participants et des utilisateurs, ou à l'ordre public; ou |
b) |
un comité d'éthique dudit État membre a émis un avis défavorable en rapport avec la modification substantielle apportée à l'étude des performances qui, conformément au droit national, est valable pour l'ensemble dudit État membre. |
4. Le ou les États membres concernés peuvent également prolonger le délai visé au paragraphe 3 de sept jours supplémentaires aux fins de la consultation d'experts.
Article 72
Mesures correctives à prendre par les États membres et échange d'informations entre les États membres concernant les études des performances
1. Lorsque l'État membre dans lequel une étude des performances est ou doit être réalisée a des raisons de considérer que les exigences énoncées dans le présent règlement ne sont pas respectées, il peut prendre au moins les mesures suivantes sur son territoire:
a) |
révoquer l'autorisation de l'étude des performances; |
b) |
suspendre ou mettre fin à l'étude des performances; |
c) |
demander au promoteur de modifier tout aspect de l'étude des performances. |
2. Avant de prendre les mesures visées au paragraphe 1, l'État membre concerné demande l'avis du promoteur ou de l'investigateur ou des deux, sauf lorsqu'une action immédiate s'impose. Cet avis lui est transmis dans un délai de sept jours.
3. Lorsqu'un État membre a pris une mesure visée au paragraphe 1 du présent article ou a refusé une étude des performances, ou a été informé par le promoteur que celui-ci a mis fin à l'étude des performances avant son terme pour des raisons de sécurité, cet État membre communique la décision correspondante et les motifs y afférents à tous les États membres et à la Commission via le système électronique visé à l'article 69.
4. Lorsque le promoteur retire une demande avant qu'un État membre n'ait arrêté une décision, cette information est mise à la disposition de tous les États membres et de la Commission via le système électronique visé à l'article 69.
Article 73
Information par le promoteur à la fin d'une étude des performances ou en cas d'interruption temporaire ou d'arrêt anticipé
1. Lorsque le promoteur interrompt temporairement une étude des performances ou met fin à une étude des performances de manière anticipée, il en informe, dans un délai de quinze jours, via le système électronique visé à l'article 69, les États membres dans lesquels cette étude des performances a été temporairement interrompue ou arrêtée de manière anticipée. Lorsque le promoteur interrompt temporairement l'étude des performances ou y met fin de manière anticipée pour des raisons de sécurité, il en informe, dans un délai de vingt-quatre heures, tous les États membres dans lesquels cette étude des performances est en cours.
2. Une étude des performances est réputée prendre fin avec la dernière visite du dernier participant, à moins que le plan d'étude des performances ne prévoie qu'elle se termine à un autre moment.
3. Le promoteur notifie à chaque État membre dans lequel une étude des performances était en cours la fin de ladite étude des performances dans l'État membre en question. Cette notification est effectuée dans un délai de quinze jours suivant la fin de l'étude des performances concernant ledit État membre.
4. Lorsqu'une étude des performances est réalisée dans plus d'un État membre, le promoteur informe tous les États membres dans lesquels cette étude était en cours de la fin de celle-ci dans l'ensemble des États membres. Cette notification est effectuée dans un délai de quinze jours suivant la fin de l'étude des performances.
5. Quel que soit le résultat de l'étude des performances, dans l'année suivant la fin de l'étude des performances ou dans un délai de trois mois suivant l'arrêt anticipé ou de l'interruption temporaire, le promoteur transmet aux États membres dans lesquels l'étude des performances était en cours, le rapport sur l'étude des performances visé à l'annexe XIII, partie A, section 2.3.3.
Le rapport sur l'étude des performances est accompagné d'un résumé rédigé en des termes aisément compréhensibles par l'utilisateur auquel le dispositif est destiné. Le rapport et le résumé sont transmis par le promoteur via le système électronique visé à l'article 69.
Lorsque, pour des raisons scientifiques, ce rapport sur l'étude des performances ne peut être transmis dans un délai d'un an après la fin de l'étude, il l'est dès qu'il est disponible. Dans ce cas, le plan d'étude des performances cliniques visé à l'annexe XIII, partie A, section 2.3.2, précise la date à laquelle les résultats de l'étude des performances seront disponibles, accompagnée d'une justification à cet égard.
6. La Commission établit des lignes directrices concernant le contenu et la structure du résumé du rapport sur l'étude des performances.
En outre, la Commission peut établir des lignes directrices concernant le format et les modalités de partage des données brutes pour les cas où le promoteur décide librement de partager de telles données. Ces lignes directrices peuvent s'appuyer, en les adaptant, dans la mesure du possible, sur des lignes directrices existantes en matière de partage de données brutes dans le cadre des études des performances.
7. Le résumé et le rapport sur l'étude des performances visés au paragraphe 5 du présent article deviennent accessibles pour le public via le système électronique visé à l'article 69, au plus tard lorsque le dispositif est enregistré conformément à l'article 26 et avant qu'il soit mis sur le marché. En cas d'arrêt anticipé ou d'interruption temporaire, le résumé et le rapport deviennent accessible pour le public immédiatement après leur transmission.
Si le dispositif n'est pas enregistré conformément à l'article 26 dans un délai d'un an après que le résumé et le rapport sur l'étude des performances ont été introduits dans le système électronique conformément au paragraphe 5 du présent article, ceux-ci deviennent accessibles pour le public à ce moment-là.
Article 74
Procédure d'évaluation coordonnée concernant les études des performances
1. Via le système électronique visé à l'article 69, le promoteur d'une étude des performances devant être réalisée dans plus d'un État membre peut, aux fins de l'article 66, introduire une demande unique, transmise dès réception par voie électronique à tous les États membres dans lesquels cette étude doit être réalisée.
2. Dans la demande unique visée au paragraphe 1, le promoteur propose l'un des États membres dans lesquels l'étude des performances doit être réalisée comme État membre coordonnateur. Dans un délai de six jours suivant l'introduction de la demande, les États membres dans lesquels l'étude des performances doit être réalisée s'entendent sur celui d'entre eux qui fera fonction d'État membre coordonnateur. S'ils ne s'entendent pas sur un État membre coordonnateur, c'est à l'État membre proposé par le promoteur qu'échoit la fonction.
3. Sous la direction de l'État membre coordonnateur visé au paragraphe 2, les États membres concernés coordonnent leur évaluation de la demande, notamment de la documentation visée à l'annexe XIV, chapitre I.
Cependant, le caractère complet de la documentation visée à l'annexe XIV, chapitre I, sections 1.13, 4.2, 4.3 et 4.4, et à l'annexe XIII, partie A, section 2.3.2, point c), est évalué séparément par chacun des États membres concernés conformément à l'article 66, paragraphes 1 à 5.
4. En ce qui concerne la documentation autre que celle visée au paragraphe 3, deuxième alinéa, l'État membre coordonnateur:
a) |
notifie au promoteur, dans un délai de six jours suivant la réception de la demande unique, qu'il est l'État membre coordonnateur (date de notification); |
b) |
prend en compte, aux fins de la validation de la demande, toute observation formulée par un État membre concerné dans un délai de sept jours suivant la date de notification; |
c) |
dans un délai de dix jours suivant la date de notification, évalue si l'étude des performances relève du présent règlement et si la demande est complète et en informe le promoteur en conséquence. L'article 66, paragraphes 1 et 3 à 5, s'applique à l'État membre coordonnateur pour ce qui est de cette évaluation; |
d) |
documente les résultats de son évaluation dans un projet de rapport d'évaluation qui doit être transmis aux États membres concernés dans un délai de vingt-six jours suivant la date de validation. Au plus tard le trente-huitième jour suivant la date de validation, les autres États membres concernés transmettent leurs observations et propositions à propos du projet de rapport d'évaluation et de la demande sous-jacente à l'État membre coordonnateur, qui en tient dûment compte lors de l'établissement du rapport définitif d'évaluation, qui doit être transmis au promoteur et aux autres États membres concernés dans un délai de quarante-cinq jours suivant la date de validation. |
Tous les autres États membres concernés tiennent compte du rapport définitif d'évaluation pour statuer sur la demande du promoteur conformément à l'article 66, paragraphe 7.
5. En ce qui concerne l'évaluation de la documentation visée au paragraphe 3, deuxième alinéa, chacun des États membres concernés peut demander, à une seule reprise, des informations complémentaires au promoteur. Le promoteur communique les informations complémentaires demandées dans le délai fixé par l'État membre concerné, qui ne dépasse pas douze jours à compter de la réception de la demande. Le dernier délai visé au paragraphe 4, point d), cesse de courir entre la date de la demande et la réception des informations complémentaires.
6. Pour les dispositifs des classes C et D, l'État membre coordonnateur peut également prolonger les délais visés au paragraphe 4 de cinquante jours supplémentaires aux fins de la consultation d'experts.
7. La Commission peut, au moyen d'actes d'exécution, définir avec davantage de précision les procédures et les calendriers applicables aux évaluations coordonnées que doivent prendre en compte les États membres concernés pour statuer sur la demande du promoteur. Ces actes d'exécution peuvent aussi fixer les procédures et les calendriers applicables aux évaluations coordonnées en cas de modifications substantielles conformément au paragraphe 12 du présent article, de notification d'un événement indésirable conformément à l'article 76, paragraphe 4, et en cas d'études des performances concernant des diagnostics compagnons dans lesquelles les médicaments font l'objet d'une évaluation coordonnée parallèle d'un essai clinique au titre du règlement (UE) no 536/2014. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107 paragraphe 3.
8. Lorsque, concernant le volet faisant l'objet d'une évaluation coordonnée, l'État membre coordonnateur parvient à la conclusion que la réalisation de l'étude des performances est acceptable, ou acceptable sous réserve du respect de conditions spécifiques, cette conclusion est réputée être la conclusion de tous les États membres concernés.
Nonobstant le premier alinéa, un État membre concerné peut contester la conclusion de l'État membre coordonnateur pour ce qui concerne le volet faisant l'objet d'une évaluation coordonnée uniquement pour les motifs suivants:
a) |
lorsqu'il considère que la participation à l'étude des performances entraînerait pour le participant un traitement de qualité inférieure à la pratique clinique normale dans l'État membre concerné; |
b) |
en cas de violation du droit national; ou |
c) |
en cas d'observations relatives à la sécurité des participants ainsi qu'à la fiabilité et à la robustesse des données transmises au titre du paragraphe 4, point d). |
Lorsque l'un des États membres concernés conteste la conclusion sur la base du deuxième alinéa du présent article, il communique son désaccord, auquel est jointe une justification détaillée, à la Commission, à tous les autres États membres concernés et au promoteur via le système électronique visé à l'article 69.
9. Lorsque la conclusion de l'État membre coordonnateur concernant le volet faisant l'objet d'une évaluation coordonnée est que l'étude des performances n'est pas acceptable, cette conclusion est réputée être la conclusion de tous les États membres concernés.
10. Un État membre concerné refuse d'autoriser une étude des performances s'il est en désaccord avec la conclusion de l'État membre coordonnateur pour l'un des motifs visés au paragraphe 8, deuxième alinéa, ou s'il estime, pour des raisons dûment justifiées, que les aspects traités dans la documentation fournie en application de l'annexe XIV, chapitre I, sections 1.13, 4.2, 4.3 et 4.4, ne sont pas respectés, ou lorsqu'un comité d'éthique a émis, concernant ladite étude des performances, un avis défavorable qui, conformément au droit national, est valable pour l'ensemble dudit État membre. L'État membre en question prévoit une procédure de recours pour un tel refus.
11. Chaque État membre concerné indique au promoteur, via le système électronique visé à l'article 69, si l'étude des performances est autorisée, si elle est autorisée sous conditions ou si l'autorisation a été refusée. La notification est effectuée sous la forme d'une décision unique dans un délai de cinq jours suivant la transmission, par l'État membre coordonnateur, du rapport définitif d'évaluation conformément au paragraphe 4, point d), du présent article. Lorsqu'une autorisation d'étude des performances est soumise à des conditions, il ne peut s'agir que de conditions qui, de par leur nature, ne peuvent pas être respectées au moment de ladite autorisation.
12. Les éventuelles modifications substantielles visées à l'article 71 sont notifiées aux États membres concernés via le système électronique visé à l'article 69. Toute évaluation destinée à déterminer d'éventuels motifs de désaccord, tels qu'ils sont visés au paragraphe 8, deuxième alinéa, du présent article, est menée sous la direction de l'État membre coordonnateur, sauf pour ce qui concerne les modifications substantielles concernant l'annexe XIV, chapitre I, sections 1.13, 4.2, 4.3 et 4.4, et l'annexe XIII, partie A, section 2.3.2, point c), qui sont évaluées séparément par chacun des États membres concernés.
13. La Commission apporte son appui administratif à l'État membre coordonnateur dans l'exécution de ses tâches en vertu du présent chapitre.
14. La procédure prévue au présent article ne s'applique, jusqu'au 25 mai 2029, qu'aux États membres dans lesquels les études de performances doivent être menées et qui ont accepté le recours à cette procédure. À partir du 26 mai 2029, la procédure s'applique à tous les États membres.
Article 75
Réexamen de la procédure d'évaluation coordonnée
Au plus tard le 27 mai 2028, la Commission présente au Parlement européen et au Conseil un rapport sur l'expérience acquise dans le cadre de l'application de l'article 74 et, au besoin, propose de réexaminer l'article 74, paragraphe 14, et l'article 113, paragraphe 3, point g).
Article 76
Enregistrement et notification des événements indésirables survenant pendant les études des performances
1. Le promoteur enregistre intégralement:
a) |
tout événement indésirable d'un type défini dans le plan d'étude des performances comme étant déterminant pour l'évaluation des résultats de ladite étude des performances; |
b) |
tout événement indésirable grave; |
c) |
toute défectuosité d'un dispositif qui aurait pu déboucher sur un événement indésirable grave en l'absence de mesures appropriées ou d'une intervention, ou si les circonstances avaient été moins favorables; |
d) |
tout nouvel élément concernant un événement visé aux points a) à c). |
2. Le promoteur notifie sans tarder à tous les États membres dans lesquels une étude des performances est en cours, via le système électronique visé à l'article 69:
a) |
tout événement indésirable grave entretenant avec le dispositif, le dispositif comparateur ou la procédure d'étude, un lien de causalité avéré ou raisonnablement envisageable; |
b) |
toute défectuosité d'un dispositif qui aurait pu déboucher sur un événement indésirable grave en l'absence de mesures appropriées ou d'une intervention, ou si les circonstances avaient été moins favorables; |
c) |
tout nouvel élément concernant un événement visé aux points a) et b). |
Le délai de notification tient compte de la sévérité de l'événement. Pour permettre une notification en temps opportun, le promoteur peut, s'il y a lieu, présenter un premier rapport incomplet avant d'en remettre un qui soit complet.
À la demande d'un État membre dans lequel l'étude des performances est en cours, le promoteur fournit toutes les informations visées au paragraphe 1.
3. Le promoteur notifie également aux États membres dans lesquels une étude des performances est en cours, via le système électronique visé à l'article 69, tout événement visé au paragraphe 2 du présent article survenu dans un pays tiers dans lequel une étude des performances est réalisée suivant le même plan d'étude des performances cliniques que celui appliqué à une étude des performances relevant du présent règlement.
4. Dans le cas d'une étude des performances pour laquelle le promoteur a introduit la demande unique visée à l'article 74, celui-ci notifie tout événement visé au paragraphe 2 du présent article via le système électronique visé à l'article 69. Dès sa réception, le rapport correspondant est transmis par voie électronique à tous les États membres dans lesquels l'étude est en cours.
Sous la direction de l'État membre coordonnateur visé à l'article 74, paragraphe 2, les États membres coordonnent leur évaluation des événements indésirables graves et des défectuosités de dispositifs pour déterminer s'il y a lieu de modifier, de suspendre ou de mettre fin à l'étude des performances ou de révoquer l'autorisation relative à ladite étude des performances.
Le présent paragraphe est sans effet sur le droit des autres États membres de réaliser leur propre évaluation et d'adopter des mesures conformément au présent règlement pour garantir la protection de la santé publique et de la sécurité des patients. L'État membre coordonnateur et la Commission sont informés des résultats d'une telle évaluation et de l'adoption de telles mesures.
5. Dans le cas des études SPAC visées à l'article 70, paragraphe 1, ce sont les dispositions relatives à la vigilance établies aux articles 82 à 85 et dans les actes d'exécution adoptés conformément à l'article 86 qui s'appliquent, et non celles du présent article.
6. Nonobstant le paragraphe 5, le présent article s'applique lorsqu'un lien de causalité a été établi entre l'événement indésirable grave et l'étude des performances qui le précède.
Article 77
Actes d'exécution
La Commission peut, au moyen d'actes d'exécution, définir les modalités et les aspects procéduraux liés à l'application du présent chapitre en ce qui concerne:
a) |
des formulaires électroniques harmonisés pour les demandes relatives aux études des performances et leur évaluation, visées aux articles 66 et 74, eu égard aux catégories ou groupes spécifiques de dispositifs; |
b) |
le fonctionnement du système électronique visé à l'article 69; |
c) |
des formulaires électroniques harmonisés pour la notification d'études SPAC visées à l'article 70, paragraphe 1, et de modifications substantielles visées à l'article 71; |
d) |
l'échange d'informations entre les États membres visé à l'article 72; |
e) |
des formulaires électroniques harmonisés pour la notification d'événements indésirables graves et de défectuosités de dispositifs, visés à l'article 76; |
f) |
les délais de notification d'événements indésirables graves et de défectuosités de dispositifs, eu égard à la sévérité de l'événement devant faire l'objet d'un rapport visé à l'article 76; |
g) |
l'application uniforme des exigences en ce qui concerne la preuve/les données cliniques requises pour démontrer la conformité avec les exigences générales en matière de sécurité et de performances énoncées à l'annexe I. |
Les actes d'exécution visés au premier alinéa sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
CHAPITRE VII
SURVEILLANCE APRÈS COMMERCIALISATION, VIGILANCE ET SURVEILLANCE DU MARCHÉ
Section 1
Surveillance après commercialisation
Article 78
Système de surveillance après commercialisation mis en place par le fabricant
1. Pour chaque dispositif, les fabricants conçoivent, établissent, documentent, appliquent, maintiennent et mettent à jour un système de surveillance après commercialisation en fonction de la classe de risque et du type de dispositif. Ce système fait partie intégrante du système de gestion de la qualité du fabricant visé à l'article 10, paragraphe 8.
2. Le système de surveillance après commercialisation permet de collecter, d'enregistrer et d'analyser, d'une manière active et systématique, les données pertinentes sur la qualité, les performances et la sécurité d'un dispositif pendant toute sa durée de vie, de tirer les conclusions qui s'imposent et de définir et d'appliquer toute mesure préventive ou corrective et d'en assurer le suivi.
3. Les données collectées au titre du système de surveillance après commercialisation mis en place par le fabricant sont en particulier utilisées pour:
a) |
actualiser la détermination du rapport bénéfice/risque et améliorer la gestion des risques visées à l'annexe I, chapitre I; |
b) |
actualiser les informations sur la conception et la fabrication, la notice d'utilisation et l'étiquetage; |
c) |
actualiser l'évaluation des performances; |
d) |
actualiser le résumé des caractéristiques de sécurité et des performances visé à l'article 29; |
e) |
faire apparaître les besoins en matière de mesures préventives, de mesures correctives ou de mesures correctives de sécurité; |
f) |
répertorier les possibilités d'amélioration de la facilité d'utilisation, des performances et de la sécurité du dispositif; |
g) |
le cas échéant, contribuer à la surveillance après commercialisation d'autres dispositifs; et |
h) |
identifier les tendances et en rendre compte conformément à l'article 83. |
La documentation technique est mise à jour en conséquence.
4. Si, dans le cadre de la surveillance après commercialisation, il apparaît que des mesures préventives ou correctives ou les deux sont nécessaires, le fabricant applique les mesures appropriées et informe les autorités compétentes concernées ainsi que, le cas échéant, l'organisme notifié. Lorsqu'un incident grave est constaté ou qu'une mesure corrective de sécurité est appliquée, cela est notifié conformément à l'article 82.
Article 79
Plan de surveillance après commercialisation
Le système de surveillance après commercialisation visé à l'article 78 est fondé sur un plan de surveillance après commercialisation, dont les caractéristiques sont exposées à l'annexe III, section 1. Le plan de surveillance après commercialisation fait partie de la documentation technique prévue à l'annexe II.
Article 80
Rapport sur la surveillance après commercialisation
Les fabricants de dispositifs des classes A et B établissent un rapport sur la surveillance après commercialisation faisant la synthèse des résultats et des conclusions de l'analyse des données de surveillance après commercialisation qui ont été collectées dans le cadre du plan de surveillance après commercialisation visé à l'article 79, exposant la justification de toute mesure préventive ou corrective prise et les décrivant. Le rapport est mis à jour selon les besoins et mis à la disposition de l'organisme notifié et de l'autorité compétente sur demande.
Article 81
Rapport périodique actualisé de sécurité
1. Les fabricants de dispositifs des classes C et D établissent, pour chaque dispositif et, le cas échéant, pour chaque catégorie ou groupe de dispositifs, un rapport périodique actualisé de sécurité (PSUR) faisant la synthèse des résultats et des conclusions de l'analyse des données de surveillance après commercialisation qui ont été collectées dans le cadre du plan de surveillance après commercialisation visé à l'article 79, exposant la justification de toute mesure préventive ou corrective prise et les décrivant. Pendant toute la durée de vie du dispositif concerné, ce PSUR décrit:
a) |
les conclusions de la détermination du rapport bénéfice/risque; |
b) |
les principales constatations du SPAC; et |
c) |
le volume des ventes du dispositif et une estimation de la taille et d'autres caractéristiques de la population utilisant le dispositif et, si possible, la fréquence d'utilisation du dispositif. |
Les fabricants de dispositifs des classes C et D mettent le PSUR à jour au moins une fois par an. Ce PSUR fait partie de la documentation technique prévue aux annexes II et III.
2. Les fabricants de dispositifs de classe D communiquent les PSUR à l'organisme notifié intervenant dans l'évaluation de la conformité de ces dispositifs conformément à l'article 48, via le système électronique visé à l'article 87. L'organisme notifié examine les rapports et enregistre son évaluation, assortie de toute mesure prise, dans ce système électronique. Ces PSUR et l'évaluation de l'organisme notifié sont mis à la disposition des autorités compétentes via ce système électronique.
3. Pour les dispositifs de classe C, les fabricants mettent les PSUR à la disposition de l'organisme notifié intervenant dans l'évaluation de la conformité et, sur demande, des autorités compétentes.
Section 2
Vigilance
Article 82
Notification des incidents graves et des mesures correctives de sécurité
1. Les fabricants de dispositifs mis à disposition sur le marché de l'Union, autres que les dispositifs devant faire l'objet d'une étude des performances, notifient aux autorités compétentes concernées, conformément à l'article 87, paragraphes 5 et 7, les éléments suivants:
a) |
tout incident grave concernant des dispositifs mis à disposition sur le marché de l'Union, à l'exception des résultats erronés attendus qui sont clairement documentés et quantifiés dans les informations relatives au produit et dans la documentation technique et qui font l'objet d'un rapport de tendances en application de l'article 83; |
|
b) |
toute mesure corrective de sécurité prise à l'égard de dispositifs mis à disposition sur le marché de l'Union, ainsi que toute mesure corrective de sécurité prise dans un pays tiers concernant un dispositif qui est aussi légalement mis à disposition sur le marché de l'Union, lorsque la raison justifiant la mesure ne concerne pas exclusivement le dispositif mis à disposition dans le pays tiers. |
Les rapports visés au premier alinéa sont soumis via le système électronique visé à l'article 87.
2. D'une manière générale, le délai de notification visé au paragraphe 1 tient compte de la sévérité de l'incident.
3. Les fabricants notifient tout incident grave visé au paragraphe 1, point a), immédiatement après avoir établi un lien de causalité avéré ou raisonnablement envisageable avec leur dispositif, et au plus tard quinze jours après qu'ils ont eu connaissance de l'incident.
4. Nonobstant le paragraphe 3, en cas de menace grave pour la santé publique, la notification visée au paragraphe 1 a lieu immédiatement, et au plus tard deux jours après que le fabricant a eu connaissance de cette menace.
5. Nonobstant le paragraphe 3, en cas de décès ou de grave détérioration inattendue de l'état de santé d'une personne, la notification a lieu immédiatement après que le fabricant a établi ou dès qu'il soupçonne un lien de causalité entre le dispositif et l'incident grave, mais au plus tard dix jours après qu'il a eu connaissance de l'incident grave.
6. Pour permettre une notification en temps opportun, le fabricant peut, s'il y a lieu, présenter un premier rapport incomplet avant d'en remettre un qui soit complet.
7. Si, après avoir eu connaissance d'un incident susceptible de devoir être notifié, le fabricant nourrit des incertitudes sur ce point, il présente néanmoins un rapport dans le délai prescrit conformément aux paragraphes 2 à 5.
8. Sauf en cas d'urgence où il doit prendre immédiatement une mesure corrective de sécurité, le fabricant notifie, sans retard injustifié, la mesure corrective de sécurité visée au paragraphe 1, point b), avant que cette mesure ne soit prise.
9. Pour les incidents graves similaires ayant trait au même dispositif ou type de dispositif, dont la cause a été déterminée ou pour lesquels une mesure corrective de sécurité a été appliquée, ou lorsque les incidents sont communs et bien documentés, le fabricant peut transmettre périodiquement des rapports de synthèse au lieu de rapports d'incidents graves distincts, à condition que l'autorité compétente coordonnatrice visée à l'article 84, paragraphe 9, en concertation avec les autorités compétentes visées à l'article 87, paragraphe 8, points a) et b), ait convenu avec le fabricant du format, du contenu et de la périodicité des rapports de synthèse. Lorsqu'une seule autorité compétente est visée à l'article 87, paragraphe 8, points a) et b), le fabricant peut transmettre périodiquement des rapports de synthèse en accord avec cette autorité compétente.
10. Les États membres prennent les mesures appropriées, telles que l'organisation de campagnes de sensibilisation ciblées, pour encourager les professionnels de la santé, les utilisateurs et les patients à communiquer aux autorités compétentes les incidents graves supposés visés au paragraphe 1, point a), et leur donner les moyens de le faire.
Les autorités compétentes enregistrent au niveau national de manière centralisée les déclarations qu'elles reçoivent des professionnels de la santé, des utilisateurs et des patients.
11. Lorsque l'autorité compétente d'un État membre reçoit, d'un professionnel de la santé, d'un utilisateur ou d'un patient, les déclarations concernant un incident grave supposé visé au paragraphe 1, point a), elle prend les mesures nécessaires pour garantir que le fabricant du dispositif est informé sans tarder de l'incident grave supposé.
Lorsque le fabricant du dispositif concerné estime que l'incident constitue un incident grave, il présente, conformément aux paragraphes 1 à 5 du présent article, un rapport sur cet incident grave à l'autorité compétente de l'État membre dans lequel cet incident s'est produit et prend les mesures de suivi appropriées conformément à l'article 84.
Lorsque le fabricant du dispositif concerné estime que l'incident ne constitue pas un incident grave ou doit être considéré comme une progression des résultats erronés attendus qui feront l'objet d'un rapport de tendances conformément à l'article 83, il fournit une déclaration explicative. Si l'autorité compétente ne partage pas les conclusions de la déclaration explicative, elle peut exiger du fabricant qu'il fasse une notification conformément aux paragraphes 1 à 5 du présent article et qu'il prenne les mesures de suivi appropriées conformément à l'article 84.
Article 83
Rapport de tendances
1. Les fabricants notifient, via le système électronique visé à l'article 87, toute progression statistiquement significative de la fréquence ou de la sévérité des incidents qui ne sont pas des incidents graves qui pourraient avoir une incidence significative sur le rapport bénéfice/risque visé à l'annexe I, sections 1 et 8, et qui ont entraîné ou pourraient entraîner des risques inacceptables pour la santé et la sécurité des patients, des utilisateurs ou d'autres personnes, ou toute progression significative des résultats erronés attendus établie par comparaison avec les performances alléguées du dispositif conformément à l'annexe I, section 9.1, points a) et b), et comme indiqué dans la documentation technique et les informations relatives au produit.
Le fabricant précise les modalités de gestion des incidents visés au premier alinéa ainsi que la méthode permettant d'établir toute progression statistiquement significative de la fréquence ou de la sévérité de ces incidents ou toute modification des performances ainsi que la période d'observation dans le plan de surveillance après commercialisation visé à l'article 79.
2. Les autorités compétentes peuvent réaliser leur propre évaluation des rapports de tendances visés au paragraphe 1 et exiger des fabricants qu'ils adoptent des mesures appropriées conformément au présent règlement pour garantir la protection de la santé publique et de la sécurité des patients. Chaque autorité compétente informe la Commission, les autres autorités compétentes et l'organisme notifié qui a délivré le certificat des résultats d'une telle évaluation et de l'adoption de telles mesures.
Article 84
Analyse des incidents graves et des mesures correctives de sécurité
1. À la suite de la notification d'un incident grave en application de l'article 82, paragraphe 1, le fabricant mène sans tarder les enquêtes nécessaires liées à cet incident et aux dispositifs concernés. Ces enquêtes comprennent notamment une évaluation des risques résultant de l'incident et des mesures correctives de sécurité en tenant compte, le cas échéant, des critères visés au paragraphe 3 du présent article.
Au cours des enquêtes visées au premier alinéa, le fabricant coopère avec les autorités compétentes et, le cas échéant, avec l'organisme notifié concerné; ce faisant, il n'entreprend aucune investigation, sans en informer au préalable les autorités compétentes, qui soit susceptible de modifier le dispositif ou un échantillon du lot concerné au point de compromettre toute évaluation ultérieure des causes de l'incident.
2. Les États membres prennent les mesures nécessaires pour que toute information concernant un incident grave survenu sur leur territoire ou une mesure corrective de sécurité appliquée ou devant être appliquée sur leur territoire, et qui leur a été notifiée conformément à l'article 82, fassent l'objet d'une évaluation centralisée au niveau national par leur autorité compétente, si possible en collaboration avec le fabricant et, le cas échéant, avec l'organisme notifié concerné.
3. Dans le cas de l'évaluation visée au paragraphe 2, l'autorité compétente évalue les risques résultant de l'incident grave et d'éventuelles mesures correctives de sécurité en tenant compte de la protection de la santé publique et de critères comme la causalité, la détectabilité et la probabilité de récurrence du problème, la fréquence d'utilisation du dispositif, la probabilité d'un dommage direct ou indirect, la sévérité de celui-ci, les bénéfices cliniques du dispositif, les utilisateurs auxquels les dispositifs sont ou pourraient être destinés et la population concernée. L'autorité compétente apprécie également le caractère adéquat des mesures correctives de sécurité envisagées ou appliquées par le fabricant, ainsi que l'opportunité et la nature de toute autre mesure corrective, compte tenu notamment du principe de sûreté inhérente inscrit à l'annexe I.
À la demande de l'autorité nationale compétente, les fabricants fournissent tous les documents nécessaires à l'évaluation des risques.
4. L'autorité compétente assure le suivi de l'enquête sur un incident grave menée par le fabricant. Au besoin, une autorité compétente peut intervenir dans l'enquête du fabricant ou lancer une enquête indépendante.
5. Le fabricant présente à l'autorité compétente un rapport définitif énonçant les conclusions qu'il a tirées de l'enquête, via le système électronique visé à l'article 87. Le rapport énonce des conclusions et, le cas échéant, indique les mesures correctives à prendre.
6. Dans le cas des diagnostics compagnons, l'autorité compétente qui réalise l'évaluation ou l'autorité compétente coordonnatrice visée au paragraphe 9 du présent article, informe, le cas échéant, l'autorité compétente concernée de l'État membre qui a autorisé les médicaments ou l'EMA selon que la première ou la seconde a été consultée par l'organisme notifié conformément aux procédures visées à l'annexe IX, section 5.2, et à l'annexe X, section 3.11.
7. Au terme de l'évaluation effectuée conformément au paragraphe 3 du présent article, l'autorité compétente qui réalise l'évaluation informe sans tarder les autres autorités compétentes, via le système électronique visé à l'article 87, de la mesure corrective prise ou envisagée par le fabricant ou imposée à ce dernier pour réduire à un minimum le risque de récurrence de l'incident grave, et leur communique des informations relatives aux incidents graves sous-jacents et aux résultats de l'évaluation qu'elle a réalisée.
8. Le fabricant veille à ce que les informations relatives aux mesures correctives prises soient portées sans tarder à l'attention des utilisateurs du dispositif en question au moyen d'un avis de sécurité. L'avis de sécurité est édité dans une ou des langues officielles de l'Union définies par l'État membre dans lequel la mesure corrective de sécurité est prise. Sauf en cas d'urgence, le contenu du projet d'avis de sécurité est soumis à l'autorité compétente chargée de l'évaluation ou, dans les cas visés au paragraphe 9, à l'autorité compétente coordonnatrice, pour lui permettre de formuler des observations. À moins que la situation particulière d'un État membre ne le justifie, le contenu de l'avis de sécurité est uniforme dans tous les États membres.
L'avis de sécurité permet l'identification correcte du ou des dispositifs concernés, notamment en indiquant l'IUD pertinent et l'identification correcte, notamment en indiquant, s'il est déjà émis, le numéro d'enregistrement unique du fabricant qui a appliqué la mesure corrective de sécurité. L'avis de sécurité expose clairement, sans sous-estimer le niveau de risque, les raisons de la mesure corrective de sécurité par référence au dysfonctionnement du dispositif et aux risques associés qui en résultent pour les patients, les utilisateurs ou d'autres personnes, et indique clairement toutes les dispositions que les utilisateurs doivent prendre.
Le fabricant introduit l'avis de sécurité dans le système électronique visé à l'article 87, de manière à ce qu'il soit accessible pour le public.
9. Les autorités compétentes participent activement à une procédure visant à coordonner leurs évaluations visées au paragraphe 3 dans les cas suivants:
a) |
un incident grave donné ou un ensemble d'incidents graves liés au même dispositif ou type de dispositif du même fabricant suscite des préoccupations dans plus d'un État membre; |
b) |
le caractère approprié d'une mesure corrective de sécurité proposée par un fabricant dans plus d'un État membre est mis en doute. |
Cette procédure coordonnée porte sur:
— |
la désignation d'une autorité compétente coordonnatrice au cas par cas, s'il y a lieu, |
— |
la définition de la procédure d'évaluation coordonnée, notamment des tâches et des responsabilités de l'autorité compétente coordinatrice et l'intervention d'autres autorités compétentes. |
Sauf si les autorités compétentes en conviennent autrement, l'autorité compétente coordonnatrice est l'autorité compétente de l'État membre dans lequel le fabricant a son siège social.
L'autorité compétente coordonnatrice informe, via le système électronique visé à l'article 87, le fabricant, les autres autorités compétentes et la Commission qu'elle assume ladite fonction.
10. La désignation d'une autorité compétente coordonnatrice est sans effet sur le droit des autres autorités compétentes de réaliser leur propre évaluation et d'adopter des mesures conformément au présent règlement pour garantir la protection de la santé publique et de la sécurité des patients. L'autorité compétente coordonnatrice et la Commission sont tenues informées des résultats d'une telle évaluation et de l'adoption de telles mesures.
11. La Commission apporte son appui administratif à l'autorité compétente coordonnatrice dans l'exécution des tâches prévues par le présent chapitre.
Article 85
Analyse des données issues de la vigilance
La Commission met en place, en collaboration avec les États membres, des systèmes et processus destinés à l'analyse active des données disponibles dans le système électronique visé à l'article 87 afin d'identifier les tendances, les évolutions ou les signaux qui, dans les données, mettraient en évidence de nouveaux risques ou de nouvelles sources de préoccupation en matière de sécurité.
Lorsqu'un risque précédemment inconnu est mis en évidence ou lorsque la fréquence d'un risque escompté modifie significativement et défavorablement la détermination du rapport bénéfice/risque, l'autorité compétente ou, le cas échéant, l'autorité compétente coordonnatrice informe le fabricant ou, le cas échéant, le mandataire, qui prend alors les mesures correctives de sécurité nécessaires.
Article 86
Actes d'exécution
La Commission peut, au moyen d'actes d'exécution, et après avoir consulté le GCDM, définir les modalités et les aspects procéduraux pour l'application des articles 80 à 85 et de l'article 87 en ce qui concerne les éléments suivants:
a) |
la typologie des incidents graves et des mesures correctives de sécurité concernant des dispositifs ou des catégories ou groupes de dispositifs donnés; |
b) |
la notification des incidents graves et des mesures correctives de sécurité et les avis de sécurité, ainsi que la fourniture par les fabricants des rapports de synthèse périodiques, des rapports sur la surveillance après commercialisation, des PSUR et des rapports de tendances, visés respectivement aux articles 80, 81, 82, 83 et 84; |
c) |
des formulaires standard structurés pour la notification électronique et non électronique, comprenant un ensemble minimal de données pour la notification des incidents graves supposés par les professionnels de la santé, les utilisateurs et les patients; |
d) |
les délais pour la notification des mesures correctives de sécurité et pour la fourniture de rapports de synthèse périodiques et de rapports de tendances par les fabricants, eu égard à la sévérité de l'incident à notifier conformément à l'article 82; |
e) |
des formulaires harmonisés pour l'échange d'informations entre autorités compétentes visé à l'article 84; |
f) |
des procédures pour la désignation d'une autorité compétente coordonnatrice, la procédure d'évaluation coordonnée, notamment les tâches et responsabilités de l'autorité compétente coordonnatrice et l'intervention d'autres autorités compétentes dans cette procédure. |
Les actes d'exécution visés au premier alinéa sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
Article 87
Système électronique relatif à la vigilance et à la surveillance après commercialisation
1. La Commission, en collaboration avec les États membres, établit et gère un système électronique de collecte et de traitement:
a) |
les rapports des fabricants sur les incidents graves et les mesures correctives de sécurité, visées à l'article 82, paragraphe 1, et à l'article 84, paragraphe 5; |
b) |
les rapports de synthèse périodiques établis par les fabricants, visés à l'article 82, paragraphe 9; |
c) |
les rapports de tendances établis par les fabricants, visés à l'article 83; |
d) |
les PSUR visés à l'article 81; |
e) |
les avis de sécurité des fabricants, visés à l'article 84, paragraphe 8; |
f) |
les informations échangées entre les autorités compétentes des États membres et entre celles-ci et la Commission conformément à l'article 84, paragraphes 7 et 9. |
Ce système électronique contient tous les liens pertinents vers la base de données IUD.
2. Les informations visées au paragraphe 1 du présent article sont mises à la disposition des autorités compétentes des États membres et de la Commission via le système électronique. Les organismes notifiés ont également accès à ces informations, dans la mesure où celles-ci ont un lien avec les dispositifs pour lesquels ils ont délivré un certificat en application de l'article 49.
3. La Commission veille à ce que les professionnels de la santé et le public aient un accès approprié au système électronique visé au paragraphe 1.
4. Sur la base d'accords entre la Commission et les autorités compétentes de pays tiers ou des organisations internationales, la Commission peut accorder à celles-ci, dans la mesure requise, un accès au système électronique visé au paragraphe 1. Ces accords sont fondés sur la réciprocité et prévoient des règles de confidentialité et de protection des données équivalentes à celles qui sont applicables dans l'Union.
5. Les rapports sur les incidents graves visés à l'article 82, paragraphe 1, point a), sont automatiquement transmis, dès réception, via le système électronique visé au paragraphe 1 du présent article, à l'autorité compétente de l'État membre dans lequel l'incident est survenu.
6. Les rapports de tendances visés à l'article 83, paragraphe 1, sont automatiquement transmis, dès réception, via le système électronique visé au paragraphe 1 du présent article, à l'autorité compétente de l'État membre dans lequel les incidents sont survenus.
7. Les rapports sur les mesures correctives de sécurité visés à l'article 82, paragraphe 1, point b), sont automatiquement transmis, dès réception, via le système électronique visé au paragraphe 1 du présent article, à l'autorité compétente des États membres suivants:
a) |
l'État membre dans lequel la mesure corrective de sécurité est ou doit être appliquée; |
b) |
l'État membre dans lequel le fabricant a son siège social. |
8. Les rapports de synthèse périodiques visés à l'article 82, paragraphe 9, sont automatiquement transmis, dès réception, via le système électronique visé au paragraphe 1 du présent article, à l'autorité compétente:
a) |
de l'État membre ou des États membres participant à la procédure de coordination visée à l'article 84, paragraphe 9, et qui ont marqué leur accord sur le rapport de synthèse périodique; |
b) |
de l'État membre dans lequel le fabricant a son siège social. |
9. Les informations visées aux paragraphes 5 à 8 du présent article sont automatiquement transmises, dès réception, via le système électronique visé au paragraphe 1 du présent article, à l'organisme notifié qui a délivré le certificat pour le dispositif concerné conformément à l'article 51.
Section 3
Surveillance du marché
Article 88
Activités de surveillance du marché
1. Les autorités compétentes contrôlent de manière appropriée les caractéristiques en matière de conformité et les performances des dispositifs notamment, le cas échéant, par l'examen de la documentation et par des essais physiques ou en laboratoire sur la base d'échantillons adéquats. Les autorités compétentes tiennent notamment compte des principes établis en matière d'évaluation et de gestion des risques, des données issues de la vigilance et des réclamations.
2. Les autorités compétentes élaborent des programmes annuels pour les activités de surveillance et y consacrent les ressources matérielles et humaines appropriées pour pouvoir réaliser ces activités, compte tenu du programme européen de surveillance du marché mis au point par le GCDM en vertu de l'article 99 et en fonction des conditions locales.
3. Afin de remplir les obligations qui leur incombent en vertu du paragraphe 1, les autorités compétentes:
a) |
peuvent exiger, entre autres, que la documentation et les informations requises pour mener leurs activités soient fournies par les opérateurs économiques et, si cela est justifié, que ceux-ci fournissent gratuitement les échantillons de dispositifs dont elles ont besoin ou donnent accès gratuitement aux dispositifs; et |
b) |
effectuent des inspections annoncées et, si nécessaire, des inspections inopinées dans les locaux des opérateurs économiques, ainsi que des fournisseurs et/ou sous-traitants, et, au besoin, dans les installations des utilisateurs professionnels. |
4. Les autorités compétentes établissent un résumé annuel des résultats de leurs activités de surveillance et le mettent à la disposition des autres autorités compétentes via le système électronique visé à l'article 95.
5. Les autorités compétentes peuvent confisquer, détruire ou rendre inutilisables par d'autres moyens les dispositifs qui présentent un risque inacceptable ou les dispositifs falsifiés si elles le jugent nécessaire dans l'intérêt de la protection de la santé publique.
6. Après chacune des inspections effectuées aux fins visées au paragraphe 1, l'autorité compétente établit un rapport sur les conclusions de l'inspection concernant le respect des exigences légales et techniques applicables en vertu du présent règlement. Le rapport indique d'éventuelles mesures correctives nécessaires.
7. L'autorité compétente qui a effectué l'inspection communique la teneur du rapport visé au paragraphe 6 du présent article à l'opérateur économique qui a fait l'objet de l'inspection. Avant d'adopter le rapport définitif, l'autorité compétente donne à cet opérateur économique la possibilité de présenter des observations. Ledit rapport d'inspection définitif est introduit dans le système électronique prévu à l'article 95.
8. Les États membres procèdent à l'examen et à l'évaluation du fonctionnement de leurs activités de surveillance du marché. Cet examen et cette évaluation sont réalisés au moins tous les quatre ans et leurs résultats sont communiqués aux autres États membres et à la Commission. Chaque État membre met un résumé de ces résultats à la disposition du public via le système électronique visé à l'article 95.
9. Les autorités compétentes des États membres coordonnent leurs activités de surveillance du marché, coopèrent et partagent, également avec la Commission, les résultats y afférents, afin d'assurer un niveau élevé et harmonisé de surveillance du marché dans l'ensemble des États membres.
S'il y a lieu, les autorités compétentes des États membres conviennent de partager leurs tâches, de mener des activités conjointes de surveillance du marché et de se spécialiser.
10. Lorsque, dans un même État membre, plusieurs autorités sont responsables de la surveillance du marché et des contrôles aux frontières extérieures, elles coopèrent en partageant les informations relatives à leur rôle et à leurs fonctions.
11. S'il y a lieu, les autorités compétentes des États membres coopèrent avec celles de pays tiers en matière d'échange d'informations, d'assistance technique et de développement d'activités liées à la surveillance du marché.
Article 89
Évaluation des dispositifs dont on suspecte qu'ils présentent un risque inacceptable ou une autre non-conformité
Lorsque les autorités compétentes d'un État membre, sur la base des données issues de la vigilance ou des activités de surveillance du marché ou d'autres informations, ont des raisons de croire qu'un dispositif:
a) |
est susceptible de présenter un risque inacceptable pour la santé ou la sécurité des patients, des utilisateurs ou d'autres personnes, ou compte tenu d'autres aspects liés à la protection de la santé publique; ou |
b) |
n'est pas conforme, de toute autre façon, aux exigences du présent règlement, |
elles réalisent une évaluation du dispositif concerné, portant sur toutes les exigences du présent règlement relatives au risque présenté par le dispositif ou à toute autre non-conformité du dispositif.
Les opérateurs économiques concernés coopèrent avec les autorités compétentes.
Article 90
Procédure applicable aux dispositifs présentant un risque inacceptable pour la santé et la sécurité
1. Lorsque, à l'issue d'une évaluation réalisée en application de l'article 89, les autorités compétentes concluent qu'un dispositif présente un risque inacceptable pour la santé ou la sécurité des patients, des utilisateurs ou d'autres personnes, ou compte tenu d'autres aspects liés à la protection de la santé publique, elles exigent sans tarder du fabricant du dispositif concerné, de son mandataire et de tous les autres opérateurs économiques concernés qu'ils prennent toutes les mesures correctives appropriées et dûment justifiées pour rendre le dispositif conforme aux exigences du présent règlement relatives au risque présenté par le dispositif et, d'une manière qui soit proportionnée à la nature du risque, restreindre la mise à disposition du dispositif sur le marché, l'assortir d'exigences particulières, retirer le dispositif du marché ou le rappeler, dans un délai raisonnable clairement défini qui est communiqué à l'opérateur économique concerné.
2. Les autorités compétentes notifient sans tarder à la Commission, aux autres États membres et, lorsqu'un certificat a été délivré, conformément à l'article 51 pour le dispositif concerné, à l'organisme notifié qui a délivré ce certificat, les résultats de l'évaluation et les mesures imposées aux opérateurs économiques concernés, via le système électronique visé à l'article 95.
3. Les opérateurs économiques visés au paragraphe 1 s'assurent sans tarder que toutes les mesures correctives appropriées sont prises dans l'ensemble de l'Union pour tous les dispositifs en cause qu'il a mis à disposition sur le marché.
4. Lorsque l'opérateur économique visé au paragraphe 1 ne prend pas de mesures correctives adéquates dans le délai visé au paragraphe 1, les autorités compétentes prennent toutes les mesures appropriées pour interdire ou restreindre la mise à disposition du dispositif sur leur marché national, pour l'en retirer ou pour le rappeler.
Les autorités compétentes notifient sans tarder ces mesures à la Commission, aux autres États membres et à l'organisme notifié visé au paragraphe 2 du présent article, via le système électronique visé à l'article 95.
5. La notification visée au paragraphe 4 précise toutes les données disponibles, notamment celles permettant d'identifier le dispositif non conforme, d'en assurer la traçabilité et de déterminer son origine, la nature et les raisons de la non-conformité alléguée et du risque encouru, ainsi que la nature et la durée des mesures prises au niveau national et les arguments avancés par l'opérateur économique concerné.
6. Les États membres autres que celui qui engage la procédure notifient sans tarder à la Commission et aux autres États membres, via le système électronique visé à l'article 95, toute information supplémentaire pertinente dont ils disposent concernant la non-conformité du dispositif concerné ainsi que toute mesure qu'ils ont adoptée à l'égard de celui-ci.
En cas de désaccord avec la mesure nationale notifiée, ils informent sans tarder la Commission et les autres États membres de leurs objections, via le système électronique visé à l'article 95.
7. Lorsque, dans un délai de deux mois à compter de la réception de la notification visée au paragraphe 4, aucune objection n'a été soulevée par un État membre ou par la Commission à l'encontre d'une des mesures prises par un État membre, ces mesures sont considérées comme justifiées. Dans ce cas, tous les États membres veillent à ce que des mesures restrictives ou des mesures d'interdiction appropriées, y compris le retrait, le rappel ou la limitation de la mise à disposition du dispositif sur leur marché national, soient prises sans tarder à l'égard du dispositif concerné.
Article 91
Procédure d'évaluation des mesures nationales au niveau de l'Union
1. Lorsque, dans un délai de deux mois suivant la réception de la notification visée à l'article 90, paragraphe 4, un État membre soulève des objections à l'encontre d'une mesure prise par un autre État membre ou que la Commission estime que celle-ci est contraire à la législation de l'Union, la Commission évalue cette mesure nationale, après avoir consulté les autorités compétentes concernées et, le cas échéant, les opérateurs économiques concernés. En fonction des résultats de cette évaluation, la Commission peut décider, au moyen d'actes d'exécution, si la mesure nationale est justifiée ou non. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
2. Lorsque la Commission considère que la mesure nationale est justifiée en application du paragraphe 1 du présent article, l'article 90, paragraphe 7, deuxième alinéa, s'applique. Si la Commission considère que la mesure nationale n'est pas justifiée, l'État membre concerné retire la mesure en cause.
Lorsque la Commission ne prend pas de décision en application du paragraphe 1 du présent article dans un délai de huit mois suivant la réception de la notification visée à l'article 90, paragraphe 4, la mesure nationale est considérée comme justifiée.
3. Lorsqu'un État membre ou la Commission considère que le risque pour la santé et la sécurité présenté par un dispositif ne peut pas être atténué de manière satisfaisante par les mesures prises par le ou les États membres concernés, la Commission, à la demande d'un État membre ou de sa propre initiative, peut prendre, au moyen d'actes d'exécution, les mesures nécessaires et dûment justifiées pour garantir la protection de la santé et de la sécurité, notamment des mesures de restriction ou d'interdiction de la mise sur le marché et de la mise en service du dispositif concerné. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
Article 92
Autre non-conformité
1. Lorsque, à l'issue d'une évaluation réalisée en application de l'article 89, les autorités compétentes d'un État membre concluent qu'un dispositif n'est pas conforme aux exigences du présent règlement mais ne présente pas un risque inacceptable pour la santé ou la sécurité des patients, des utilisateurs ou d'autres personnes, ou compte tenu d'autres aspects liés à la protection de la santé publique, elles exigent de l'opérateur économique concerné qu'il mette un terme à la non-conformité en cause dans un délai raisonnable clairement défini qui est communiqué à l'opérateur économique et qui est proportionné à la non-conformité.
2. Lorsque l'opérateur économique ne met pas un terme à la non-conformité dans le délai visé au paragraphe 1 du présent article, l'État membre concerné prend sans tarder toutes les mesures appropriées pour restreindre ou interdire la mise à disposition du produit sur le marché, ou pour que celui-ci soit rappelé ou retiré du marché. Il notifie sans tarder ces mesures à la Commission et aux autres États membres via le système électronique visé à l'article 95.
3. Afin d'assurer l'application uniforme du présent article, la Commission peut, au moyen d'actes d'exécution, définir les mesures appropriées à prendre par les autorités compétentes pour traiter certains types de non-conformité. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
Article 93
Mesures préventives de protection de la santé
1. Lorsqu'un État membre, à l'issue d'une évaluation indiquant qu'un dispositif ou une catégorie ou un groupe spécifique de dispositifs présente un risque potentiel, considère que, pour protéger la santé et la sécurité des patients, des utilisateurs ou d'autres personnes, ou compte tenu d'autres aspects liés à la santé publique, la mise à disposition sur le marché ou la mise en service d'un dispositif ou d'une catégorie ou d'un groupe spécifique de dispositifs devrait être interdite, restreinte ou assortie d'exigences particulières, ou que le dispositif ou la catégorie ou le groupe de dispositifs en question devrait être retiré du marché ou rappelé, il peut prendre toute mesure nécessaire et justifiée.
2. L'État membre visé au paragraphe 1 notifie immédiatement ces mesures, en motivant sa décision, à la Commission et à tous les autres États membres via le système électronique visé à l'article 95.
3. La Commission, en concertation avec le GCDM et, le cas échéant, les opérateurs économiques concernés, évalue les mesures nationales prises. La Commission peut décider, au moyen d'actes d'exécution, si les mesures nationales sont justifiées ou non. En l'absence de décision de la Commission dans un délai de six mois suivant leur notification, les mesures nationales sont considérées comme justifiées. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
4. Lorsque l'évaluation visée au paragraphe 3 du présent article montre que la mise à disposition sur le marché ou la mise en service d'un dispositif ou d'une catégorie ou d'un groupe spécifique de dispositifs devrait être interdite, restreinte ou assortie d'exigences particulières, ou que le dispositif ou la catégorie ou le groupe de dispositifs en question devrait être retiré du marché ou rappelé dans tous les États membres pour protéger la santé et la sécurité des patients, des utilisateurs ou d'autres personnes, ou compte tenu d'autres aspects liés à la santé publique, la Commission peut adopter des actes d'exécution pour prendre les mesures nécessaires et dûment justifiées. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
Article 94
Bonnes pratiques administratives
1. Toute mesure adoptée par les autorités compétentes des États membres en vertu des articles 90 à 93 indique les motifs exacts sur lesquels elle repose. Lorsqu'une telle mesure est adressée à un opérateur économique particulier, l'autorité compétente la notifie sans tarder à l'opérateur économique en question et elle l'informe en même temps des voies de recours dont il dispose en vertu du droit ou des pratiques administratives de l'État membre concerné ainsi que des délais y afférents. Si la mesure présente une applicabilité générale, elle est publiée en conséquence.
2. Sauf lorsqu'une action immédiate est requise en raison d'un risque inacceptable pour la santé et la sécurité des personnes, l'opérateur économique concerné doit avoir la possibilité de présenter ses observations à l'autorité compétente dans un délai approprié clairement défini avant l'adoption d'une mesure.
Lorsqu'une mesure a été prise sans que l'opérateur économique ait eu la possibilité de présenter ses observations conformément au premier alinéa, il doit pouvoir présenter ses observations dès que possible, après quoi la mesure adoptée est réexaminée dans les meilleurs délais.
3. Toute mesure adoptée est immédiatement retirée ou modifiée si l'opérateur économique prouve qu'il a pris des mesures correctives efficaces et que le dispositif est conforme aux exigences du présent règlement.
4. Lorsqu'une mesure adoptée en vertu des articles 90 à 93 concerne un dispositif pour l'évaluation de la conformité duquel un organisme notifié est intervenu, les autorités compétentes informent celui-ci ainsi que l'autorité responsable dont il relève de la mesure prise, via le système électronique visé à l'article 95.
Article 95
Système électronique relatif à la surveillance du marché
1. La Commission, en collaboration avec les États membres, établit et gère un système électronique de collecte et de traitement:
a) |
des résumés des résultats des activités de surveillance, visés à l'article 88, paragraphe 7; |
b) |
du rapport d'inspection définitif visé à l'article 88, paragraphe 7; |
c) |
des informations relatives aux dispositifs présentant un risque inacceptable pour la santé et la sécurité, visées à l'article 90, paragraphes 2, 4 et 6; |
d) |
des informations relatives à la non-conformité des produits, visées à l'article 92, paragraphe 2; |
e) |
des informations relatives aux mesures préventives de protection de la santé, visées à l'article 93, paragraphe 2; |
f) |
des résumés des résultats des examens et évaluations des activités de surveillance du marché menées par les États membres, visés à l'article 88, paragraphe 8. |
2. Les informations visées au paragraphe 1 du présent article sont immédiatement transmises via le système électronique à toutes les autorités compétentes concernées et, le cas échéant, à l'organisme notifié qui a délivré le certificat conformément à l'article 51 pour le dispositif concerné, et sont accessibles aux États membres et à la Commission.
3. Les informations échangées entre États membres ne sont pas rendues publiques lorsque les activités de surveillance du marché et la coopération entre les États membres risqueraient de s'en ressentir.
CHAPITRE VIII
COOPÉRATION ENTRE LES ÉTATS MEMBRES, LE GROUPE DE COORDINATION EN MATIÈRE DE DISPOSITIFS MÉDICAUX, LES LABORATOIRES DE RÉFÉRENCE DE L'UE ET LES REGISTRES DE DISPOSITIFS
Article 96
Autorités compétentes
Les États membres désignent la ou les autorités compétentes chargées de la mise en œuvre du présent règlement. Ils veillent à ce que celles-ci disposent des pouvoirs, des ressources, de l'équipement et des connaissances nécessaires pour accomplir correctement les tâches qui leur incombent en vertu du présent règlement. Les États membres communiquent les noms et coordonnées des autorités compétentes à la Commission, qui en publie la liste.
Article 97
Coopération
1. Les autorités compétentes des États membres coopèrent les unes avec les autres ainsi qu'avec la Commission. La Commission veille à l'organisation des échanges d'informations nécessaires à une application uniforme du présent règlement.
2. Les États membres, avec le soutien de la Commission, participent, s'il y a lieu, aux initiatives mises au point au niveau international dans le but d'assurer la coopération des autorités chargées de la réglementation dans le domaine des dispositifs médicaux.
Article 98
Groupe de coordination en matière de dispositifs médicaux
Le GCDM institué conformément aux conditions et modalités visées aux articles 103 et 107 du règlement (UE) 2017/745 s'acquitte, avec le soutien de la Commission, conformément à l'article 104 du règlement (UE) 2017/745, des tâches qui lui incombent en vertu du présent règlement, ainsi que du règlement (UE) 2017/745.
Article 99
Tâches du GCDM
En vertu du présent règlement, les tâches du GCDM sont les suivantes:
a) |
contribuer à l'évaluation des candidats à la fonction d'organisme d'évaluation de la conformité et d'organisme notifié conformément aux dispositions établies au chapitre IV; |
b) |
fournir des conseils à la Commission, à sa demande, pour les questions concernant le groupe de coordination des organismes notifiés mis en place en vertu de l'article 45; |
c) |
contribuer à l'élaboration d'orientations pour une application efficace et harmonisée du présent règlement, notamment en ce qui concerne la désignation et la surveillance des organismes notifiés, l'application des exigences générales en matière de sécurité et de performances et la réalisation d'évaluations des performances par les fabricants, l'évaluation réalisée par les organismes notifiés et les activités de vigilance; |
d) |
contribuer à assurer le suivi permanent des progrès techniques, à évaluer si les exigences générales en matière de sécurité et de performances énoncées dans le présent règlement et dans le règlement (UE) 2017/745 permettent de garantir la sécurité et les performances des dispositifs, et contribuer ainsi à apprécier la nécessité de modifier l'annexe I du présent règlement; |
e) |
contribuer à l'élaboration de normes concernant les dispositifs et de spécifications communes; |
f) |
assister les autorités compétentes des États membres dans leurs activités de coordination, notamment dans les domaines de la classification des dispositifs et de la détermination de leur statut au regard de la réglementation, des études des performances, de la vigilance et de la surveillance du marché, y compris l'élaboration et le maintien d'un cadre pour un programme européen de surveillance du marché, dans un souci d'efficacité et d'harmonisation de la surveillance du marché dans l'Union, conformément à l'article 88; |
g) |
fournir des conseils, de sa propre initiative ou à la demande de la Commission, dans l'examen de toute question liée à l'application du présent règlement; |
h) |
contribuer à l'harmonisation des pratiques administratives relatives aux dispositifs dans les États membres. |
Article 100
Les laboratoires de référence de l'Union européenne
1. Pour des dispositifs particuliers ou une catégorie ou un groupe de dispositifs, ou pour des dangers particuliers liés à une catégorie ou un groupe de dispositifs, la Commission peut désigner, au moyen d'actes d'exécution, un ou plusieurs laboratoires de référence de l'Union européenne (ci-après dénommés «laboratoires de référence de l'UE») satisfaisant aux critères établis au paragraphe 4. La Commission ne désigne que des laboratoires de référence de l'UE pour lesquels une candidature a été présentée à cette fin par un État membre ou par le Centre commun de recherche de la Commission.
2. Dans les limites du champ couvert par la désignation, les laboratoires de référence de l'UE réalisent, selon les cas, les tâches suivantes:
a) |
vérifier les performances alléguées par le fabricant et la conformité de dispositifs de classe D avec les spécifications communes applicables, le cas échéant, ou avec d'autres solutions retenues par le fabricant pour garantir un niveau de sécurité et de performances au moins équivalent, conformément à l'article 48, paragraphe 3, troisième alinéa; |
b) |
réaliser les essais appropriés sur les échantillons de dispositifs fabriqués de classe D ou de lots de dispositifs de classe D, conformément à l'annexe IX, section 4.12, et à l'annexe XI, section 5.1; |
c) |
fournir une assistance scientifique et technique à la Commission, au GCDM, aux États membres et aux organismes notifiés en rapport avec l'application du présent règlement; |
d) |
fournir des conseils scientifiques sur l'état de l'art pour des dispositifs particuliers ou une catégorie ou un groupe de dispositifs; |
e) |
mettre en place et gérer un réseau de laboratoires de référence nationaux après consultation des autorités nationales et publier une liste répertoriant les laboratoires y participant et leurs tâches respectives; |
f) |
contribuer à l'élaboration des méthodes d'essai et d'analyse appropriées pour les procédures d'évaluation de la conformité et la surveillance du marché; |
g) |
collaborer avec les organismes notifiés à l'élaboration de bonnes pratiques pour l'application des procédures d'évaluation de la conformité; |
h) |
formuler des recommandations sur les matériaux de référence adéquats et les procédures de mesure de référence de rang supérieur; |
i) |
contribuer à l'élaboration de spécifications communes ainsi que de normes internationales; |
j) |
émettre des avis scientifiques sur consultation des organismes notifiés, conformément au présent règlement, et les publier via des moyens électroniques en tenant compte des dispositions nationales relatives à la confidentialité des données. |
3. À la demande d'un État membre, la Commission peut également désigner les laboratoires de référence de l'UE lorsque l'État membre en question souhaite faire appel à de tels laboratoires pour vérifier les performances alléguées par le fabricant et la conformité de dispositifs de classe C avec les spécifications communes applicables, le cas échéant, ou avec d'autres solutions retenues par le fabricant pour garantir un niveau de sécurité et de performances au moins équivalent.
4. Les laboratoires de référence de l'UE satisfont aux critères suivants:
a) |
ils disposent d'un personnel suffisant et qualifié doté des connaissances et de l'expérience adéquates dans le domaine des dispositifs médicaux de diagnostic in vitro pour lequel ils sont désignés; |
b) |
ils disposent des équipements et des matériaux de référence nécessaires pour exécuter les tâches qui leur incombent; |
c) |
ils disposent d'une connaissance adéquate des normes et des bonnes pratiques internationales; |
d) |
ils disposent d'une organisation et d'une structure administratives appropriées; |
e) |
ils garantissent que les membres de leur personnel respectent la confidentialité des informations et données obtenues dans l'exécution de leurs tâches; |
f) |
ils agissent dans l'intérêt général et de manière indépendante; |
g) |
ils garantissent que les membres de leur personnel n'ont pas d'intérêts financiers ou d'autre nature dans l'industrie des dispositifs médicaux de diagnostic in vitro susceptibles de compromettre leur impartialité, et que ceux-ci déclarent tout autre intérêt direct ou indirect détenu dans l'industrie des dispositifs médicaux de diagnostic in vitro et actualisent leur déclaration dès lors qu'un changement pertinent survient dans leur situation. |
5. Les laboratoires de référence de l'UE forment un réseau afin de coordonner et d'harmoniser leurs méthodes de travail pour ce qui est des essais et des évaluations. Il s'agit à cet effet notamment:
a) |
d'appliquer des méthodes, des procédures et des processus coordonnés; |
b) |
de convenir de l'utilisation des mêmes matériaux de référence et d'échantillons d'essai et de panels de séroconversion communs; |
c) |
de mettre en place des critères d'évaluation et d'interprétation communs; |
d) |
d'utiliser des protocoles d'essai communs et d'évaluer les résultats des essais en appliquant des méthodes d'évaluation normalisées et coordonnées; |
e) |
d'utiliser des rapports d'essai normalisés et coordonnés; |
f) |
de mettre au point, appliquer et maintenir un système d'évaluation par les pairs; |
g) |
d'organiser des tests d'évaluation de la qualité (notamment des vérifications réciproques de la qualité et de la comparabilité des résultats des essais); |
h) |
de convenir d'orientations, d'instructions, d'instructions de procédure ou de procédures opérationnelles standards communes; |
i) |
de coordonner l'introduction de méthodes d'essai pour les nouvelles technologies et de veiller à leur conformité avec des spécifications communes nouvelles ou modifiées; |
j) |
de réévaluer, à la demande d'un État membre ou de la Commission, l'état de l'art sur la base de résultats d'essais comparatifs ou en réalisant des études supplémentaires. |
6. Les laboratoires de référence de l'UE peuvent bénéficier d'une contribution financière de l'Union.
La Commission peut fixer, au moyen d'actes d'exécution, le montant d'une contribution financière de l'Union octroyée aux laboratoires de référence de l'UE ainsi que les modalités y afférentes, en tenant compte des objectifs en matière de protection de la santé et de la sécurité, de soutien à l'innovation et d'efficacité économique. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
7. Lorsqu'un organisme notifié ou un État membre demande à un laboratoire de référence de l'UE de lui apporter une assistance scientifique ou technique ou d'émettre un avis scientifique, une redevance peut être exigée pour couvrir tout ou partie des frais engagés par le laboratoire en question pour l'exécution de la tâche requise; celle-ci est fixée suivant des modalités prédéterminées et transparentes.
8. La Commission précise, au moyen d'actes d'exécution:
a) |
les modalités destinées à faciliter l'application du paragraphe 2 du présent article et les modalités permettant de garantir le respect des critères visés au paragraphe 4 du présent article; |
b) |
la structure et le montant des redevances visées au paragraphe 7 du présent article qui peuvent être exigées par un laboratoire de référence de l'UE pour la formulation d'un avis scientifique sur consultation des organismes notifiés et des États membres conformément au présent règlement, eu égard aux objectifs en matière de protection de la santé et de la sécurité des personnes, de soutien à l'innovation et d'efficacité économique. |
Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
9. Les laboratoires de référence de l'UE font l'objet de contrôles, y compris de visites sur place et d'audits, par la Commission dans le but de vérifier le respect des exigences établies par le présent règlement. S'il ressort desdits contrôles qu'un laboratoire de référence de l'UE ne respecte pas les exigences applicables eu égard à la mission pour laquelle il a été désigné, la Commission prend, au moyen d'actes d'exécution, des mesures appropriées, dont la limitation du champ couvert par la désignation ou la suspension ou la révocation de la désignation.
10. Les dispositions de l'article 107, paragraphe 1, du règlement (UE) 2017/745 s'appliquent au personnel des laboratoires de référence de l'UE.
Article 101
Registres de dispositifs et banques de données
La Commission et les États membres prennent toutes les mesures appropriées pour encourager la mise en place de registres et de banques de données pour des types de dispositifs donnés, en définissant des principes communs pour collecter des données comparables. Ces registres et banques de données contribuent à l'évaluation indépendante de la sécurité et des performances à long terme des dispositifs.
CHAPITRE IX
CONFIDENTIALITÉ, PROTECTION DES DONNÉES, FINANCEMENT ET SANCTIONS
Article 102
Confidentialité
1. Sauf disposition contraire du présent règlement et sans préjudice des dispositions et pratiques nationales en vigueur dans les États membres en matière de confidentialité, toutes les parties concernées par l'application du présent règlement respectent la confidentialité des informations et données obtenues dans l'exécution de leurs tâches de manière à protéger:
a) |
les données à caractère personnel conformément à l'article 103; |
b) |
les informations confidentielles de nature commerciale et des secrets d'affaires des personnes physiques ou morales, y compris les droits de propriété intellectuelle, sauf si l'intérêt public justifie la divulgation; |
c) |
l'application effective du présent règlement, notamment en ce qui concerne les inspections, les investigations ou les audits. |
2. Sans préjudice du paragraphe 1, les informations échangées à titre confidentiel entre les autorités compétentes et entre celles-ci et la Commission ne sont pas divulguées sans l'accord préalable de l'autorité dont elles émanent.
3. Les paragraphes 1 et 2 sont sans effet sur les droits et obligations de la Commission, des États membres et des organismes notifiés en matière d'échange d'informations et de diffusion de mises en garde, et sur les obligations d'information incombant aux personnes concernées en vertu du droit pénal.
4. La Commission et les États membres peuvent échanger des informations confidentielles avec les autorités de réglementation de pays tiers avec lesquels ils ont conclu des accords bilatéraux ou multilatéraux en matière de confidentialité.
Article 103
Protection des données
1. Les États membres appliquent la directive 95/46/CE au traitement des données à caractère personnel effectué dans les États membres en vertu du présent règlement.
2. Le règlement (CE) no 45/2001 s'applique au traitement des données à caractère personnel effectué par la Commission en vertu du présent règlement.
Article 104
Perception de redevances
1. Le présent règlement ne préjuge pas de la possibilité des États membres de prélever une redevance pour les activités prévues par le présent règlement, à condition que le montant de celle-ci soit fixé de manière transparente et conformément au principe de couverture des coûts.
2. Les États membres informent la Commission et les autres États membres, au moins trois mois avant leur mise en place, de la structure et du montant des redevances. La structure et le montant des redevances sont rendus publics sur demande.
Article 105
Financement des activités liées à la désignation et au contrôle des organismes notifiés
Les coûts liés aux activités d'évaluation conjointe sont à la charge de la Commission. La Commission établit, au moyen d'actes d'exécution, le niveau et la structure des frais remboursables ainsi que d'autres modalités d'application nécessaires. Ces actes d'exécution sont adoptés en conformité avec la procédure d'examen visée à l'article 107, paragraphe 3.
Article 106
Sanctions
Les États membres déterminent le régime des sanctions applicables aux violations des dispositions du présent règlement et prennent toutes les mesures nécessaires pour assurer leur mise en œuvre. Ces sanctions sont effectives, proportionnées et dissuasives. Les États membres notifient ce régime et ces mesures à la Commission au plus tard le 25 février 2022 et toute modification ultérieure les concernant dans les meilleurs délais.
CHAPITRE X
DISPOSITIONS FINALES
Article 107
Comité
1. La Commission est assistée par le comité «Dispositifs médicaux» institué en vertu de l'article 114 du règlement (UE) 2017/745. Ledit comité est un comité au sens du règlement (UE) no 182/2011.
2. Lorsqu'il est fait référence au présent paragraphe, l'article 4 du règlement (UE) no 182/2011 s'applique.
3. Lorsqu'il est fait référence au présent paragraphe, l'article 5 du règlement (UE) no 182/2011 s'applique.
Lorsque le comité n'émet aucun avis, la Commission n'adopte pas le projet d'acte d'exécution, et l'article 5, paragraphe 4, troisième alinéa, du règlement (UE) no 182/2011 s'applique.
4. Lorsqu'il est fait référence au présent paragraphe, l'article 8 du règlement (UE) no 182/2011, s'applique, en liaison avec l'article 4 ou l'article 5, selon le cas.
Article 108
Exercice de la délégation
1. Le pouvoir d'adopter des actes délégués conféré à la Commission est soumis aux conditions fixées au présent article.
2. Le pouvoir d'adopter des actes délégués visé à l'article 10, paragraphe 4, à l'article 17, paragraphe 4, à l'article 24, paragraphe 10, à l'article 51, paragraphe 6, et à l'article 66, paragraphe 8, est conféré à la Commission pour une période de cinq ans à compter du 25 mai 2017. La Commission élabore un rapport relatif à la délégation de pouvoir au plus tard neuf mois avant la fin de la période de cinq ans. La délégation de pouvoir est tacitement prorogée pour des périodes d'une durée identique, sauf si le Parlement européen ou le Conseil s'oppose à cette prorogation trois mois au plus tard avant la fin de chaque période.
3. La délégation de pouvoir visée à l'article 10, paragraphe 4, à l'article 17, paragraphe 4, à l'article 24, paragraphe 10, à l'article 51, paragraphe 6, et à l'article 66, paragraphe 8, peut être révoquée à tout moment par le Parlement européen ou le Conseil. La décision de révocation met fin à la délégation de pouvoir qui y est précisée. La révocation prend effet le jour suivant celui de la publication de ladite décision au Journal officiel de l'Union européenne ou à une date ultérieure qui est précisée dans ladite décision. Elle ne porte pas atteinte à la validité des actes délégués déjà en vigueur.
4. Avant l'adoption d'un acte délégué, la Commission consulte les experts désignés par chaque État membre, conformément aux principes définis dans l'accord interinstitutionnel du 13 avril 2016«Mieux légiférer».
5. Aussitôt qu'elle adopte un acte délégué, la Commission le notifie au Parlement européen et au Conseil simultanément.
6. Un acte délégué adopté en vertu de l'article 10, paragraphe 4, de l'article 17, paragraphe 4, de l'article 24, paragraphe 10, de l'article 51, paragraphe 6, et de l'article 66, paragraphe 8, n'entre en vigueur que si le Parlement européen ou le Conseil n'a pas exprimé d'objections dans un délai de trois mois à compter de la notification de cet acte au Parlement européen et au Conseil ou si, avant l'expiration de ce délai, le Parlement européen et le Conseil ont tous deux informé la Commission de leur intention de ne pas exprimer d'objections. Ce délai est prolongé de trois mois à l'initiative du Parlement européen ou du Conseil.
Article 109
Actes délégués distincts pour chaque délégation de pouvoir
La Commission adopte un acte délégué distinct pour chaque délégation de pouvoir prévue par le présent règlement.
Article 110
Dispositions transitoires
1. À compter du 26 mai 2022, toute publication d'une notification relative à un organisme notifié conformément à la directive 98/79/CE est invalidée.
2. Les certificats délivrés par des organismes notifiés conformément à la directive 98/79/CE avant le 25 mai 2017 conservent leur validité jusqu'à la fin de la période indiquée sur ces certificats, sauf pour les certificats délivrés conformément à l'annexe VI de la directive 98/79/CE, qui sont invalidés au plus tard le 27 mai 2024.
Les certificats délivrés par des organismes notifiés conformément à la directive 98/79/CE à partir du 25 mai 2017 sont invalidés au plus tard le 27 mai 2024.
3. Par dérogation à l'article 5 du présent règlement, un dispositif muni d'un certificat délivré conformément à la directive 98/79/CE et qui est valide en vertu du paragraphe 2 du présent article, ne peut être mis sur le marché ou mis en service que si, à compter de la date d'application du présent règlement, il continue de respecter ladite directive et pour autant qu'il n'y ait pas de changement significatif dans la conception et la finalité. Cependant, les exigences du présent règlement relatives à la surveillance après commercialisation, à la surveillance du marché, à la vigilance, à l'enregistrement des opérateurs économiques et des dispositifs, s'appliquent et remplacent les exigences correspondantes de ladite directive.
Sans préjudice du chapitre IV et du paragraphe 1 du présent article, l'organisme notifié qui a délivré le certificat visé au premier alinéa continue d'être responsable de la surveillance appropriée en ce qui concerne l'ensemble des exigences applicables relatives aux dispositifs qu'il a certifiés.
4. Les dispositifs légalement mis sur le marché conformément à la directive 98/79/CE avant le 26 mai 2022 et les dispositifs mis sur le marché à compter du 26 mai 2022 en vertu d'un certificat visé au paragraphe 2 du présent article peuvent continuer d'être mis à disposition sur le marché ou mis en service jusqu'au 27 mai 2025.
5. Par dérogation à la directive 98/79/CE, les dispositifs conformes au présent règlement peuvent être mis sur le marché avant le 26 mai 2022.
6. Par dérogation à la directive 98/79/CE, les organismes d'évaluation de la conformité conformes au présent règlement peuvent être désignés et notifiés avant le 26 mai 2022. Les organismes notifiés qui sont désignés et notifiés conformément au présent règlement peuvent mettre en œuvre les procédures d'évaluation de la conformité établies par celui-ci et délivrer des certificats conformément au présent règlement avant le 26 mai 2022.
7. Pour ce qui est des dispositifs faisant l'objet des procédures prévues à l'article 48, paragraphes 3 et 4, le paragraphe 5 du présent article s'applique, pour autant qu'il ait été procédé aux nominations nécessaires au sein du GCDM et des groupes d'experts et que les laboratoires de référence de l'UE aient été désignés.
8. Par dérogation à l'article 10, à l'article 12, paragraphe 1, points a) et b), et à l'article 15, paragraphe 5, de la directive 98/79/CE, les fabricants, les mandataires, les importateurs et les organismes notifiés qui, pendant la période commençant à la plus tardive des dates visées à l'article 113, paragraphe 3, point f), et se terminant dix-huit mois plus tard, se conforment à l'article 26, paragraphe 3, à l'article 28, paragraphe 1, et à l'article 51, paragraphe 5, du présent règlement, sont réputés se conformer aux dispositions législatives et réglementaires adoptées par les États membres en application de l'article 10, de l'article 12, paragraphe 1, points a) et b), et de l'article 15, paragraphe 5, de la directive 98/79/CE, comme prévu dans la décision 2010/227/UE.
9. Les autorisations accordées par les autorités compétentes des États membres conformément à l'article 9, paragraphe 12, de la directive 98/79/CE, conservent leur validité pour la durée indiquée sur ces autorisations.
10. Tant que la Commission n'a pas désigné, conformément à l'article 24, paragraphe 2, les entités d'attribution, GS1, HIBCC et ICCBBA sont considérées comme les entités d'attribution désignées.
Article 111
Évaluation
Au plus tard le 27 mai 2027, la Commission évalue l'application du présent règlement et établit un rapport d'évaluation sur les progrès réalisés en vue des objectifs qui y figurent, ainsi que sur les ressources nécessaires à la mise en œuvre de celui-ci. Une attention particulière est accordée à la traçabilité des dispositifs grâce à l'enregistrement de l'IUD, en vertu de l'article 24, par les opérateurs économiques, les établissements de santé et les professionnels de la santé. L'évaluation comporte en outre un examen de l'application de l'article 4.
Article 112
Abrogation
Sans préjudice de l'article 110, paragraphes 3 et 4, du présent règlement, et sans préjudice des obligations des États membres et des fabricants en ce qui concerne la vigilance et des obligations des fabricants en ce qui concerne la mise à disposition de la documentation, au titre de la directive 98/79/CE, ladite directive est abrogée avec effet à compter du 26 mai 2022, à l'exception:
a) |
de l'article 11, de l'article 12, paragraphe 1, point c), et de l'article 12, paragraphes 2 et 3, de la directive 98/79/CE, et des obligations relatives à la vigilance et aux études de performances prévues dans les annexes correspondantes, qui sont abrogés avec effet à compter de la plus tardive des dates visées à l'article 113, paragraphe 2, et à l'article 113, paragraphe 3, point f), du présent règlement; et |
b) |
de l'article 10, de l'article 12, paragraphe 1, points a) et b), et de l'article 15, paragraphe 5, de la directive 98/79/CE, et des obligations relatives à l'enregistrement des dispositifs et des opérateurs économiques et aux notifications de certificat prévues dans les annexes correspondantes, qui sont abrogés avec effet à compter d'une date postérieure de dix-huit mois à la plus tardive des dates visées à l'article 113, paragraphe 2, et à l'article 113, paragraphe 3, point f), du présent règlement. |
En ce qui concerne les dispositifs visés à l'article 110, paragraphes 3 et 4, du présent règlement, la directive 98/79/CE continue de s'appliquer jusqu'au 27 mai 2025 dans la mesure où cela est nécessaire à l'application desdits paragraphes.
La décision 2010/227/UE, adoptée en application des directives 90/385/CEE, 93/42/CEE et 98/79/CE, est abrogée avec effet à compter de la plus tardive des dates visées à l'article 113, paragraphe 2, et à l'article 113, paragraphe 3, point f), du présent règlement.
Les références faites à la directive abrogée s'entendent comme faites au présent règlement et sont à lire selon le tableau de correspondance figurant à l'annexe XV.
Article 113
Entrée en vigueur et date d'application
1. Le présent règlement entre en vigueur le vingtième jour suivant celui de sa publication au Journal officiel de l'Union européenne.
2. Il est applicable à partir du 26 mai 2022.
3. Par dérogation au paragraphe 2:
a) |
l'article 26, paragraphe 3, et l'article 51, paragraphe 5, s'appliquent dix-huit mois après la date la plus tardive des dates visées au point f); |
||||||||||||||||||||||||||||||||||||||||||||
b) |
les articles 31 à 46 et l'article 96 s'appliquent à compter du 26 novembre 2017. Cependant, entre cette date et le 26 mai 2022, les obligations incombant aux organismes notifiés en vertu des articles 31 à 46 ne s'appliquent qu'aux organismes qui présentent une demande de désignation conformément à l'article 34; |
||||||||||||||||||||||||||||||||||||||||||||
c) |
l'article 97 s'applique à compter du 26 mai 2018; |
||||||||||||||||||||||||||||||||||||||||||||
d) |
l'article 100 s'applique à compter du 25 novembre 2020; |
||||||||||||||||||||||||||||||||||||||||||||
e) |
pour les dispositifs de classe D, l'article 24, paragraphe 4, s'applique à compter du 26 mai 2023. Pour les dispositifs de classes B et C, l'article 24, paragraphe 4, s'applique à compter du 26 mai 2025. Pour les dispositifs de classe A, l'article 24, paragraphe 4, s'applique à compter du 26 mai 2027; |
||||||||||||||||||||||||||||||||||||||||||||
f) |
sans préjudice des obligations incombant à la Commission en vertu de l'article 34 du règlement (UE) 2017/745, si, en raison de circonstances qui n'étaient pas raisonnablement prévisibles lors de l'élaboration du plan visé à l'article 34, paragraphe 1, dudit règlement, Eudamed n'est pas pleinement opérationnelle le 26 mai 2022, les obligations et les exigences qui ont trait à Eudamed s'appliquent à compter d'une date postérieure de six mois à la date de publication de l'avis visé à l'article 34, paragraphe 3, dudit règlement. Les dispositions visées à la phrase précédente sont les suivantes:
Tant qu'Eudamed n'est pas pleinement fonctionnelle, les dispositions correspondantes de la directive 98/79/CEE et 93/42/CEE continuent de s'appliquer aux fins de satisfaire aux obligations énoncées dans les dispositions énumérées au premier alinéa du présent point en ce qui concerne l'échange d'informations, y compris et en particulier les informations relatives aux études des performances, les notifications dans le cadre de la vigilance, l'enregistrement des dispositifs et des opérateurs économiques et les notifications de certificats. |
||||||||||||||||||||||||||||||||||||||||||||
g) |
la procédure prévue à l'article 74 s'applique à compter du 26 mai 2029 sans préjudice de l'article 74, paragraphe 14; |
||||||||||||||||||||||||||||||||||||||||||||
h) |
l'article 110, paragraphe 10, est applicable à partir du 26 mai 2019. |
Le présent règlement est obligatoire dans tous ses éléments et directement applicable dans tout État membre.
ANNEXES
ANNEXE I
EXIGENCES GÉNÉRALES EN MATIÈRE DE SÉCURITÉ ET DE PERFORMANCES
CHAPITRE I
EXIGENCES GÉNÉRALES
1. |
Les dispositifs atteignent les performances prévues par leur fabricant et sont conçus et fabriqués de telle manière que, dans des conditions normales d'utilisation, ils soient adaptés à leur destination. Ils sont sûrs et efficaces et ne compromettent pas l'état clinique ou la sécurité des patients ni la sécurité ou la santé des utilisateurs ou, le cas échéant, d'autres personnes, étant entendu que les risques éventuels liés à leur utilisation constituent des risques acceptables au regard des bénéfices pour le patient et compatibles avec un niveau élevé de protection de la santé et de la sécurité, compte tenu de l'état de l'art généralement admis. |
||||||||||||
2. |
Les exigences de la présente annexe prévoyant qu'il convient de réduire les risques autant que possible signifient réduire les risques autant que possible sans altérer le rapport bénéfice/risque. |
||||||||||||
3. |
Les fabricants établissent, appliquent, documentent et maintiennent un système de gestion des risques. La gestion des risques s'entend comme un processus itératif continu concernant l'ensemble du cycle de vie d'un dispositif, qui doit périodiquement faire l'objet d'une mise à jour systématique. Lorsqu'ils assurent la gestion des risques, les fabricants
|
||||||||||||
4. |
Les mesures de maîtrise des risques adoptées par les fabricants pour la conception et la fabrication des dispositifs sont conformes aux principes de sécurité, compte tenu de l'état de l'art généralement admis. Pour réduire les risques, les fabricants gèrent ceux-ci de sorte que le risque résiduel associé à chaque danger ainsi que le risque résiduel global soient jugés acceptables. Lorsqu'ils choisissent les solutions les plus appropriées, les fabricants appliquent les principes suivants, dans l'ordre de priorité suivant:
Les fabricants informent les utilisateurs concernant tout risque résiduel. |
||||||||||||
5. |
Lorsqu'il s'agit d'éliminer ou de réduire les risques liés à une erreur d'utilisation, le fabricant:
|
||||||||||||
6. |
Les caractéristiques et les performances d'un dispositif ne sont pas altérées au point de mettre en danger la santé ou la sécurité du patient, de l'utilisateur et, le cas échéant, d'autres personnes pendant la durée de vie du dispositif, telle qu'elle est indiquée par le fabricant, lorsque le dispositif est soumis aux contraintes pouvant survenir dans des conditions normales d'utilisation et qu'il a été entretenu selon les instructions du fabricant. |
||||||||||||
7. |
Les dispositifs sont conçus, fabriqués et conditionnés de façon à ce que leurs caractéristiques et leurs performances pendant leur utilisation prévue ne soient pas altérées pendant le transport et le stockage, par exemple par des variations de température et d'humidité, en tenant compte des instructions et des informations fournies par le fabricant. |
||||||||||||
8. |
Tous les risques connus et prévisibles ainsi que tous les effets indésirables sont réduits au minimum et sont acceptables au regard des bénéfices potentiels évalués que présentent pour le patient et/ou l'utilisateur les performances prévues du dispositif dans des conditions normales d'utilisation. |
CHAPITRE II
EXIGENCES RELATIVES AUX PERFORMANCES, À LA CONCEPTION ET À LA FABRICATION
9. |
Caractéristiques en matière de performances |
||||||||||||||
9.1. |
Les dispositifs sont conçus et fabriqués de façon à être adaptés aux buts visés à l'article 2, point 2), tels qu'ils sont précisés par le fabricant, ainsi qu'aux performances compte tenu de l'état général de la technique généralement admis. Ils atteignent les performances alléguées par le fabricant, en particulier, s'il y a lieu:
|
||||||||||||||
9.2. |
Les caractéristiques de performance du dispositif restent inchangées pendant toute la durée de vie du dispositif, telle qu'elle est indiquée par le fabricant. |
||||||||||||||
9.3. |
Lorsque les performances des dispositifs dépendent de l'utilisation de matériaux d'étalonnage et/ou de contrôle, la traçabilité métrologique des valeurs assignées à ces matériaux est garantie par des procédures de mesure de référence adaptées et/ou des matériaux de référence adaptés de rang supérieur. S'il y a lieu, la traçabilité métrologique des valeurs attribuées aux matériaux d'étalonnage et de contrôle est garantie par des matériaux ou procédures de mesure de référence certifiés. |
||||||||||||||
9.4. |
Les caractéristiques et les performances des dispositifs sont vérifiées en particulier au cas où elles peuvent être affectées lorsque le dispositif est utilisé dans des conditions normales d'utilisation eu égard à sa destination, en ce qui concerne:
|
||||||||||||||
10. |
Propriétés chimiques, physiques et biologiques |
||||||||||||||
10.1. |
Les dispositifs sont conçus et fabriqués de manière à garantir que les caractéristiques et les exigences en matière de performance visées au chapitre I sont satisfaites. Une attention particulière est accordée à l'éventualité d'une dégradation des performances analytiques due à l'incompatibilité physique et/ou chimique entre les matériaux utilisés et les échantillons, l'analyte ou le marqueur (par exemple, tissus biologiques, cellules, liquides corporels ou micro-organismes), eu égard à la destination du dispositif. |
||||||||||||||
10.2. |
Les dispositifs sont conçus, fabriqués et conditionnés de manière à réduire au minimum le risque lié aux contaminants et aux résidus pour les patients, eu égard à la destination du dispositif, et pour les personnes intervenant dans le transport, le stockage et l'utilisation des dispositifs. Une attention particulière est accordée aux tissus exposés à ces contaminants et à ces résidus ainsi qu'à la durée et à la fréquence de l'exposition. |
||||||||||||||
10.3. |
Les dispositifs sont conçus et fabriqués de manière à réduire à un niveau aussi faible que raisonnablement possible les risques liés aux substances ou aux particules, y compris les débris dus à l'usure, les produits de dégradation et les résidus de transformation, susceptibles d'être libérés d'un dispositif. Une attention particulière est accordée aux substances carcinogènes, mutagènes ou reprotoxiques, conformément à l'annexe VI, partie 3, du règlement (CE) no 1272/2008 du Parlement européen et du Conseil, ainsi qu'aux substances ayant des propriétés perturbant le système endocrinien, pour lesquelles de probables effets graves sur la santé humaine ont été scientifiquement démontrés et qui ont été identifiées conformément à la procédure établie à l'article 59 du règlement (CE) no 1907/2006 du Parlement européen et du Conseil. |
||||||||||||||
10.4. |
Les dispositifs sont conçus et fabriqués de façon à réduire autant que possible les risques liés à la pénétration non intentionnelle de substances dans le dispositif, en tenant compte de la nature du dispositif et de l'environnement dans lequel il est destiné à être utilisé. |
||||||||||||||
11. |
Infection et contamination microbienne |
||||||||||||||
11.1. |
Les dispositifs et les procédés de fabrication y afférents sont conçus de manière à éliminer ou à réduire autant que possible le risque d'infection de l'utilisateur ou, le cas échéant, d'autres personnes. Leur conception:
|
||||||||||||||
11.2. |
Les dispositifs étiquetés comme étant stériles ou présentant un état microbien particulier sont conçus, fabriqués et conditionnés de manière à garantir que leur état stérile ou microbien soit préservé, dans les conditions de transport et de stockage spécifiées par le fabricant, jusqu'à ce que ce conditionnement soit ouvert au point d'utilisation, à moins que le conditionnement destiné à en préserver l'état stérile ou microbien soit endommagé. |
||||||||||||||
11.3. |
Les dispositifs étiquetés comme étant stériles sont traités, fabriqués, conditionnés et stérilisés grâce à des méthodes appropriées et validées. |
||||||||||||||
11.4. |
Les dispositifs destinés à être stérilisés sont fabriqués et conditionnés dans des conditions et des installations contrôlées et appropriées. |
||||||||||||||
11.5. |
Les systèmes de conditionnement destinés à des dispositifs non stériles garantissent l'intégrité et la propreté du produit et, lorsque ces dispositifs sont destinés à être stérilisés avant leur utilisation, réduisent au minimum le risque de contamination microbienne; le système de conditionnement est adapté à la méthode de stérilisation préconisée par le fabricant. |
||||||||||||||
11.6. |
L'étiquetage des dispositifs permet de distinguer les dispositifs identiques ou similaires placés sur le marché à la fois à l'état stérile et non stérile, parallèlement au symbole utilisé pour indiquer que les dispositifs sont stériles. |
||||||||||||||
12. |
Dispositifs contenant du matériel d'origine biologique Lorsque les dispositifs contiennent des tissus, des cellules et des substances d'origine animale, humaine ou microbienne, la sélection des sources, le traitement, la conservation, le contrôle et la manipulation de ces tissus, cellules et substances et les procédures de contrôle sont menés de manière à assurer la sécurité de l'utilisateur ou de toute autre personne. En particulier, la sécurité en ce qui concerne les agents microbiens et autres agents transmissibles est assurée par l'application de méthodes validées d'élimination ou d'inactivation au cours du processus de fabrication. Ces dispositions pourraient ne pas s'appliquer à certains dispositifs si l'activité de l'agent microbien et d'autres agents transmissibles fait partie intégrante de la destination du dispositif ou si un tel procédé d'élimination ou d'inactivation est susceptible d'altérer les performances du dispositif. |
||||||||||||||
13. |
Fabrication des dispositifs et interaction avec leur environnement |
||||||||||||||
13.1. |
Si le dispositif est destiné à être utilisé en combinaison avec d'autres dispositifs ou équipements, l'ensemble, y compris le système de raccordement, est sûr et n'altère pas les performances prévues des dispositifs. Toute restriction d'utilisation applicable à de telles combinaisons figure sur l'étiquette et/ou dans la notice d'utilisation. |
||||||||||||||
13.2. |
Les dispositifs sont conçus et fabriqués de manière à éliminer ou à réduire autant que possible:
|
||||||||||||||
13.3. |
Les dispositifs sont conçus et fabriqués de façon à réduire au minimum les risques d'incendie ou d'explosion dans des conditions normales d'utilisation et en condition de premier défaut. Une attention particulière est accordée aux dispositifs dont l'utilisation prévue implique une exposition à des substances inflammables ou explosives ou à des substances susceptibles de favoriser la combustion, ou une utilisation en association avec de telles substances. |
||||||||||||||
13.4. |
Les dispositifs sont conçus et fabriqués de manière à ce que toute opération de réglage, d'étalonnage et de maintenance puisse être réalisée en toute sécurité et de manière efficace. |
||||||||||||||
13.5. |
Les dispositifs qui sont destinés à être mis en œuvre avec d'autres dispositifs ou produits sont conçus et fabriqués de manière à ce que leur interopérabilité et leur compatibilité soient fiables et sûres. |
||||||||||||||
13.6. |
Les dispositifs sont conçus et fabriqués de manière à favoriser leur élimination sûre et l'élimination sûre des déchets associés par l'utilisateur ou toute autre personne. À cet effet, les fabricants recensent et expérimentent des procédures et des mesures permettant une élimination sûre de leurs dispositifs après utilisation. Ces procédures sont décrites dans la notice d'utilisation. |
||||||||||||||
13.7. |
L'échelle de mesure, de contrôle ou d'affichage (y compris les changements de couleur et autres indicateurs optiques) est conçue et fabriquée suivant des principes ergonomiques, en tenant compte de la destination du dispositif, des utilisateurs et des conditions d'environnement dans lesquelles les dispositifs sont destinés à être utilisés. |
||||||||||||||
14. |
Dispositifs ayant une fonction de mesurage |
||||||||||||||
14.1. |
Les dispositifs dont la fonction analytique primaire est le mesurage sont conçus et fabriqués de manière à garantir des performances analytiques appropriées, conformément à la section 9. point 1 a), eu égard à leur destination. |
||||||||||||||
14.2. |
Les mesures effectuées par les dispositifs ayant une fonction de mesurage sont exprimées en unités légales conformes aux dispositions de la directive 80/181/CEE du Conseil. |
||||||||||||||
15. |
Protection contre les rayonnements |
||||||||||||||
15.1. |
Les dispositifs sont conçus, fabriqués et conditionnés de façon à réduire autant que possible l'exposition des utilisateurs ou d'autres personnes aux rayonnements (irradiation intentionnelle ou non intentionnelle, rayonnements parasites ou diffus), d'une manière compatible avec la destination des dispositifs, sans restreindre l'application des doses appropriées spécifiées à des fins diagnostiques. |
||||||||||||||
15.2. |
Lorsque les dispositifs sont destinés à émettre des rayonnements dangereux ou potentiellement dangereux, ionisants et/ou non ionisants, ils sont, dans la mesure du possible:
|
||||||||||||||
15.3. |
La notice d'utilisation des dispositifs émettant des rayonnements dangereux ou potentiellement dangereux comporte des informations détaillées sur la nature des rayonnements émis ainsi que sur les moyens de protéger l'utilisateur, d'éviter les mauvaises utilisations et de réduire autant que possible et dans la mesure appropriée les risques inhérents à l'installation. Des informations sont également communiquées concernant les essais d'acceptation et de performances, les critères d'acceptation et la procédure de maintenance. |
||||||||||||||
16. |
Systèmes électroniques programmables — dispositifs comportant des systèmes électroniques programmables et logiciels qui sont des dispositifs à part entière |
||||||||||||||
16.1. |
Les dispositifs comportant des systèmes électroniques programmables, notamment des logiciels, ou les logiciels qui sont des dispositifs à part entière sont conçus de manière à garantir la répétabilité, la fiabilité et les performances eu égard à leur utilisation prévue. En condition de premier défaut, des moyens adéquats sont adoptés pour éliminer ou réduire autant que possible les risques qui en résultent ou la dégradation des performances. |
||||||||||||||
16.2. |
Pour les dispositifs qui comprennent des logiciels ou pour les logiciels qui sont des dispositifs à part entière, ces logiciels sont développés et fabriqués conformément à l'état de l'art compte tenu des principes du cycle de développement, de gestion des risques, y compris la sécurité de l'information, de vérification et de validation. |
||||||||||||||
16.3. |
Les logiciels visés à la présente section qui sont destinés à être utilisés en combinaison avec des plateformes informatiques mobiles sont conçus et fabriqués en tenant compte des caractéristiques spécifiques de la plateforme mobile (par exemple, taille et rapport de contraste de l'écran) et des facteurs externes liés à leur utilisation (variation du niveau sonore ou de la luminosité dans l'environnement). |
||||||||||||||
16.4. |
Le fabricant indique les exigences minimales concernant le matériel informatique, les caractéristiques des réseaux informatiques et les mesures de sécurité informatique, y compris la protection contre l'accès non autorisé, qui sont nécessaires pour faire fonctionner le logiciel comme prévu. |
||||||||||||||
17. |
Dispositifs raccordés à une source d'énergie ou équipés d'une source d'énergie |
||||||||||||||
17.1. |
Pour les dispositifs raccordés à une source d'énergie ou équipés d'une source d'énergie, en condition de premier défaut, des moyens adéquats sont adoptés pour éliminer ou réduire autant que possible les risques qui en résultent. |
||||||||||||||
17.2. |
Les dispositifs pour lesquels la sécurité du patient dépend d'une source d'énergie interne sont munis d'un moyen de vérification de l'état de celle-ci et comportent une mise en garde ou une indication appropriée au cas où l'alimentation en énergie devient critique. Au besoin, cette mise en garde ou indication intervient avant que l'alimentation en énergie ne devienne critique. |
||||||||||||||
17.3. |
Les dispositifs sont conçus et fabriqués de manière à réduire autant que possible les risques de perturbations électromagnétiques susceptibles d'affecter le fonctionnement du dispositif lui-même ou d'autres dispositifs ou équipements situés dans l'environnement prévu. |
||||||||||||||
17.4. |
Les dispositifs sont conçus et fabriqués de manière à garantir le niveau d'immunité intrinsèque contre les interférences électromagnétiques qui est approprié pour leur permettre de fonctionner comme prévu. |
||||||||||||||
17.5. |
Les dispositifs sont conçus et fabriqués de manière à éviter autant que possible les risques d'électrocution accidentelle des utilisateurs ou de toute autre personne dans des conditions normales d'utilisation des dispositifs et en condition de premier défaut, lorsque les dispositifs sont installés et entretenus conformément aux instructions du fabricant. |
||||||||||||||
18. |
Protection contre les risques mécaniques et thermiques |
||||||||||||||
18.1. |
Les dispositifs sont conçus et fabriqués de manière à protéger les utilisateurs et d'autres personnes contre les risques mécaniques. |
||||||||||||||
18.2. |
Les dispositifs ont une stabilité suffisante dans les conditions de fonctionnement prévues. Ils sont capables de résister aux contraintes inhérentes à l'environnement de fonctionnement prévu et de conserver cette résistance pendant leur durée de vie prévue, sous réserve du respect des exigences préconisées par le fabricant en matière de contrôle et de maintenance. |
||||||||||||||
18.3. |
Lorsqu'il existe des risques dus à la présence de pièces mobiles, des risques de rupture ou de détachement, ou des risques de fuite de substances, des moyens appropriés de protection sont prévus. Tout protecteur ou autre moyen de protection, notamment contre les éléments mobiles, inclus dans le dispositif est solidement fixé et ne gêne pas l'accès au dispositif dans les conditions normales de fonctionnement, ni n'entrave les opérations de maintenance de routine prévues par le fabricant. |
||||||||||||||
18.4. |
Les dispositifs sont conçus et fabriqués de manière à réduire au minimum les risques résultant des vibrations produites par les dispositifs, compte tenu du progrès technique et des moyens disponibles d'atténuation des vibrations, notamment à la source, sauf si les vibrations font partie des performances prévues. |
||||||||||||||
18.5. |
Les dispositifs sont conçus et fabriqués de manière à réduire au minimum les risques résultant des émissions sonores, compte tenu du progrès technique et des moyens disponibles de réduction du bruit, notamment à la source, sauf si les émissions sonores font partie des performances prévues. |
||||||||||||||
18.6. |
Les terminaux et les systèmes de raccordement à des sources d'électricité, de gaz et d'énergie hydraulique ou pneumatique qui doivent être manipulés par l'utilisateur ou d'autres personnes, sont conçus et fabriqués de manière à réduire au minimum tous les risques possibles. |
||||||||||||||
18.7. |
Les erreurs susceptibles d'être commises lors du montage et du remontage de certaines pièces avant ou pendant l'utilisation, et qui peuvent engendrer des risques, sont rendues impossibles par la conception et la construction de ces pièces ou, à défaut, par des indications figurant sur les pièces elles-mêmes et/ou sur leur enveloppe. Ces indications figurent aussi sur les éléments mobiles et/ou sur leur enveloppe lorsqu'il est nécessaire de connaître le sens du mouvement pour éviter un risque. |
||||||||||||||
18.8. |
Les parties accessibles des dispositifs (à l'exclusion des parties ou des zones destinées à fournir de la chaleur ou à atteindre une température donnée) et leur environnement n'atteignent pas des températures susceptibles de présenter un danger dans des conditions normales d'utilisation. |
||||||||||||||
19. |
Protection contre les risques émanant des dispositifs destinés aux autodiagnostics ou aux diagnostics près du patient |
||||||||||||||
19.1. |
Les dispositifs destinés aux autodiagnostics ou aux diagnostics près du patient sont conçus et fabriqués de manière à fonctionner conformément à leur destination compte tenu des aptitudes et des moyens dont disposent les utilisateurs auxquels ils sont destinés, ainsi que de l'influence des variations raisonnablement prévisibles de la maîtrise technique et de l'environnement desdits utilisateurs. Les informations et les instructions fournies par le fabricant sont faciles à comprendre et à appliquer par l'utilisateur auquel le dispositif est destiné afin d'interpréter correctement le résultat fourni par le dispositif et d'éviter toute information trompeuse. Dans le cas des diagnostics près du patient, les informations et les instructions fournies par le fabricant exposent clairement le niveau de formation, les qualifications et/ou l'expérience dont l'utilisateur doit disposer. |
||||||||||||||
19.2. |
Les dispositifs destinés aux autodiagnostics ou aux diagnostics près du patient sont conçus et fabriqués de manière:
|
||||||||||||||
19.3. |
Les dispositifs destinés aux autodiagnostics ou aux diagnostics près du patient prévoient, dans la mesure du possible, une procédure permettant à l'utilisateur auquel ils sont destinés:
|
CHAPITRE III
EXIGENCES RELATIVES AUX INFORMATIONS FOURNIES AVEC LE DISPOSITIF
20. |
Étiquetage et notice d'utilisation |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
20.1. |
Exigences générales relatives aux informations fournies par le fabricant Chaque dispositif est accompagné des informations nécessaires à l'identification de celui-ci et de son fabricant, ainsi que de toute information relative à la sécurité et aux performances utile à l'utilisateur ou à toute autre personne, le cas échéant. Ces informations peuvent figurer sur le dispositif lui-même, sur le conditionnement ou dans la notice d'utilisation et, si le fabricant dispose d'un site internet, sont mises à disposition et mises à jour sur le site internet; en outre:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
20.2. |
Informations figurant sur l'étiquette L'étiquette comporte toutes les informations suivantes:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
20.3. |
Informations figurant sur le conditionnement qui préserve l'état stérile d'un dispositif («conditionnement stérile») Les informations suivantes figurent sur le conditionnement stérile:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
20.4. |
Informations figurant dans la notice d'utilisation |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
20.4.1. |
La notice d'utilisation contient toutes les informations suivantes:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
20.4.2. |
En outre, la notice d'utilisation des dispositifs destinés aux autodiagnostics est conforme à l'ensemble des principes suivants:
|
ANNEXE II
DOCUMENTATION TECHNIQUE
La documentation technique et, le cas échéant, un résumé de celle-ci, que le fabricant doit élaborer, sont présentés de manière claire, organisée et non ambiguë, sous une forme facilement consultable, et comprennent en particulier les éléments énumérés dans la présente annexe.
1. |
DESCRIPTION ET SPÉCIFICATION DU DISPOSITIF, Y COMPRIS LES VARIANTES ET LES ACCESSOIRES |
||||||||||||||||||||||||||||||||||||||||||||
1.1. |
Description et spécification du dispositif
|
||||||||||||||||||||||||||||||||||||||||||||
1.2. |
Référence à des générations précédentes et similaires du dispositif
|
||||||||||||||||||||||||||||||||||||||||||||
2. |
INFORMATIONS DEVANT ÊTRE FOURNIES PAR LE FABRICANT Un jeu complet comprenant:
|
||||||||||||||||||||||||||||||||||||||||||||
3. |
INFORMATIONS SUR LA CONCEPTION ET LA FABRICATION |
||||||||||||||||||||||||||||||||||||||||||||
3.1. |
Informations sur la conception Les informations permettant de comprendre les étapes de la conception du dispositif comprennent:
|
||||||||||||||||||||||||||||||||||||||||||||
3.2. |
Informations sur la fabrication
|
||||||||||||||||||||||||||||||||||||||||||||
4. |
EXIGENCES GÉNÉRALES EN MATIÈRE DE SÉCURITÉ ET DE PERFORMANCES La documentation contient des informations permettant de démontrer la conformité avec les exigences générales en matière de sécurité et de performances établies à l'annexe I qui sont applicables au dispositif compte tenu de sa destination, y compris une justification, une validation et une vérification des solutions retenues pour satisfaire auxdites exigences. La démonstration de conformité contient aussi:
|
||||||||||||||||||||||||||||||||||||||||||||
5. |
ANALYSE BÉNÉFICE/RISQUE ET GESTION DES RISQUES La documentation contient des informations sur:
|
||||||||||||||||||||||||||||||||||||||||||||
6. |
VÉRIFICATION ET VALIDATION DU PRODUIT La documentation contient les résultats et les analyses critiques de l'ensemble des études et/ou des essais de vérification et de validation qui ont été effectués pour démontrer que le dispositif respecte les exigences du présent règlement, en particulier les exigences générales applicables en matière de sécurité et de performances. Cela inclut les éléments ci-après. |
||||||||||||||||||||||||||||||||||||||||||||
6.1. |
Informations sur les performances analytiques du dispositif |
||||||||||||||||||||||||||||||||||||||||||||
6.1.1. |
Type d'échantillon Cette section décrit les différents types d'échantillons qui peuvent être analysés, en incluant leur stabilité (par exemple, le stockage, s'il y a lieu, les conditions de transport de l'échantillon et, dans l'optique des méthodes d'analyse d'urgence, des informations sur le délai entre le prélèvement et l'analyse de l'échantillon), et les conditions de stockage (par exemple, la durée, les limites de température et les cycles de congélation/décongélation). |
||||||||||||||||||||||||||||||||||||||||||||
6.1.2. |
Caractéristiques en matière de performances analytiques |
||||||||||||||||||||||||||||||||||||||||||||
6.1.2.1. |
Exactitude de mesure
|
||||||||||||||||||||||||||||||||||||||||||||
6.1.2.2. |
Sensibilité analytique Cette section inclut des informations sur la conception et les résultats de l'étude. Elle contient une description du type d'échantillon et de sa préparation, notamment la matrice, les niveaux d'analytes et la manière dont ces niveaux ont été établis. Le nombre de réplicats testés pour chaque concentration est également fourni, de même qu'une description du calcul effectué pour déterminer la sensibilité de l'essai. |
||||||||||||||||||||||||||||||||||||||||||||
6.1.2.3. |
Spécificité analytique Cette section décrit les études sur l'interférence et la réactivité croisée menées en vue de déterminer la spécificité analytique lorsque d'autres substances ou agents sont présents dans l'échantillon. Des informations sont fournies sur l'évaluation des substances ou agents susceptibles de provoquer une interférence ou une réaction croisée lors de l'essai, le type de substance ou d'agent faisant l'objet de l'essai et sa concentration, le type d'échantillon, la concentration de l'essai sur l'analyse et les résultats. Les interférents et les substances ou agents provoquant une réaction croisée, qui varient de manière significative suivant le type et la conception de l'essai, peuvent provenir de sources exogènes ou endogènes telles que:
|
||||||||||||||||||||||||||||||||||||||||||||
6.1.2.4. |
Traçabilité métrologique des valeurs des matériaux d'étalonnage et de contrôle |
||||||||||||||||||||||||||||||||||||||||||||
6.1.2.5. |
Plage de mesure de l'essai Cette section inclut des informations sur la plage de mesure, qu'il s'agisse de systèmes de mesure linéaires ou non linéaires, y compris le seuil de détection, et décrit la manière dont la plage de mesure et le seuil de détection ont été établis. Ces informations incluent une description du type d'échantillon, le nombre d'échantillons, le nombre de réplicats et une description de la préparation de l'échantillon, dont des informations sur la matrice, les niveaux d'analytes et la manière dont ces niveaux ont été établis. Le cas échéant, une description de tout effet crochet à haute dose et les données à l'appui des étapes d'atténuation, telle que la dilution, sont ajoutées. |
||||||||||||||||||||||||||||||||||||||||||||
6.1.2.6. |
Définition de la valeur-seuil Cette section fournit un résumé des données analytiques comprenant une description de la conception de l'étude avec les méthodes de détermination de la valeur-seuil, par exemple:
|
||||||||||||||||||||||||||||||||||||||||||||
6.1.3. |
Rapport sur les performances analytiques visé à l'annexe XIII |
||||||||||||||||||||||||||||||||||||||||||||
6.2. |
Informations sur les performances cliniques et les preuves cliniques. Rapport sur l'évaluation des performances La documentation contient le rapport sur l'évaluation des performances qui, lui-même, inclut les rapports sur la validité scientifique, les performances analytiques et les performances cliniques visés à l'annexe XIII, ainsi qu'une évaluation de ces rapports. Les documents relatifs à l'étude des performances cliniques visée à l'annexe XIII, partie A, section 2 sont inclus dans la documentation technique et/ou leurs références complètes y sont mentionnées. |
||||||||||||||||||||||||||||||||||||||||||||
6.3. |
Stabilité (à l'exclusion de la stabilité des échantillons) Cette section décrit les études relatives à la durée de conservation en stock déclarée et à la stabilité à l'utilisation et pendant le transport. |
||||||||||||||||||||||||||||||||||||||||||||
6.3.1. |
Durée de conservation en stock déclarée Cette section fournit des informations sur les études de stabilité étayant la durée de conservation en stock déclarée pour le dispositif. Les essais sont effectués sur au moins trois lots différents fabriqués dans des conditions globalement équivalentes aux conditions normales de production. Les trois lots ne doivent pas obligatoirement être des lots consécutifs. Des études accélérées ou des données extrapolées à partir de données en temps réel sont acceptables pour déclarer une première durée de conservation en stock mais sont suivies par des études de stabilité en temps réel. Ces informations détaillées comprennent:
|
||||||||||||||||||||||||||||||||||||||||||||
6.3.2. |
Stabilité à l'utilisation Cette section fournit des informations sur les études de stabilité à l'utilisation d'un lot correspondant à l'utilisation normale du dispositif, que celle-ci soit réelle ou simulée. Cela peut inclure la stabilité en flacon ouvert et/ou, pour les instruments automatisés, la stabilité dans le dispositif. Dans le cas d'une instrumentation automatisée, si la stabilité de l'étalonnage est déclarée, les données justificatives sont incluses. Ces informations détaillées comprennent:
|
||||||||||||||||||||||||||||||||||||||||||||
6.3.3. |
Stabilité pendant le transport Cette section fournit des informations sur les études de stabilité pendant le transport d'un lot de dispositifs visant à évaluer la tolérance des dispositifs aux conditions de transport prévues. Les études sur le transport peuvent être effectuées dans des conditions réelles et/ou simulées et envisagent différentes conditions telles qu'un transport par une chaleur et/ou un froid extrême. Ces informations décrivent:
|
||||||||||||||||||||||||||||||||||||||||||||
6.4. |
Vérification et validation du logiciel La documentation contient les preuves de la validation du logiciel tel qu'il est utilisé dans le dispositif fini. Ces informations incluent en règle générale un résumé des résultats de l'ensemble de la vérification, de la validation et des essais réalisés en interne et applicables dans un environnement d'utilisation réel avant la libération finale. En outre, elles prennent en compte toutes les différentes configurations du matériel informatique et, le cas échéant, des différents systèmes d'exploitation figurant sur l'étiquette. |
||||||||||||||||||||||||||||||||||||||||||||
6.5. |
Informations supplémentaires requises dans des cas spécifiques
|
ANNEXE III
DOCUMENTATION TECHNIQUE RELATIVE À LA SURVEILLANCE APRÈS COMMERCIALISATION
La documentation technique relative à la surveillance après commercialisation, que le fabricant est tenu d'élaborer conformément aux articles 78 à 81, est présentée de manière claire, organisée et non ambiguë, sous une forme facilement consultable, et comprend les éléments visés dans la présente annexe.
1. |
Plan de surveillance après commercialisation établi conformément à l'article 79. Le fabricant démontre, dans un plan de surveillance après commercialisation, qu'il satisfait à l'obligation visée à l'article 78.
|
||||||||||||||||||||||||||||||||||||
2. |
Rapport périodique actualisé de sécurité visé à l'article 81 et rapport sur la surveillance après commercialisation visé à l'article 80. |
ANNEXE IV
DÉCLARATION DE CONFORMITÉ UE
La déclaration de conformité UE contient les informations suivantes:
1. |
le nom, la raison sociale ou la marque déposée, et, s'il a déjà été délivré, le numéro d'enregistrement unique visé à l'article 28 du fabricant et, le cas échéant, de son mandataire, et l'adresse de leur siège social à laquelle ils peuvent être joints et celle de leur lieu d'établissement; |
2. |
une attestation certifiant que la déclaration de conformité UE est établie sous la seule responsabilité du fabricant; |
3. |
l'IUD-ID de base visé à l'annexe VI, partie C; |
4. |
le nom et la dénomination commerciale du produit, le code du produit, le numéro dans le catalogue ou une autre référence non équivoque permettant l'identification et la traçabilité du dispositif faisant l'objet de la déclaration de conformité UE, telle qu'une photo, si nécessaire, ainsi que sa destination. À l'exception du nom ou de la dénomination commerciale du produit, les informations permettant l'identification et la traçabilité peuvent être contenues dans l'IUD-ID de base visé au point 3; |
5. |
la classe de risque du dispositif conformément aux règles établies à l'annexe VIII; |
6. |
une déclaration attestant que le dispositif faisant l'objet de la déclaration de conformité UE respecte le présent règlement et, le cas échéant, toute autre législation de l'Union applicable prévoyant l'établissement d'une déclaration de conformité UE; |
7. |
des références à toute spécification commune qui a été utilisée et par rapport à laquelle la conformité est déclarée; |
8. |
le cas échéant, le nom et le numéro d'identification de l'organisme notifié, une description de la procédure d'évaluation de la conformité suivie et la référence du ou des certificats délivrés; |
9. |
le cas échéant, des informations supplémentaires; |
10. |
Le lieu et la date de délivrance de la déclaration, le nom et la fonction du signataire ainsi que la mention de la personne pour le compte de laquelle ce dernier a signé, et la signature. |
ANNEXE V
MARQUAGE DE CONFORMITÉ CE
1 |
Le marquage CE est constitué des initiales «CE» selon le graphisme suivant: |

2 |
En cas de réduction ou d'agrandissement du marquage CE, les proportions telles qu'elles ressortent du graphisme gradué figurant ci-dessus sont respectées. |
3 |
Les différents éléments du marquage CE ont sensiblement la même dimension verticale, qui ne peut être inférieure à 5 mm. Il peut être dérogé à cette dimension minimale pour les dispositifs de petites dimensions. |
ANNEXE VI
INFORMATIONS À FOURNIR POUR L'ENREGISTREMENT DES DISPOSITIFS ET DES OPÉRATEURS ÉCONOMIQUES CONFORMÉMENT À L'ARTICLE 26, PARAGRAPHE 3, ET À L'ARTICLE 28, PRINCIPAUX ÉLÉMENTS DE DONNÉES À FOURNIR À LA BASE DE DONNÉES IUD AVEC L'IUD-ID CONFORMÉMENT À l'ARTICLE 25 ET SYSTÈME DIUD
PARTIE A
INFORMATIONS À FOURNIR LORS DE L'ENREGISTREMENT DES DISPOSITIFS ET DES OPÉRATEURS ÉCONOMIQUES CONFORMÉMENT À L'ARTICLE 26, PARAGRAPHE 3, ET À L'ARTICLE 28
Les fabricants ou, le cas échéant, leurs mandataires et, le cas échéant, les importateurs fournissent les informations visées à la section 1 et veillent à ce que les informations concernant leurs dispositifs visées à la section 2 soient complètes et exactes et mises à jour par la partie concernée.
1. |
Informations relatives à l'opérateur économique |
||||
1.1. |
Le type d'opérateur économique (fabricant, mandataire ou importateur); |
||||
1.2. |
le nom, l'adresse et les coordonnées de l'opérateur économique; |
||||
1.3. |
lorsque les informations sont communiquées par une tierce personne pour le compte de l'un des opérateurs économiques mentionnés à la section 1.1, le nom, l'adresse et les coordonnées de cette tierce personne; |
||||
1.4. |
le nom, l'adresse et les coordonnées de la ou des personnes chargées de veiller au respect de la réglementation visées à l'article 15. |
||||
2. |
Informations relatives au dispositif |
||||
2.1. |
L'IUD-ID de base; |
||||
2.2. |
le type, le numéro et la date d'expiration du certificat délivré par l'organisme notifié ainsi que le nom ou le numéro d'identification dudit organisme et le lien vers les informations figurant sur le certificat qui ont été entrées par l'organisme notifié dans le système électronique relatif aux organismes notifiés et aux certificats; |
||||
2.3. |
l'État membre dans lequel le dispositif a été ou sera mis sur le marché dans l'Union; |
||||
2.4. |
dans le cas des dispositifs de classe B, C ou D, les États membres dans lesquels le dispositif est ou sera mis à disposition; |
||||
2.5. |
présence de tissus, de cellules ou de leurs dérivés d'origine humaine (oui/non); |
||||
2.6. |
présence de tissus, de cellules ou de leurs dérivés d'origine animale visés dans le règlement (UE) no 722/2012 (oui/non); |
||||
2.7. |
présence de cellules ou de substances d'origine microbienne (oui/non); |
||||
2.8. |
la classe de risque du dispositif; |
||||
2.9. |
le cas échéant, le numéro d'identification unique de l'étude des performances; |
||||
2.10. |
dans le cas des dispositifs conçus et fabriqués par une autre personne physique ou morale visée à l'article 10, paragraphe 14, le nom, l'adresse et les coordonnées de cette personne physique ou morale; |
||||
2.11. |
dans le cas des dispositifs de classe C ou D, le résumé des caractéristiques de sécurité et des performances; |
||||
2.12. |
le statut du dispositif (sur le marché, plus mis sur le marché, rappelé, mesures correctives de sécurité mises en place); |
||||
2.13. |
l'indication que le dispositif est un dispositif «nouveau», le cas échéant. Un dispositif est considéré comme «nouveau» si:
|
||||
2.14. |
l'indication que le dispositif est destiné à l'autodiagnostic ou au diagnostic près du patient. |
PARTIE B
PRINCIPAUX ÉLÉMENTS DE DONNÉES À FOURNIR À LA BASE DE DONNÉES IUD AVEC L'IUD-ID CONFORMÉMENT AUX ARTICLES 25 ET 26
Le fabricant fournit à la base de données IUD l'IUD-ID et les informations suivantes relatives au fabricant et au dispositif:
1. |
la quantité par unité de conditionnement; |
2. |
l'IUD-ID de base visé à l'article 24, paragraphe 6, et tout IUD-ID supplémentaire; |
3. |
la manière selon laquelle la production du dispositif est contrôlée (date d'expiration ou date de fabrication, numéro de lot, numéro de série); |
4. |
le cas échéant, l'IUD-ID de l'unité d'utilisation (lorsqu'un IUD n'est pas indiqué sur l'étiquette du dispositif au niveau de son unité d'utilisation, un ID «unité d'utilisation» est attribué de manière à associer l'utilisation d'un dispositif à un patient); |
5. |
le nom et l'adresse du fabricant, tels qu'ils figurent sur l'étiquette; |
6. |
le numéro d'enregistrement unique délivré conformément à l'article 28, paragraphe 2; |
7. |
le cas échéant, le nom et l'adresse du mandataire, tels qu'ils figurent sur l'étiquette; |
8. |
le code de la nomenclature des dispositifs médicaux prévu à l'article 23; |
9. |
la classe de risque du dispositif; |
10. |
le cas échéant, le nom ou la dénomination commerciale; |
11. |
le cas échéant, le modèle du dispositif, la référence ou le numéro dans le catalogue; |
12. |
une description supplémentaire du produit (facultatif); |
13. |
le cas échéant, les conditions de stockage et/ou de manipulation, telles qu'elles sont indiquées sur l'étiquette ou dans la notice d'utilisation; |
14. |
le cas échéant, d'autres dénominations commerciales du dispositif; |
15. |
une mention précisant si le dispositif a été étiqueté comme un dispositif à usage unique (oui/non); |
16. |
le cas échéant, le nombre maximal de réutilisations; |
17. |
une mention précisant si le dispositif a été étiqueté comme stérile (oui/non); |
18. |
une mention précisant si une stérilisation est nécessaire avant utilisation (oui/non); |
19. |
une URL pour des informations supplémentaires, telles qu'une notice d'utilisation électronique (facultatif); |
20. |
le cas échéant, des mises en garde ou contre-indications importantes; |
21. |
le statut du dispositif (sur le marché, plus mis sur le marché, rappelé, mesures correctives de sécurité mises en place). |
PARTIE C
SYSTÈME IUD
1. |
Définitions Identification et saisie automatiques des données (AIDC) L'AIDC est une technologie utilisée pour procéder à la capture automatique de données. Les techniques concernées sont notamment les codes à barres, les cartes à puce, la biométrie et l'identification par radiofréquence (RFID). IUD-ID de base L'IUD-ID de base est le principal identifiant d'un modèle de dispositif. C'est l'ID attribuée au niveau de l'unité d'utilisation du dispositif. C'est la principale clé permettant d'introduire des informations dans la base de données IUD et il est mentionné sur les certificats et les déclarations de conformité UE. ID de l'unité d'utilisation L'ID de l'unité d'utilisation a pour objet d'associer l'utilisation d'un dispositif à un patient lorsqu'un IUD n'est pas indiqué sur l'étiquette d'un dispositif individuel au niveau de son unité d'utilisation, par exemple lorsque plusieurs unités du même dispositif sont conditionnées ensemble. Dispositif configurable Un dispositif configurable est un dispositif constitué de plusieurs composants que le fabricant peut assembler pour former diverses configurations. Ces composants individuels peuvent être des dispositifs à part entière. Configuration Une configuration est une combinaison d'éléments d'équipement, conforme aux instructions du fabricant, dont l'action conjointe en tant que dispositif permet d'atteindre la destination souhaitée. Cette combinaison peut être modifiée, adaptée ou personnalisée pour répondre à des besoins spécifiques. IUD-ID L'IUD-ID est un code numérique ou alphanumérique unique propre à un modèle de dispositif qui sert également de «clé d'accès» aux informations stockées dans une base de données IUD. Marquage en clair Le marquage en clair est une interprétation lisible des caractères d'information encodés dans le support IUD. Niveaux de conditionnement Les niveaux de conditionnement sont les différents niveaux de conditionnement d'un dispositif contenant une quantité fixe de dispositifs, tels qu'une boîte en carton ou caisse. Identifiant «production» (IUD-IP) L'IUD-IP est un code numérique ou alphanumérique unique identifiant l'unité de production d'un dispositif. Les différents types d'IUD-IP sont le numéro de série, le numéro de lot, l'identifiant de logiciel et la date de fabrication ou d'expiration ou ces deux types de date. Identification par radiofréquences (RFID) La RFID est une technologie qui utilise les ondes radio pour permettre l'échange de données entre un lecteur et un marqueur électronique apposé sur un objet à des fins d'identification. Conteneur de transport Un conteneur de transport est un conteneur dont la traçabilité est assurée selon un processus propre aux systèmes logistiques. Identifiant unique des dispositifs (IUD) L'IUD est une série de chiffres ou de lettres créée selon une norme d'identification et de codification internationale. Il permet l'identification formelle d'un dispositif donné sur le marché. Il se compose de l'IUD-ID et de l'IUD-IP. Le terme «unique» n'est pas réputé impliquer que différentes unités de production sont considérées comme une série. Support IUD Le support IUD est la manière dont l'IUD est communiqué grâce à l'AIDC et, le cas échéant, son marquage en clair. Parmi les supports IUD, on trouve notamment les codes à barres unidimensionnels ou linéaires, les codes à barres à deux dimensions/code QR, les identifiants RFID. |
||||||||||||||
2. |
Exigences générales |
||||||||||||||
2.1. |
L'apposition de l'IUD est une exigence supplémentaire; elle ne remplace aucune des autres exigences de marquage ou d'étiquetage énoncées à l'annexe I du présent règlement. |
||||||||||||||
2.2. |
Le fabricant attribue et maintient des IUD uniques pour ses dispositifs. |
||||||||||||||
2.3. |
Seul le fabricant peut placer l'IUD sur le dispositif ou son conditionnement. |
||||||||||||||
2.4. |
Seules les normes de codification prévues par les entités d'attribution désignées par la Commission en application de l'article 24, paragraphe 2 peuvent être utilisées. |
||||||||||||||
3. |
IUD |
||||||||||||||
3.1. |
Un IUD est attribué au dispositif proprement dit ou à son conditionnement. Les niveaux de conditionnement supérieurs ont leur propre IUD. |
||||||||||||||
3.2. |
Les conteneurs de transport sont exemptés de l'exigence de la section 3.1. Par exemple, un IUD n'est pas requis sur une unité logistique lorsqu'un professionnel de la santé commande des dispositifs multiples au moyen de l'IUD ou du numéro de modèle des dispositifs individuels et que le fabricant met ces dispositifs dans un conteneur en vue de leur transport ou de protéger les dispositifs conditionnés séparément, le conteneur (unité logistique) n'est pas soumis aux exigences en matière d'IUD. |
||||||||||||||
3.3. |
L'IUD se compose de deux parties: un IUD-ID et un IUD-IP. |
||||||||||||||
3.4. |
L'IUD-ID est unique pour chaque niveau de conditionnement du dispositif. |
||||||||||||||
3.5. |
Si un numéro de lot, un numéro de série, un identifiant de logiciel ou une date d'expiration apparaît sur l'étiquette, il fait partie de l'IUD-IP. Si l'étiquette comprend également une date de fabrication, celle-ci ne doit pas être incluse dans l'IUD-IP. Si l'étiquette comprend uniquement une date de fabrication, celle-ci fait office d'IUD-IP. |
||||||||||||||
3.6. |
Chaque composant qui est considéré comme un dispositif et est disponible en tant que tel dans le commerce se voit attribuer un IUD distinct, sauf si les composants font partie d'un dispositif configurable portant son propre IUD. |
||||||||||||||
3.7. |
Les trousses se voient attribuer et portent leurs propres IUD. |
||||||||||||||
3.8. |
Le fabricant attribue l'IUD à un dispositif conformément à la norme de codification applicable. |
||||||||||||||
3.9. |
Un nouvel IUD-ID est requis chaque fois qu'une modification est susceptible de susciter une erreur d'identification du dispositif et/ou une ambiguïté dans sa traçabilité. En particulier, toute modification de l'un des éléments de données suivants figurant dans la base de données IUD exige un nouvel IUD-ID:
|
||||||||||||||
3.10. |
Les fabricants qui reconditionnent et/ou réétiquettent des dispositifs en y apposant leur propre étiquette, gardent une trace de l'IUD du fabricant du dispositif d'origine. |
||||||||||||||
4. |
Support IUD |
||||||||||||||
4.1. |
Le support IUD (transcription AIDC et marquage en clair de l'IUD) est apposé sur l'étiquette et sur tous les niveaux de conditionnement supérieurs du dispositif. Les conteneurs de transport ne font pas partie des niveaux de conditionnement supérieurs. |
||||||||||||||
4.2. |
En cas d'espace limité sur le conditionnement de l'unité d'utilisation, le support IUD peut être apposé sur le niveau de conditionnement supérieur suivant. |
||||||||||||||
4.3. |
Pour les dispositifs à usage unique de classe A et de classe B conditionnés et étiquetés séparément, le support IUD ne doit pas obligatoirement apparaître sur le conditionnement mais sur un niveau de conditionnement supérieur, par exemple une boîte en carton contenant plusieurs conditionnements. Cependant, lorsque le professionnel de la santé n'est pas censé avoir accès, dans les cas de soins à domicile, au niveau de conditionnement supérieur, l'IUD est apposé sur le conditionnement. |
||||||||||||||
4.4. |
Pour les dispositifs exclusivement destinés à des points de vente au consommateur, les IUD-IP AIDC ne doivent pas obligatoirement apparaître sur le conditionnement au point de vente. |
||||||||||||||
4.5. |
Lorsque des supports AIDC autres que le support IUD font partie de l'étiquetage du produit, ce dernier est aisément identifiable. |
||||||||||||||
4.6. |
S'il est fait usage de codes à barres linéaires, l'IUD-ID et l'IUD-IP peuvent être concaténés ou non concaténés en deux codes à barres ou plus. Toutes les parties et tous les éléments du code à barres linéaire sont reconnaissables et identifiables. |
||||||||||||||
4.7. |
Si des contraintes importantes limitent l'utilisation de l'AIDC et du marquage en clair sur l'étiquette, seul l'AIDC doit y apparaître. Pour les dispositifs destinés à une utilisation en dehors des établissements de soins, par exemple pour les soins à domicile, le marquage en clair figure néanmoins sur l'étiquette, même s'il n'y a dès lors plus de place pour l'AIDC. |
||||||||||||||
4.8. |
Le marquage en clair est conforme aux règles de l'entité attribuant le code IUD. |
||||||||||||||
4.9. |
Si le fabricant recourt à la technologie RFID, un code à barres linéaire ou à deux dimensions conforme à la norme prévue par les entités d'attribution apparaît également sur l'étiquette. |
||||||||||||||
4.10. |
Les dispositifs réutilisables comportent un support IUD apposé sur le dispositif proprement dit. Les dispositifs réutilisables devant être nettoyés, désinfectés, stérilisés ou remis à neuf entre deux utilisations comportent un support IUD permanent qui reste lisible après chaque opération destinée à permettre l'utilisation ultérieure du dispositif, tout au long de sa durée de vie prévue. |
||||||||||||||
4.11. |
Le support IUD est lisible pendant l'utilisation normale et tout au long de la durée de vie prévue du dispositif. |
||||||||||||||
4.12. |
Si le support IUD peut être aisément lu ou scanné à travers le conditionnement du dispositif, il n'est pas nécessaire de l'apposer sur le conditionnement. |
||||||||||||||
4.13. |
Dans le cas de dispositifs finis unique composés de plusieurs parties qui doivent être assemblées avant la première utilisation, il suffit de placer le support IUD sur une seule partie de chaque dispositif. |
||||||||||||||
4.14. |
Le support IUD est apposé de façon que l'on puisse accéder à l'AIDC pendant le fonctionnement normal ou le stockage. |
||||||||||||||
4.15. |
Les supports de codes à barres comprenant à la fois un IUD-ID et un IUD-IP peuvent également comprendre des données essentielles pour le fonctionnement du dispositif ou d'autres données. |
||||||||||||||
5. |
Principes généraux de la base de données IUD |
||||||||||||||
5.1. |
La base de données IUD facilite l'utilisation de tous les principaux éléments de données qu'elle contient, visés à la partie B de la présente annexe. |
||||||||||||||
5.2. |
Les fabricants sont responsables de l'introduction initiale et de la mise à jour des données d'identification et des autres éléments de données concernant le dispositif dans la base de données IUD. |
||||||||||||||
5.3. |
Des méthodes/procédures appropriées sont appliquées pour valider les données fournies. |
||||||||||||||
5.4. |
Les fabricants vérifient périodiquement l'exactitude de toutes les données pertinentes relatives aux dispositifs qu'ils ont mis sur le marché, sauf en ce qui concerne ceux qui ne sont plus disponibles sur le marché. |
||||||||||||||
5.5. |
La présence de l'IUD-ID d'un dispositif dans la base de données IUD n'est pas interprétée comme signifiant que ce dispositif est conforme au présent règlement. |
||||||||||||||
5.6. |
La base de données permet d'établir un lien entre l'ensemble des niveaux de conditionnement du dispositif. |
||||||||||||||
5.7. |
Les données relatives à de nouveaux IUD-ID sont disponibles au moment où le dispositif est mis sur le marché. |
||||||||||||||
5.8. |
Les fabricants mettent à jour les données correspondantes enregistrées dans la base de données IUD dans un délai de trente jours après que des modifications ont été apportées à un élément qui n'exige pas de nouvel IUD-ID. |
||||||||||||||
5.9. |
Dans toute la mesure du possible, la base de données IUD applique des normes acceptées à l'échelle internationale pour l'introduction et la mise à jour des données. |
||||||||||||||
5.10. |
L'interface utilisateur de la base de données IUD est disponible dans toutes les langues officielles de l'Union. Les champs de texte libre sont toutefois réduits au minimum afin de limiter les besoins de traduction. |
||||||||||||||
5.11. |
Les données relatives aux dispositifs qui ne sont plus disponibles sur le marché sont conservées dans la base de données IUD. |
||||||||||||||
6. |
Règles applicables à certains types de dispositifs |
||||||||||||||
6.1. |
Dispositifs réutilisables faisant partie de trousses et qui doivent être nettoyés, désinfectés, stérilisés ou remis à neuf entre deux utilisations |
||||||||||||||
6.1.1. |
L'IUD de ces dispositifs est apposé sur le dispositif et est aisément lisible après chaque opération destinée à permettre la réutilisation du dispositif. |
||||||||||||||
6.1.2. |
Les caractéristiques de l'IUD-IP, telles que le numéro de série ou de lot, sont définies par le fabricant. |
||||||||||||||
6.2. |
Dispositifs consistant en un logiciel |
||||||||||||||
6.2.1. |
Critères d'attribution de l'IUD L'IUD est attribué au niveau du système du logiciel. Seuls les logiciels qui sont disponibles en soi dans le commerce et ceux qui constituent un dispositif à part entière sont soumis à cette exigence. L'identification du logiciel est considérée comme un mécanisme de contrôle de la fabrication et est indiquée dans l'IUD-IP. |
||||||||||||||
6.2.2. |
Un nouvel IUD-ID est exigé en cas de modification portant sur:
Ces modifications comprennent des algorithmes nouveaux ou modifiés ou peuvent concerner les structures de la base de données, la plateforme d'exploitation, l'architecture, de nouvelles interfaces utilisateurs ou de nouveaux canaux d'interopérabilité. |
||||||||||||||
6.2.3. |
Les révisions mineures d'un logiciel exigent un nouvel IUD-IP et non un nouvel IUD-ID: Les révisions mineures sont généralement associées à la suppression de bogues, à l'amélioration de la facilité d'utilisation qui n'ont pas d'objectifs de sûreté, à des correctifs de sécurité ou à l'efficacité. Les révisions mineures de logiciel sont identifiées par une forme d'identifiant «fabricant» spécifique. |
||||||||||||||
6.2.4. |
Critères d'application de l'IUD pour les logiciels
|
ANNEXE VII
EXIGENCES AUXQUELLES DOIVENT SATISFAIRE LES ORGANISMES NOTIFIÉS
1. |
EXIGENCES ORGANISATIONNELLES ET GÉNÉRALES |
||||||||||||||||||||||||||||||||||||||||
1.1. |
Statut juridique et structure organisationnelle |
||||||||||||||||||||||||||||||||||||||||
1.1.1. |
Les organismes notifiés sont établis conformément au droit national des États membres ou au droit d'un pays tiers avec lequel l'Union a conclu un accord à cet égard. Leur personnalité et leur statut juridiques sont entièrement documentés. Cette documentation inclut des informations sur la propriété et les personnes physiques ou morales exerçant un contrôle sur les organismes notifiés. |
||||||||||||||||||||||||||||||||||||||||
1.1.2. |
Si l'organisme notifié est une entité juridique faisant partie d'une organisation plus vaste, les activités de cette organisation, sa structure organisationnelle et sa gouvernance ainsi que sa relation avec l'organisme notifié sont clairement documentées. Dans ce cas, les exigences de la section 1.2 s'appliquent à la fois à l'organisme notifié et à l'organisation dont il fait partie. |
||||||||||||||||||||||||||||||||||||||||
1.1.3. |
Si l'organisme notifié détient, entièrement ou partiellement, des entités juridiques établies dans un État membre ou dans un pays tiers ou est détenu par une autre entité juridique, les activités et les responsabilités de ces entités ainsi que leurs relations sur le plan juridique et opérationnel avec l'organisme notifié sont clairement définies et documentées. Le personnel de ces entités qui mène des activités d'évaluation de la conformité au titre du présent règlement est soumis aux exigences applicables du présent règlement. |
||||||||||||||||||||||||||||||||||||||||
1.1.4. |
La structure organisationnelle, la répartition des responsabilités, les liens hiérarchiques et le fonctionnement de l'organisme notifié sont tels qu'ils garantissent la fiabilité des activités d'évaluation de conformité menées par l'organisme notifié et de leurs résultats. |
||||||||||||||||||||||||||||||||||||||||
1.1.5. |
L'organisme notifié documente clairement sa structure organisationnelle et les fonctions, les responsabilités et l'autorité des cadres supérieurs et des autres membres du personnel qui peuvent avoir une influence sur les activités d'évaluation de la conformité menées par l'organisme notifié et sur leurs résultats. |
||||||||||||||||||||||||||||||||||||||||
1.1.6. |
L'organisme notifié indique quels sont les cadres supérieurs qui détiennent l'autorité et la responsabilité générales pour chacun des éléments suivants:
|
||||||||||||||||||||||||||||||||||||||||
1.2. |
Indépendance et impartialité |
||||||||||||||||||||||||||||||||||||||||
1.2.1. |
Les organismes notifiés sont des organismes tiers qui sont indépendants du fabricant du dispositif pour lequel ils mènent les activités d'évaluation de la conformité. Les organismes notifiés sont également indépendants de tout autre opérateur économique ayant un intérêt dans le dispositif ainsi que de tout concurrent du fabricant. Cela n'exclut pas la possibilité pour un organisme notifié de mener des activités d'évaluation de la conformité pour des fabricants concurrents. |
||||||||||||||||||||||||||||||||||||||||
1.2.2. |
Les organismes notifiés sont organisés et fonctionnent de façon à garantir l'indépendance, l'objectivité et l'impartialité de leurs activités. Les organismes notifiés documentent et appliquent une structure et des procédures permettant de garantir l'impartialité et d'encourager et appliquer les principes d'impartialité dans l'ensemble de leur organisation, du personnel et des activités d'évaluation. Ces procédures permettent de détecter toute situation qui pourrait donner lieu à un conflit d'intérêts, y compris la participation à des services de conseil dans le domaine des dispositifs avant l'entrée en fonctions auprès de l'organisme notifié, ainsi que de mener une enquête à ce sujet et de trouver une solution. L'enquête, son résultat et la solution sont documentés. |
||||||||||||||||||||||||||||||||||||||||
1.2.3. |
L'organisme notifié, ses cadres supérieurs et le personnel chargé d'exécuter les tâches d'évaluation de la conformité:
|
||||||||||||||||||||||||||||||||||||||||
1.2.4. |
La participation à des services de conseil dans le domaine des dispositifs avant l'entrée en fonctions auprès d'un organisme notifié est pleinement documentée au moment de l'entrée en fonctions et les conflits d'intérêts potentiels sont examinés et résolus conformément à la présente annexe. Les membres du personnel qui ont été auparavant employés par un client donné ou lui ont fourni des services de conseils dans le domaine des dispositifs avant de prendre leurs fonctions auprès d'un organisme notifié ne sont pas désignés, pendant une période de trois ans, pour mener des activités d'évaluation de la conformité pour ce client en particulier ou pour des entreprises faisant partie du même groupe que ce client. |
||||||||||||||||||||||||||||||||||||||||
1.2.5. |
L'impartialité des organismes notifiés, de leurs cadres supérieurs et de leur personnel effectuant l'évaluation est garantie. Le niveau de rémunération des cadres supérieurs d'un organisme notifié et du personnel effectuant l'évaluation ainsi que des sous-traitants participant aux activités d'évaluation ne dépend pas des résultats des évaluations. Les organismes notifiés mettent à la disposition du public les déclarations d'intérêts de leurs cadres supérieurs. |
||||||||||||||||||||||||||||||||||||||||
1.2.6. |
Si un organisme notifié appartient à une entité ou une institution publique, l'indépendance et l'absence de conflit d'intérêts entre l'autorité responsable des organismes notifiés et/ou l'autorité compétente, d'une part, et l'organisme notifié, d'autre part, sont garanties et documentées. |
||||||||||||||||||||||||||||||||||||||||
1.2.7. |
Les organismes notifiés veillent à ce que les activités de leurs filiales, de leurs sous-traitants ou de tout organisme associé, y compris les activités de leurs propriétaires, ne portent pas atteinte à leur indépendance, à leur impartialité ou à l'objectivité de leurs activités d'évaluation de la conformité et le prouvent par des documents. |
||||||||||||||||||||||||||||||||||||||||
1.2.8. |
Les organismes notifiés agissent conformément à un ensemble de conditions cohérentes, justes et raisonnables, en tenant compte des intérêts des petites et moyennes entreprises au sens de la recommandation 2003/361/CE pour ce qui est des redevances. |
||||||||||||||||||||||||||||||||||||||||
1.2.9. |
Les exigences énoncées dans la présente section n'excluent en aucun cas les échanges d'informations techniques et d'orientations en matière de réglementation entre un organisme notifié et un fabricant introduisant une demande d'évaluation de la conformité. |
||||||||||||||||||||||||||||||||||||||||
1.3. |
Confidentialité |
||||||||||||||||||||||||||||||||||||||||
1.3.1. |
Les organismes notifiés disposent de procédures documentées pour veiller à ce que leur personnel, leurs comités, leurs filiales, leurs sous-traitants et tout organisme associé ou le personnel d'organismes externes respectent la confidentialité des informations auxquelles ils accèdent durant l'exercice de leurs activités d'évaluation de la conformité, sauf lorsque leur divulgation est requise par la loi. |
||||||||||||||||||||||||||||||||||||||||
1.3.2. |
Le personnel d'un organisme notifié est lié par le secret professionnel dans l'exercice de ses fonctions en vertu du présent règlement ou de toute disposition de la législation nationale lui donnant effet, sauf à l'égard des autorités responsables des organismes notifiés, des autorités compétentes pour les dispositifs dans les États membres ou de la Commission. Les droits de propriété sont protégés. Les organismes notifiés disposent de procédures documentées conformément aux exigences de la présente section. |
||||||||||||||||||||||||||||||||||||||||
1.4. |
Responsabilité |
||||||||||||||||||||||||||||||||||||||||
1.4.1. |
Les organismes notifiés souscrivent pour leurs activités d'évaluation de la conformité une assurance de responsabilité civile appropriée, à moins que cette responsabilité ne soit couverte par l'État membre concerné sur la base de la législation nationale ou que l'évaluation de la conformité ne soit réalisée directement par cet État membre. |
||||||||||||||||||||||||||||||||||||||||
1.4.2. |
La couverture et la valeur financière globale de l'assurance de responsabilité civile correspondent à l'ampleur et au champ géographique des activités de l'organisme notifié et sont proportionnées au profil de risque des dispositifs certifiés par l'organisme notifié. L'assurance couvre les cas dans lesquels l'organisme notifié pourrait être obligé d'annuler ou de suspendre des certificats ou de les assortir de restrictions. |
||||||||||||||||||||||||||||||||||||||||
1.5. |
Exigences en matière financière Les organismes notifiés disposent des ressources financières requises pour mener leurs activités d'évaluation de la conformité dans le cadre du champ couvert par la désignation et les opérations commerciales connexes. Ils documentent et fournissent la preuve de leur capacité financière et de leur viabilité économique à long terme, en tenant compte, le cas échéant, des circonstances spécifiques liées à une phase initiale de démarrage. |
||||||||||||||||||||||||||||||||||||||||
1.6. |
Participation aux activités de coordination |
||||||||||||||||||||||||||||||||||||||||
1.6.1. |
Les organismes notifiés participent aux activités de normalisation pertinentes et aux activités de leur groupe de coordination visé à l'article 49 du règlement (UE) 2017/745, ou veillent à ce que leur personnel effectuant l'évaluation en soit informé, et veillent également à ce que leur personnel effectuant l'évaluation et leurs décideurs aient connaissance de l'ensemble de la législation applicable, des documents d'orientation et des documents sur les bonnes pratiques adoptés dans le cadre du présent règlement. |
||||||||||||||||||||||||||||||||||||||||
1.6.2. |
Les organismes notifiés tiennent compte des documents d'orientation et des documents sur les bonnes pratiques. |
||||||||||||||||||||||||||||||||||||||||
2. |
EXIGENCES EN MATIÈRE DE GESTION DE LA QUALITÉ |
||||||||||||||||||||||||||||||||||||||||
2.1. |
Les organismes notifiés établissent, documentent, mettent en œuvre, mettent à jour et exploitent un système de gestion de la qualité approprié à la nature, au domaine et à l'ampleur de leurs activités d'évaluation de la conformité et permettant de favoriser et de démontrer le respect constant des exigences du présent règlement. |
||||||||||||||||||||||||||||||||||||||||
2.2. |
Le système de gestion de la qualité d'un organisme notifié porte, au minimum, sur les aspects suivants:
Lorsque les documents existent dans plusieurs langues, l'organisme notifié s'assure et vérifie que leur contenu est identique. |
||||||||||||||||||||||||||||||||||||||||
2.3. |
Les cadres supérieurs des organismes notifiés font en sorte que le système de gestion de la qualité est compris, appliqué et mis à jour dans l'ensemble de l'organisation de l'organisme notifié, y compris les filiales et sous-traitants participant aux activités d'évaluation de la conformité au titre du présent règlement. |
||||||||||||||||||||||||||||||||||||||||
2.4. |
Les organismes notifiés exigent que l'ensemble du personnel s'engage formellement, par une signature ou un procédé équivalent, à respecter les procédures définies par les organismes notifiés. Cet engagement porte sur des aspects ayant trait à la confidentialité et à l'indépendance par rapport à des intérêts commerciaux et autres, ainsi qu'à tout lien antérieur ou actuel avec des clients. Les membres du personnel sont invités à faire une déclaration écrite attestant de leur engagement vis-à-vis des principes de confidentialité, d'indépendance et d'impartialité. |
||||||||||||||||||||||||||||||||||||||||
3. |
EXIGENCES EN MATIÈRE DE RESSOURCES |
||||||||||||||||||||||||||||||||||||||||
3.1. |
Généralités |
||||||||||||||||||||||||||||||||||||||||
3.1.1. |
Les organismes notifiés sont en mesure d'accomplir toutes les tâches qui leur incombent au titre du présent règlement avec la plus haute intégrité professionnelle et la compétence requise dans le domaine spécifique, qu'ils exécutent eux-mêmes ces tâches ou que celles-ci soient exécutées pour leur compte et sous leur responsabilité. En particulier, les organismes notifiés disposent du personnel suffisant et possèdent l'ensemble des équipements, installations et compétences nécessaires pour accomplir de façon adéquate les tâches techniques, scientifiques et administratives liées aux activités d'évaluation de la conformité pour lesquelles ils ont été désignés, ou ont accès à de tels équipements, installations et compétences. Cette exigence suppose que, en toutes circonstances et pour chaque procédure d'évaluation de la conformité et chaque type de dispositifs pour lequel ils ont été désignés, les organismes notifiés disposent en permanence d'un personnel administratif, technique et scientifique en nombre suffisant et doté d'une expérience et de connaissances liées aux dispositifs concernés et aux technologies correspondantes. Ce personnel est en nombre suffisant pour que l'organisme notifié concerné puisse exécuter les tâches d'évaluation de la conformité, y compris l'évaluation de la fonctionnalité médicale, des évaluations des performances, ainsi que des performances et de la sécurité des dispositifs pour lesquels il a été désigné par rapport aux exigences du présent règlement, notamment celles de l'annexe I. Les compétences cumulées d'un organisme notifié sont telles qu'elles lui permettent d'évaluer les types de dispositifs pour lesquels il a été désigné. L'organisme notifié dispose de compétences internes suffisantes pour procéder à une évaluation critique des évaluations réalisées par des experts externes. Les tâches qu'un organisme notifié n'est pas autorisé à sous-traiter figurent à la section 4.1. Le personnel participant à la gestion de l'exercice des activités d'un organisme notifié dans le domaine de l'évaluation de la conformité dispose de connaissances appropriées pour mettre en place et exploiter un système permettant de sélectionner le personnel effectuant l'évaluation et la vérification, de vérifier ses compétences, de lui délivrer les autorisations, de répartir ses tâches, d'organiser sa formation initiale et permanente, d'attribuer ses fonctions à ce personnel et de procéder à des contrôles pour s'assurer que le personnel qui prend en charge et effectue les activités d'évaluation et de vérification a les compétences requises pour exécuter les tâches qu'on attend de lui. Les organismes notifiés désignent, parmi leurs cadres supérieurs, au moins une personne physique qui a la responsabilité générale de l'ensemble des activités d'évaluation de la conformité des dispositifs. |
||||||||||||||||||||||||||||||||||||||||
3.1.2. |
Les organismes notifiés veillent à ce que le personnel participant aux activités d'évaluation de la conformité maintienne son niveau de qualification et d'expertise, en mettant en œuvre un système d'échange d'expérience et un programme d'éducation et de formation permanentes. |
||||||||||||||||||||||||||||||||||||||||
3.1.3. |
Les organismes notifiés documentent clairement l'étendue et les limites des fonctions et des responsabilités ainsi que le niveau des autorisations octroyées au personnel, y compris les sous-traitants et les experts externes, participant aux activités d'évaluation de la conformité et informe ce personnel en conséquence. |
||||||||||||||||||||||||||||||||||||||||
3.2. |
Critères de qualification du personnel |
||||||||||||||||||||||||||||||||||||||||
3.2.1. |
Les organismes notifiés établissent et documentent les critères de qualification et les procédures de sélection et d'autorisation des personnes participant aux activités d'évaluation de la conformité, notamment en termes de connaissances, d'expérience et d'autres compétences requises, ainsi que la formation initiale et permanente requise. Les critères de qualification se rapportent aux différentes fonctions du processus d'évaluation de la conformité, telles que l'audit, l'évaluation ou le test des produits, l'examen de la documentation technique, la prise de décision et la libération des lots, ainsi qu'aux dispositifs, aux technologies et aux secteurs, tels que la biocompatibilité, la stérilisation, l'autodiagnostic et le diagnostic près du patient, les diagnostics compagnons et l'évaluation des performances, relevant du champ couvert par la désignation. |
||||||||||||||||||||||||||||||||||||||||
3.2.2. |
Les critères de qualification visés à la section 3.2.1 font référence au champ couvert par la désignation d'un organisme notifié conformément à la description du champ utilisée par l'État membre pour la notification visée à l'article 38, paragraphe 3, et présentent un niveau de détail suffisant pour les qualifications requises dans les subdivisions de la description du champ. Des critères de qualification spécifiques sont définis au moins pour l'évaluation portant sur:
|
||||||||||||||||||||||||||||||||||||||||
3.2.3. |
Les membres du personnel chargés d'établir des critères de qualification et d'autoriser d'autres membres du personnel à exécuter des activités d'évaluation de la conformité spécifiques sont employés par l'organisme notifié lui-même et ne sont ni des experts externes ni des sous-traitants. Ce personnel possède des connaissances et une expérience attestées dans l'ensemble des domaines suivants:
|
||||||||||||||||||||||||||||||||||||||||
3.2.4. |
Les organismes notifiés disposent en permanence d'un personnel possédant une expertise clinique pertinente et employé si possible par les organismes notifiés eux-mêmes. Ce personnel participe à l'ensemble du processus décisionnel et du processus d'évaluation d'un organisme notifié pour:
|
||||||||||||||||||||||||||||||||||||||||
3.2.5. |
Le personnel chargé d'effectuer les examens relatifs à un produit (examinateurs de produits), par exemple les examens de la documentation technique ou l'examen de type incluant des aspects tels que l'évaluation des performances, la sécurité biologique, la stérilisation et la validation du logiciel, possède l'ensemble des qualifications attestées suivantes:
|
||||||||||||||||||||||||||||||||||||||||
3.2.6. |
Le personnel chargé d'effectuer les audits du système de gestion de la qualité mis en place par le fabricant (auditeurs sur place) possède l'ensemble des qualifications attestées suivantes:
|
||||||||||||||||||||||||||||||||||||||||
3.2.7. |
Les membres du personnel assumant la responsabilité générale des examens finaux et de la prise de décision en matière de certification sont employés par l'organisme notifié lui-même et ne sont ni des experts externes ni des sous-traitants. Ce personnel possède, à titre collectif, des connaissances attestées et une expérience étendue dans l'ensemble des domaines suivants:
|
||||||||||||||||||||||||||||||||||||||||
3.3. |
Documentation relative à la qualification, à la formation et à l'autorisation du personnel |
||||||||||||||||||||||||||||||||||||||||
3.3.1. |
Les organismes notifiés ont mis en place une procédure afin de documenter de façon complète la qualification de chaque membre du personnel participant aux activités d'évaluation de la conformité et le respect des critères de qualification établis à la section 3.2. Lorsque, dans des cas exceptionnels, le respect des critères de qualification établis à la section 3.2 ne peut être entièrement prouvé, l'organisme notifié justifie auprès de l'autorité responsable des organismes notifiés l'autorisation des membres du personnel concernés à exécuter les activités spécifiques d'évaluation de la conformité. |
||||||||||||||||||||||||||||||||||||||||
3.3.2. |
Pour l'ensemble de son personnel visé aux sections 3.2.3 à 3.2.7, les organismes notifiés établissent et tiennent à jour:
|
||||||||||||||||||||||||||||||||||||||||
3.4. |
Sous-traitants et experts externes |
||||||||||||||||||||||||||||||||||||||||
3.4.1. |
Sans préjudice de la section 3.2, les organismes notifiés peuvent sous-traiter certaines parties clairement définies d'une activité d'évaluation de la conformité. La sous-traitance de l'ensemble de l'audit des systèmes de gestion de la qualité ou des examens relatifs au produit n'est pas autorisée; une partie de ces activités peut toutefois être menée par des sous-traitants et des auditeurs et experts externes au nom de l'organisme notifié. L'organisme notifié en question assume l'entière responsabilité d'être en mesure d'apporter la preuve que les sous-traitants et experts ont les compétences pour accomplir leurs tâches spécifiques et de prendre toute décision sur la base de l'évaluation réalisée par un sous-traitant, ainsi que des activités réalisées en son nom par des sous-traitants et des experts. Les organismes notifiés ne peuvent pas sous-traiter les activités suivantes:
|
||||||||||||||||||||||||||||||||||||||||
3.4.2. |
Lorsqu'un organisme notifié sous-traite certaines activités d'évaluation de la conformité à une organisation ou à une personne physique, il applique une politique de sous-traitance décrivant les conditions dans lesquelles celle-ci peut avoir lieu et veille à ce que:
Toute sous-traitance ou consultation de personnes externes est documentée de manière appropriée, ne fait intervenir aucun intermédiaire et fait l'objet d'un accord écrit concernant, entre autres, la confidentialité et les conflits d'intérêts. L'organisme notifié concerné assume l'entière responsabilité des tâches réalisées en son nom par des sous-traitants. |
||||||||||||||||||||||||||||||||||||||||
3.4.3. |
Lorsqu'il fait appel à des sous-traitants ou à des experts externes dans le cadre d'une évaluation de la conformité, en particulier en ce qui concerne les technologies ou les dispositifs nouveaux, l'organisme notifié concerné possède des compétences internes dans chaque type de produit pour lequel il est désigné, qui lui permettent de diriger l'ensemble de l'évaluation de la conformité, de vérifier l'adéquation et la validité des avis d'experts et de prendre des décisions quant à la certification. |
||||||||||||||||||||||||||||||||||||||||
3.5. |
Surveillance des compétences, formation et échange d'expérience |
||||||||||||||||||||||||||||||||||||||||
3.5.1. |
Les organismes notifiés établissent des procédures pour l'évaluation initiale et la surveillance permanente des compétences, des activités d'évaluation de la conformité et des performances de l'ensemble du personnel interne et externe et des sous-traitants participant à des activités d'évaluation de la conformité. |
||||||||||||||||||||||||||||||||||||||||
3.5.2. |
Les organismes notifiés font périodiquement le bilan des compétences de leur personnel, recensent les besoins en formation et établissent un plan de formation afin de maintenir le niveau de qualification et de connaissance requis de chacun des membres du personnel. Dans le cadre de ce bilan, ils vérifient au minimum que le personnel:
|
||||||||||||||||||||||||||||||||||||||||
4. |
EXIGENCES RELATIVES AU PROCESSUS |
||||||||||||||||||||||||||||||||||||||||
4.1. |
Généralités Les organismes notifiés ont mis en place des processus documentés et des procédures suffisamment détaillées pour la réalisation de chacune des activités d'évaluation de la conformité pour lesquelles ils sont désignés, qui vont des activités préalables à la demande jusqu'à la prise de décision et à la surveillance et compte tenu, au besoin, des spécificités respectives des dispositifs. Les exigences énoncées aux sections 4.3, 4.4, 4.7 et 4.8 sont respectées dans le cadre des activités internes des organismes notifiés et ne sont pas sous-traitées. |
||||||||||||||||||||||||||||||||||||||||
4.2. |
Devis et activités préalables à la demande Les organismes notifiés:
|
||||||||||||||||||||||||||||||||||||||||
4.3. |
Examen de la demande et contrat Les organismes notifiés exigent une demande formelle signée par un fabricant ou un mandataire, contenant toutes les informations et déclarations du fabricant requises par les procédures d'évaluation de la conformité visées aux annexes IX à XI. Le contrat entre un organisme notifié et un fabricant prend la forme d'un accord écrit signé par les deux parties. Il est conservé par l'organisme notifié. Ce contrat contient des conditions et des obligations précises permettant à l'organisme notifié d'agir comme le prescrit le présent règlement, y compris l'obligation pour le fabricant d'informer l'organisme notifié des rapports issus de la vigilance, le droit pour l'organisme notifié de suspendre ou d'annuler des certificats qu'il a délivrés, ou de les assortir de restrictions, et le devoir pour l'organisme notifié de remplir les obligations qui lui incombent en matière d'information. L'organisme notifié dispose de procédures documentées pour examiner les demandes, portant sur les aspects suivants:
Le résultat de chaque examen d'une demande est documenté. Le rejet ou le retrait d'une demande est notifié dans le système électronique visé à l'article 52 et l'information en la matière est accessible aux autres organismes notifiés. |
||||||||||||||||||||||||||||||||||||||||
4.4. |
Répartition des ressources Les organismes notifiés disposent de procédures documentées pour veiller à ce que toutes les activités d'évaluation de la conformité soient réalisées par du personnel dûment qualifié et autorisé et ayant une expérience suffisante de l'évaluation des dispositifs, systèmes et processus et de la documentation connexe faisant l'objet de l'évaluation de la conformité. Pour chaque demande, l'organisme notifié détermine les ressources nécessaires et désigne une personne physique chargée de veiller à ce que l'évaluation de cette demande soit réalisée dans le respect des procédures applicables et à ce que les ressources appropriées, notamment en termes de personnel, soient mobilisées pour chacune des tâches de l'évaluation. La répartition des tâches qui doivent être exécutées dans le cadre de l'évaluation de la conformité et toute modification ultérieure de celle-ci est documentée. |
||||||||||||||||||||||||||||||||||||||||
4.5. |
Activités d'évaluation de la conformité |
||||||||||||||||||||||||||||||||||||||||
4.5.1. |
Généralités Les organismes notifiés et leur personnel accomplissent les activités d'évaluation de la conformité avec toute l'intégrité professionnelle et la compétence technique et scientifique requises dans les domaines concernés. Les organismes notifiés disposent de l'expertise, d'installations et de procédures documentées suffisantes pour mener avec efficacité les activités d'évaluation de la conformité pour lesquelles ils sont désignés, compte tenu des exigences pertinentes énoncées aux annexes IX à XI, et notamment les suivantes:
Le cas échéant, l'organisme notifié tient compte des spécifications communes, des documents d'orientation et des documents sur les bonnes pratiques disponibles ainsi que des normes harmonisées, même si le fabricant ne prétend pas s'y être conformé. |
||||||||||||||||||||||||||||||||||||||||
4.5.2. |
Audits du système de gestion de la qualité
|
||||||||||||||||||||||||||||||||||||||||
4.5.3. |
Vérification du produit Évaluation de la documentation technique En ce qui concerne l'évaluation de la documentation technique visée à l'annexe IX, chapitre II, les organismes notifiés disposent de l'expertise, d'installations et de procédures documentées suffisantes portant sur les éléments suivants:
Examen de type En ce qui concerne l'examen de type des dispositifs conformément à l'annexe X, les organismes notifiés disposent de procédures documentées ainsi que de l'expertise et d'installations suffisantes, notamment la capacité nécessaire pour:
Vérification par contrôle et essai de chaque lot de produit Les organismes notifiés:
|
||||||||||||||||||||||||||||||||||||||||
4.5.4. |
Évaluation de l'évaluation des performances L'évaluation, par les organismes notifiés, des procédures et de la documentation porte sur les résultats des recherches dans la documentation et l'ensemble des validations, vérifications et essais effectués ainsi que sur les conclusions tirées, et elle inclut en règle générale des éléments de réflexion concernant l'utilisation d'autres matériaux ou substances et tient compte du conditionnement et de la stabilité du dispositif fini, notamment de sa durée de conservation en stock. Lorsqu'aucun nouvel essai n'a été effectué par un fabricant ou lorsqu'on s'est écarté des procédures, l'organisme notifié concerné fait un examen critique approprié de la justification avancée par le fabricant. Les organismes notifiés ont mis en place des procédures documentées pour examiner les procédures et la documentation du fabricant relatives à l'évaluation des performances, à la fois pour l'évaluation initiale de la conformité et sur une base permanente. Les organismes notifiés examinent et valident les procédures et la documentation du fabricant et vérifient qu'elles traitent de manière adéquate des éléments suivants:
Les procédures visées au deuxième alinéa tiennent compte des spécifications communes, documents d'orientation et documents sur les bonnes pratiques disponibles. Les évaluations faites par les organismes notifiés des évaluations des performances prévues à l'annexe XIII portent sur:
Pour ce qui est des données issues des études des performances comprises dans l'évaluation des performances, l'organisme notifié concerné veille à ce que les conclusions tirées par le fabricant soient valables au regard du plan d'étude des performances qui a été approuvé. L'organisme notifié veille à ce que l'évaluation des performances traite de manière adéquate des exigences applicables en matière de sécurité et de performances énoncées à l'annexe I, cadre avec les exigences en matière de gestion des risques, soit réalisée conformément à l'annexe XIII et trouve un écho approprié dans les informations fournies à propos du dispositif. |
||||||||||||||||||||||||||||||||||||||||
4.5.5. |
Procédures spéciales Les organismes notifiés disposent de procédures documentées ainsi que de l'expertise et d'installations suffisantes pour les procédures visées à l'annexe IX, section 5, pour lesquels ils sont désignés. Dans le cas des diagnostics compagnons, les organismes notifiés ont mis en place des procédures documentées qui visent à satisfaire aux exigences du présent règlement pour ce qui est de consulter l'Agence européenne des médicaments (EMA) ou une autorité compétente en matière de médicaments lorsqu'ils procèdent à l'évaluation de ce type de dispositif. |
||||||||||||||||||||||||||||||||||||||||
4.6. |
Rapports Les organismes notifiés:
Le rapport d'un organisme notifié:
|
||||||||||||||||||||||||||||||||||||||||
4.7. |
Examen final Avant de prendre une décision finale, les organismes notifiés:
|
||||||||||||||||||||||||||||||||||||||||
4.8. |
Décision et certification Les organismes notifiés disposent de procédures documentées pour la prise de décision, y compris en ce qui concerne la répartition des responsabilités en matière de délivrance, de suspension ou d'annulation de certificats ou l'imposition de restrictions. Ces procédures comprennent les exigences de notification établies au chapitre V du présent règlement. Les procédures permettent à l'organisme notifié concerné:
|
||||||||||||||||||||||||||||||||||||||||
4.9. |
Modifications Les organismes notifiés ont mis en place des procédures documentées et des arrangements contractuels avec les fabricants concernant les obligations d'information du fabricant et l'évaluation des modifications apportées:
Les procédures et arrangements contractuels visés au premier alinéa comportent des mesures permettant de contrôler la portée des modifications visées à l'alinéa en question. Conformément à ses procédures documentées, l'organisme notifié concerné:
|
||||||||||||||||||||||||||||||||||||||||
4.10. |
Activités de surveillance et contrôle après certification Les organismes notifiés disposent de procédures documentées:
Lorsqu'un fabricant ou les autorités compétentes lui communiquent que des produits font l'objet d'une vigilance, l'organisme notifié concerné décide laquelle des options suivantes choisir:
En ce qui concerne les audits de surveillance chez les fabricants, les organismes notifiés disposent de procédures documentées pour:
Si cela figure parmi les conditions dont est assortie la certification, l'organisme notifié:
|
||||||||||||||||||||||||||||||||||||||||
4.11. |
Recertification Les organismes notifiés ont mis en place des procédures documentées concernant les examens liés à la recertification et au renouvellement des certificats. Tous les cinq ans au moins, il est prévu de recertifier les systèmes de gestion de la qualité qui ont été approuvés ou de renouveler les certificats d'évaluation UE de la documentation technique et les certificats d'examen UE de type. Les organismes notifiés disposent de procédures documentées concernant le renouvellement des certificats d'évaluation UE de la documentation technique et des certificats d'examen UE de type, et ces procédures exigent du fabricant en question qu'il présente un résumé des modifications et des données scientifiques récentes concernant le dispositif, notamment:
Les organismes notifiés disposent de procédures documentées pour évaluer les informations visées au deuxième alinéa et accordent une attention particulière aux données cliniques issues des activités de surveillance après commercialisation et de SPAC entreprises depuis la certification ou la recertification précédente, y compris les actualisations des rapports d'évaluation des performances établis par les fabricants. Pour statuer sur la recertification, l'organisme notifié concerné utilise les mêmes méthodes et principes que pour la décision de certification initiale. Au besoin, des formulaires distincts sont établis pour la recertification compte tenu des mesures à prendre pour la certification, telles que la demande et l'examen de la demande. |
ANNEXE VIII
RÈGLES DE CLASSIFICATION
1. |
RÈGLES D'APPLICATION |
||||||||||||||||||||||||||
1.1. |
Les règles de classification s'appliquent en fonction de la destination des dispositifs. |
||||||||||||||||||||||||||
1.2. |
Si le dispositif en question est destiné à être utilisé en combinaison avec un autre dispositif, les règles de classification s'appliquent séparément à chacun des dispositifs. |
||||||||||||||||||||||||||
1.3. |
Les accessoires d'un dispositif médical de diagnostic in vitro sont classés en soi, indépendamment des dispositifs avec lesquels ils sont utilisés. |
||||||||||||||||||||||||||
1.4. |
Le logiciel commandant un dispositif ou agissant sur son utilisation relève de la même classe que le dispositif. Si le logiciel est indépendant de tout autre dispositif, il est classé en soi. |
||||||||||||||||||||||||||
1.5. |
Les matériaux d'étalonnage destinés à être utilisés avec un dispositif relèvent de la même classe que le dispositif. |
||||||||||||||||||||||||||
1.6. |
Les matériaux de contrôle ayant des valeurs assignées quantitatives ou qualitatives destinés à un analyte spécifique ou à des analytes multiples relèvent de la même classe que le dispositif. |
||||||||||||||||||||||||||
1.7. |
Le fabricant prend en considération toutes les règles de classification et de mise en œuvre afin d'établir la classification correcte du dispositif. |
||||||||||||||||||||||||||
1.8. |
Lorsqu'un fabricant établit plusieurs destinations pour un dispositif et que, par conséquent, le dispositif en question relève de plus d'une classe, celui-ci est classé dans la classe la plus élevée. |
||||||||||||||||||||||||||
1.9. |
Si plusieurs règles de classification s'appliquent au même dispositif, la règle qui s'applique est celle qui classe le dispositif dans la classe la plus élevée. |
||||||||||||||||||||||||||
1.10. |
Chacune des règles de classification s'applique aux premiers essais, aux essais de confirmation et aux essais supplémentaires. |
||||||||||||||||||||||||||
2. |
RÈGLES DE CLASSIFICATION |
||||||||||||||||||||||||||
2.1. |
Règle 1 Les dispositifs destinés à être utilisés pour les objectifs suivants relèvent de la classe D:
|
||||||||||||||||||||||||||
2.2. |
Règle 2 Les dispositifs destinés à être utilisés pour déterminer les groupes sanguins, l'incompatibilité sanguine foeto-maternelle ou les groupes tissulaires afin de garantir la compatibilité immunologique du sang, des composants sanguins, des cellules, des tissus ou des organes destinés à la transfusion, à la transplantation ou à l'administration de cellules relèvent de la classe C, sauf lorsqu'ils sont destinés à la détermination d'un des marqueurs suivants:
auquel cas ils relèvent de la classe D. |
||||||||||||||||||||||||||
2.3. |
Règle 3 Les dispositifs relèvent de la classe C s'ils sont destinés:
|
||||||||||||||||||||||||||
2.4. |
Règle 4
|
||||||||||||||||||||||||||
2.5. |
Règle 5 Les dispositifs suivants relèvent de la classe A:
|
||||||||||||||||||||||||||
2.6. |
Règle 6 Les dispositifs non concernés par les règles de classification ci-dessus relèvent de la classe B. |
||||||||||||||||||||||||||
2.7. |
Règle 7 Les dispositifs destinés à des contrôles sans valeur assignée quantitative ou qualitative relèvent de la classe B. |
ANNEXE IX
ÉVALUATION DE LA CONFORMITÉ SUR LA BASE D'UN SYSTÈME DE GESTION DE LA QUALITÉ ET DE L'ÉVALUATION DE LA DOCUMENTATION TECHNIQUE
CHAPITRE I
SYSTÈME DE GESTION DE LA QUALITÉ
1. |
Le fabricant établit, documente et applique un système de gestion de la qualité tel qu'il est décrit à l'article 10, paragraphe 8, et en maintient l'efficacité tout au long du cycle de vie des dispositifs concernés. Le fabricant veille à l'application du système de gestion de la qualité tel qu'il est décrit à la section 2 et est soumis à l'audit prévu aux sections 2.3 et 2.4 et à la surveillance prévue à la section 3. |
||||||||||||||||||||||||||||||||||
2. |
Évaluation du système de gestion de la qualité |
||||||||||||||||||||||||||||||||||
2.1. |
Le fabricant soumet une demande d'évaluation de son système de gestion de la qualité à un organisme notifié. La demande comprend:
|
||||||||||||||||||||||||||||||||||
2.2. |
L'application du système de gestion de la qualité garantit la conformité avec le présent règlement. L'ensemble des éléments, des exigences et des dispositions adoptés par le fabricant pour son système de gestion de la qualité figurent dans une documentation tenue de manière systématique et ordonnée sous la forme d'un manuel de la qualité et de politiques et de procédures écrites, telles que des programmes, des plans et des enregistrements relatifs à la qualité. De plus, la documentation à présenter pour l'évaluation du système de gestion de la qualité comprend notamment une description adéquate des éléments suivants:
De plus, les fabricants permettent aux organismes notifiés l'accès à la documentation technique visée aux annexes II et III. |
||||||||||||||||||||||||||||||||||
2.3. |
Audit L'organisme notifié effectue un audit du système de gestion de la qualité pour déterminer s'il satisfait aux exigences visées à la section 2.2. Dans les cas où le fabricant applique une norme harmonisée ou une spécification commune ayant trait à un système de gestion de la qualité, l'organisme notifié évalue la conformité avec ces normes et spécifications. Sauf raisons dûment justifiées, l'organisme notifié présume qu'un système de gestion de la qualité qui satisfait aux normes harmonisées ou spécifications communes pertinentes est conforme aux exigences couvertes par lesdites normes ou spécifications. L'équipe d'audit de l'organisme notifié comprend au moins un membre ayant déjà l'expérience d'évaluations de la technologie concernée, conformément à l'annexe VII, sections 4.3 à 4.5. Lorsque cette expérience n'est pas immédiatement manifeste ou applicable, l'organisme notifié expose, documents à l'appui, les raisons justifiant la composition de cette équipe. La procédure d'évaluation comprend un audit dans les locaux du fabricant et, le cas échéant, des fournisseurs et/ou des sous-traitants du fabricant pour vérifier les procédés de fabrication et autres processus pertinents. De plus, dans le cas des dispositifs de classes B et C, l'évaluation du système de gestion de la qualité va de pair avec l'évaluation de la documentation technique en ce qui concerne les dispositifs sélectionnés sur une base représentative comme il est indiqué à la section 4. Pour le choix des échantillons représentatifs, l'organisme notifié tient compte des orientations élaborées et publiées par le GCDM conformément à l'article 99 et notamment de la nouveauté de la technologie, de l'incidence potentielle sur le patient et la pratique médicale standard, des similitudes dans la conception, la technologie, la fabrication et, le cas échéant, les méthodes de stérilisation, de la destination et des résultats de toute évaluation antérieure pertinente réalisée conformément au présent règlement. L'organisme notifié en question établit un dossier justifiant le choix des échantillons. Si le système de gestion de la qualité est conforme aux dispositions pertinentes du présent règlement, l'organisme notifié délivre un certificat UE relatif au système de gestion de la qualité. L'organisme notifié informe le fabricant de sa décision de délivrer le certificat. Cette décision contient les conclusions de l'audit et un rapport motivé. |
||||||||||||||||||||||||||||||||||
2.4. |
Le fabricant en question informe l'organisme notifié qui a approuvé le système de gestion de la qualité de tout projet de modification importante de ce système ou de la gamme des dispositifs couverts. L'organisme notifié évalue les modifications envisagées, détermine si des audits supplémentaires sont nécessaires et vérifie qu'une fois modifié, le système de gestion de la qualité satisfait toujours aux exigences visées à la section 2.2. Il informe le fabricant de sa décision, laquelle contient les conclusions de l'évaluation et, le cas échéant, les conclusions des audits supplémentaires. L'approbation de toute modification importante du système de gestion de la qualité ou de la gamme des dispositifs couverts prend la forme d'un document complémentaire au certificat UE relatif au système de gestion de la qualité. |
||||||||||||||||||||||||||||||||||
3. |
Évaluation de la surveillance |
||||||||||||||||||||||||||||||||||
3.1. |
Le but de la surveillance est d'assurer que le fabricant remplit correctement les obligations qui découlent du système de gestion de la qualité approuvé. |
||||||||||||||||||||||||||||||||||
3.2. |
Le fabricant autorise l'organisme notifié à effectuer tous les audits nécessaires, y compris des audits sur place, et lui fournit toutes les informations pertinentes, en particulier:
|
||||||||||||||||||||||||||||||||||
3.3. |
Les organismes notifiés effectuent périodiquement, au moins tous les douze mois, les audits et les évaluations appropriés pour s'assurer que le fabricant en question applique le système de gestion de la qualité approuvé et le plan de surveillance après commercialisation. Ces audits et évaluations incluent des audits dans les locaux du fabricant et, le cas échéant, des fournisseurs et/ou des sous-traitants du fabricant. Lors de ces audits sur place, l'organisme notifié effectue ou fait effectuer, s'il l'estime nécessaire, des essais pour vérifier le bon fonctionnement du système de gestion de la qualité. Il fournit au fabricant un rapport d'audit de surveillance et, si un essai a été effectué, un rapport d'essai. |
||||||||||||||||||||||||||||||||||
3.4. |
L'organisme notifié effectue de manière aléatoire, au moins une fois tous les cinq ans, des audits sur place inopinés chez le fabricant et, le cas échéant, chez les fournisseurs et/ou les sous-traitants du fabricant, audits qui peuvent être réalisés parallèlement à l'évaluation de surveillance périodique visée à la section 3.3 ou en sus de celle-ci. Pour les audits sur place inopinés, l'organisme notifié établit un plan mais ne le communique pas au fabricant. Dans le cadre de ces audits sur place inopinés, l'organisme notifié procède à des essais sur un échantillon adéquat des dispositifs produits ou sur un échantillon adéquat issu du procédé de fabrication pour vérifier que le dispositif fabriqué est conforme à la documentation technique. Avant l'audit sur place inopiné, l'organisme notifié précise les critères d'échantillonnage et la procédure d'essai. Au lieu des échantillons visés au deuxième alinéa ou en plus de ceux-ci, les organismes notifiés prélèvent des échantillons des dispositifs sur le marché pour vérifier que le dispositif fabriqué est conforme à la documentation technique. Avant le prélèvement d'échantillons, l'organisme notifié en question précise les critères d'échantillonnage et la procédure d'essai. L'organisme notifié fournit au fabricant en question un rapport d'audit sur place incluant, le cas échéant, le résultat des essais auxquels ont été soumis les échantillons. |
||||||||||||||||||||||||||||||||||
3.5. |
Dans le cas des dispositifs de classes B et C, l'évaluation de la surveillance inclut également l'évaluation de la documentation technique telle qu'elle est indiquée à la section 4 pour le ou les dispositifs concernés, sur la base d'échantillons représentatifs choisis suivant les critères établis et documentés par l'organisme notifié conformément à la section 2.3, troisième alinéa. |
||||||||||||||||||||||||||||||||||
3.6. |
Les organismes notifiés veillent à ce que la composition de l'équipe d'évaluation garantisse une expérience dans la technologie concernée, une objectivité et une neutralité constantes, ce qui suppose un roulement des membres de l'équipe d'évaluation à des intervalles appropriés. En règle générale, un auditeur n'est pas responsable ou chargé des audits auprès d'un même fabricant pendant plus de trois années consécutives. |
||||||||||||||||||||||||||||||||||
3.7. |
Si l'organisme notifié constate qu'il existe une divergence entre l'échantillon prélevé à la production ou sur le marché et les spécifications définies dans la documentation technique ou la conception approuvée, il suspend ou annule le certificat correspondant ou l'assortit de restrictions. |
CHAPITRE II
ÉVALUATION DE LA DOCUMENTATION TECHNIQUE
4. |
Évaluation de la documentation technique des dispositifs des classes B, C et D et vérification des lots, applicables aux dispositifs de classe D |
||||||||||||||||||||
4.1. |
Outre l'obligation énoncée à la section 2, le fabricant de dispositifs de classe D soumet à l'organisme notifié une demande d'évaluation de la documentation technique relative au dispositif qu'il prévoit de mettre sur le marché ou de mettre en service et qui est concerné par le système de gestion de la qualité visé à la section 2. |
||||||||||||||||||||
4.2. |
La demande contient une description de la conception, de la fabrication et des performances du dispositif en question. Elle inclut la documentation technique visée aux annexes II et III. Dans le cas des dispositifs d'autodiagnostic ou de diagnostic près du patient, la demande inclut également les aspects visés à la section 5.1, point b). |
||||||||||||||||||||
4.3. |
L'organisme notifié fait évaluer la documentation technique par un personnel qui possède des connaissances et une expérience attestées de l'évaluation de la technologie et des dispositifs concernés et de l'évaluation des preuves cliniques. L'organisme notifié peut exiger que la demande soit complétée en faisant effectuant des essais ou en demandant la fourniture de preuves supplémentaires, afin de permettre l'évaluation de la conformité avec les exigences applicables du présent règlement. L'organisme notifié effectue les essais physiques ou les essais en laboratoire adéquats pour le dispositif ou demande au fabricant d'effectuer ces essais. |
||||||||||||||||||||
4.4. |
L'organisme notifié examine les preuves cliniques présentées par le fabricant dans le rapport sur l'évaluation des performances et l'évaluation des performances connexe qui a été réalisée. Aux fins de cet examen, il recourt à des examinateurs de dispositifs qu'il emploie et qui disposent d'une expertise clinique suffisante, ainsi qu'à des experts cliniques externes ayant une expérience directe et récente en rapport avec la mise en œuvre clinique du dispositif en question. |
||||||||||||||||||||
4.5. |
Dans le cas où les preuves cliniques reposent partiellement ou totalement sur des données provenant de dispositifs revendiqués comme équivalents au dispositif faisant l'objet de l'évaluation, l'organisme notifié évalue s'il convient d'utiliser ces données, compte tenu de facteurs tels que les nouvelles indications et l'innovation. L'organisme notifié documente clairement ses conclusions sur l'équivalence alléguée et sur la pertinence et la validité des données pour ce qui est de démontrer la conformité. |
||||||||||||||||||||
4.6. |
L'organisme notifié vérifie la validité des preuves cliniques et de l'évaluation des performances et les conclusions tirées par le fabricant quant à la conformité avec les exigences générales applicables en matière de sécurité et de performances. Cette vérification porte sur l'examen de la pertinence de la détermination du rapport bénéfice/risque, de la gestion des risques, de la notice d'utilisation, de la formation de l'utilisateur et du plan de surveillance après commercialisation établi par le fabricant, et comporte également un examen de la nécessité et de la validité du plan de SPAC proposé, selon le cas. |
||||||||||||||||||||
4.7. |
Sur la base de l'évaluation qu'il fait des preuves cliniques, l'organisme notifié analyse l'évaluation des performances et la détermination du rapport bénéfice/risque et examine s'il convient de fixer des échéances spécifiques pour lui permettre d'examiner les actualisations des preuves cliniques reposant sur les données issues de la surveillance après commercialisation et du SPAC. |
||||||||||||||||||||
4.8. |
L'organisme notifié documente clairement les résultats de son évaluation dans le rapport d'évaluation sur l'évaluation des performances. |
||||||||||||||||||||
4.9. |
Avant de délivrer un certificat d'évaluation UE de la documentation technique, l'organisme notifié demande à un laboratoire de référence de l'UE, lorsqu'un tel laboratoire a été désigné conformément à l'article 100, de vérifier les performances du dispositif revendiquées par le fabricant et la conformité du dispositif avec les spécifications communes, lorsque celles-ci existent, ou avec les autres solutions choisies par le fabricant pour garantir un niveau de sécurité et de performances au moins équivalent. Cette vérification comporte des essais en laboratoire effectués par le laboratoire de référence de l'UE visé à l'article 48, paragraphe 5. En outre, dans les cas visés à l'article 48, paragraphe 6, du présent règlement, l'organisme notifié consulte, en suivant la procédure établie à l'article 48, paragraphe 6, du présent règlement, les experts concernés visés à l'article 106 du règlement (UE) 2017/745 au sujet du rapport sur l'évaluation des performances présenté par le fabricant. Le laboratoire de référence de l'UE rend un avis scientifique dans un délai de soixante jours. L'avis scientifique du laboratoire de référence de l'UE et, le cas échéant, les points de vue des experts consultés, en application de la procédure établie à l'article 48, paragraphe 6, ainsi que toute mise à jour éventuelle sont inclus dans la documentation de l'organisme notifié concernant le dispositif. En arrêtant sa décision, l'organisme notifié prend dûment en considération les points de vues exprimés dans l'avis scientifique du laboratoire de référence de l'UE et, le cas échéant, les points de vue exprimés par les experts consultés en application de l'article 48, paragraphe 6. L'organisme notifié ne délivre pas le certificat si l'avis scientifique du laboratoire de référence de l'UE est défavorable. |
||||||||||||||||||||
4.10. |
L'organisme notifié fournit au fabricant un rapport sur l'évaluation de la documentation technique comprenant un rapport d'évaluation sur l'évaluation des performances. Si le dispositif est conforme aux dispositions pertinentes du présent règlement, l'organisme notifié délivre un certificat d'évaluation UE de la documentation technique. Le certificat contient les conclusions de l'évaluation de la documentation technique, les conditions de validité dont il est assorti, les données nécessaires à l'identification du dispositif approuvé et, le cas échéant, une description de la destination du dispositif. |
||||||||||||||||||||
4.11. |
Les modifications du dispositif approuvé requièrent une approbation complémentaire par l'organisme notifié qui a délivré le certificat d'évaluation UE de la documentation technique lorsqu'elles sont susceptibles de remettre en cause la sécurité et les performances du dispositif ou les conditions prescrites pour l'utilisation du dispositif. Lorsque le fabricant envisage une modification de ce type, il en informe l'organisme notifié qui a délivré le certificat d'évaluation UE de la documentation technique. L'organisme notifié évalue les modifications envisagées et décide si celles-ci exigent une nouvelle évaluation de la conformité conformément à l'article 48 ou si elles peuvent faire l'objet d'un document complémentaire au certificat d'évaluation UE de la documentation technique. Dans ce dernier cas, l'organisme notifié évalue les modifications, informe le fabricant de sa décision et, lorsque les modifications sont approuvées, lui fournit un document complémentaire au certificat d'évaluation UE de la documentation technique. Lorsque les modifications sont susceptibles de compromettre la conformité avec les spécifications communes ou les autres solutions retenues par le fabricant qui ont été approuvées par le certificat d'évaluation UE de la documentation technique, l'organisme notifié consulte le laboratoire de référence de l'UE qui a participé à la consultation initiale afin d'obtenir la confirmation du maintien de la conformité avec les spécifications communes ou les autres solutions retenues par le fabricant pour garantir un niveau de sécurité et de performances au moins équivalent. Le laboratoire de référence de l'UE rend un avis scientifique dans un délai de soixante jours. |
||||||||||||||||||||
4.12. |
Pour vérifier la conformité des dispositifs fabriqués de classe D, le fabricant effectue des essais sur chaque lot de dispositifs fabriqués. Une fois les contrôles et les essais terminés, il transmet sans tarder à l'organisme notifié les rapports d'essai correspondants. En outre, le fabricant met à la disposition de l'organisme notifié les échantillons des lots de dispositifs fabriqués, selon des conditions et des modalités convenues au préalable, qui prévoient que l'organisme notifié ou le fabricant envoie des échantillons des lots de dispositifs fabriqués à un laboratoire de référence de l'UE, lorsqu'un tel laboratoire a été désigné conformément à l'article 100, afin que les essais appropriés soient effectués. Le laboratoire de référence de l'UE informe l'organisme notifié des résultats. |
||||||||||||||||||||
4.13. |
Le fabricant peut mettre les dispositifs sur le marché à moins que, dans le délai convenu, qui ne peut dépasser trente jours à compter de la réception des échantillons, l'organisme notifié ne lui communique toute autre décision, notamment toute condition de validité des certificats délivrés. |
||||||||||||||||||||
5. |
Évaluation de la documentation technique pour des types spécifiques de dispositifs |
||||||||||||||||||||
5.1. |
Évaluation de la documentation technique des dispositifs d'autodiagnostic et de diagnostic près du patient des classes B, C et D
|
||||||||||||||||||||
5.2. |
Évaluation de la documentation technique des diagnostics compagnons
|
CHAPITRE III
DISPOSITIONS ADMINISTRATIVES
6. |
Le fabricant ou, lorsque le fabricant ne dispose pas d'un siège social dans un État membre, son mandataire, tient à la disposition des autorités compétentes, pendant une période expirant au plus tôt dix ans après la mise sur le marché du dernier dispositif:
|
||||||||||
7. |
Chaque État membre veille à ce que la documentation visée à la section 6 soit tenue à la disposition des autorités compétentes pendant la période indiquée à ladite section au cas où un fabricant, ou son mandataire, établi sur son territoire fait faillite ou met fin à son activité commerciale avant la fin de cette période. |
ANNEXE X
ÉVALUATION DE LA CONFORMITÉ SUR LA BASE DE L'EXAMEN DE TYPE
1. |
L'examen UE de type est la procédure par laquelle un organisme notifié constate et atteste qu'un dispositif, y compris sa documentation technique et les processus du cycle de vie pertinents ainsi qu'un échantillon représentatif correspondant de la production de dispositifs envisagée, satisfait aux dispositions pertinentes du présent règlement. |
||||||||||||||||||||||||
2. |
Demande Le fabricant présente une demande d'évaluation auprès d'un organisme notifié. La demande comprend:
|
||||||||||||||||||||||||
3. |
Évaluation L'organisme notifié:
|
||||||||||||||||||||||||
4. |
Certificat Si le type est conforme au présent règlement, l'organisme notifié délivre un certificat d'examen UE de type. Le certificat comporte le nom et l'adresse du fabricant, les conclusions de l'évaluation de l'examen de type, les conditions de validité du certificat et les données nécessaires à l'identification du type approuvé. Le certificat est établi conformément à l'annexe XII. Les parties pertinentes de la documentation sont annexées au certificat et une copie est conservée par l'organisme notifié. |
||||||||||||||||||||||||
5. |
Modifications du type |
||||||||||||||||||||||||
5.1. |
Le demandeur informe l'organisme notifié qui a délivré le certificat d'examen UE de type de toute modification prévue du type approuvé, de sa destination et des conditions d'utilisation. |
||||||||||||||||||||||||
5.2. |
Les modifications du dispositif approuvé, y compris la limitation de sa destination ou des conditions d'utilisation, requièrent une approbation complémentaire par l'organisme notifié qui a délivré le certificat d'examen UE de type lorsqu'elles sont susceptibles de remettre en cause la conformité avec les exigences générales en matière de sécurité et de performances ou les conditions prescrites pour l'utilisation du produit. L'organisme notifié examine les modifications envisagées, informe le fabricant de sa décision et lui fournit un document complémentaire au rapport d'examen UE de type. L'approbation de toute modification du type approuvé prend la forme d'un document complémentaire au certificat d'examen UE de type. |
||||||||||||||||||||||||
5.3. |
Les modifications de la destination ou des conditions d'utilisation du dispositif approuvé, sauf s'il s'agit d'une limitation de la destination ou des conditions d'utilisation, nécessitent une nouvelle demande d'évaluation de la conformité. |
||||||||||||||||||||||||
5.4. |
Lorsque les modifications sont susceptibles de compromettre les performances du dispositif revendiquées par le fabricant ou la conformité avec les spécifications communes ou les autres solutions retenues par le fabricant qui ont été approuvées par le certificat d'examen UE de type, l'organisme notifié consulte le laboratoire de référence de l'UE qui a participé à la consultation initiale afin d'obtenir la confirmation du maintien de la conformité avec les spécifications communes, le cas échéant, ou les autres solutions retenues par le fabricant pour garantir un niveau de sécurité et de performances au moins équivalent. Le laboratoire de référence de l'UE rend un avis scientifique dans un délai de soixante jours. |
||||||||||||||||||||||||
5.5. |
Lorsque les modifications sont susceptibles d'avoir une incidence sur les performances ou l'utilisation prévue d'un diagnostic compagnon approuvé par le certificat UE d'examen de type ou sur son adéquation à un médicament, l'organisme notifié consulte l'autorité des médicaments compétente qui a participé à la consultation initiale ou l'EMA. L'autorité des médicaments consultée rend son avis, le cas échéant, dans un délai de trente jours à compter de la réception de la documentation valide concernant les modifications. L'approbation de toute modification du type approuvé prend la forme d'un document complémentaire au certificat d'examen UE de type. |
||||||||||||||||||||||||
6. |
Dispositions administratives Le fabricant ou, lorsque le fabricant ne dispose pas d'un siège social dans un État membre, son mandataire, tient à la disposition des autorités compétentes, pendant une période expirant au plus tôt dix ans après la mise sur le marché du dernier dispositif:
L'annexe IX, section 7, s'applique. |
ANNEXE XI
ÉVALUATION DE LA CONFORMITÉ SUR LA BASE DE L'ASSURANCE DE LA QUALITÉ DE LA PRODUCTION
1. |
Le fabricant veille à la mise en œuvre du système de gestion de la qualité approuvé pour la fabrication des dispositifs concernés, effectue la vérification finale, comme prévu à la section 3, et est soumis à la surveillance visée à la section 4. |
||||||||||
2. |
Lorsque le fabricant respecte les obligations énoncées à la section 1, il établit et conserve une déclaration de conformité UE conformément à l'article 17 et à l'annexe IV pour le dispositif concerné par la procédure d'évaluation de la conformité. En délivrant une déclaration de conformité UE, le fabricant est réputé assurer et déclarer que le dispositif concerné satisfait aux exigences du présent règlement qui sont applicables au dispositif et, dans le cas des dispositifs de classe C et de classe D qui font l'objet d'un examen de type, est conforme au type décrit dans le certificat d'examen UE de type. |
||||||||||
3. |
Système de gestion de la qualité |
||||||||||
3.1. |
Le fabricant soumet une demande d'évaluation de son système de gestion de la qualité à un organisme notifié. La demande comprend:
|
||||||||||
3.2. |
L'application du système de gestion de la qualité permet de garantir la conformité avec le type décrit dans le certificat d'examen UE de type et avec les dispositions du présent règlement qui sont applicables aux dispositifs à chaque étape. L'ensemble des éléments, des exigences et des dispositions adoptés par le fabricant pour son système de gestion de la qualité figurent dans une documentation tenue de manière systématique et ordonnée sous la forme d'un manuel relatif à la qualité et de politiques et de procédures écrites, telles que des programmes, des plans et des enregistrements relatifs à la qualité. Cette documentation comprend notamment une description adéquate de tous les éléments énumérés à l'annexe IX, section 2.2, points a), b), d) et e). |
||||||||||
3.3. |
L'annexe IX, section 2.3, premier et deuxième alinéas, s'applique. Si le système de gestion de la qualité est de nature à garantir que les dispositifs sont conformes au type décrit dans le certificat d'examen UE de type et aux dispositions pertinentes du présent règlement, l'organisme notifié délivre un certificat UE d'assurance de la qualité de la production. L'organisme notifié informe le fabricant de sa décision de délivrer le certificat. Cette décision contient les conclusions de l'audit de l'organisme notifié et une évaluation motivée. |
||||||||||
3.4. |
L'annexe IX, section 2.4, s'applique. |
||||||||||
4. |
Surveillance L'annexe IX, section 3.1, section 3.2, premier, deuxième et quatrième tirets, et sections 3.3, 3.4, 3.6 et 3.7, s'applique. |
||||||||||
5. |
Vérification des dispositifs fabriqués de classe D |
||||||||||
5.1. |
Dans le cas des dispositifs de classe D, le fabricant effectue des essais sur chaque lot de dispositifs. Une fois les contrôles et les essais terminés, il transmet sans tarder à l'organisme notifié les rapports d'essai correspondants. En outre, le fabricant met à la disposition de l'organisme notifié les échantillons des dispositifs ou des lots de dispositifs fabriqués, selon des conditions et des modalités convenues au préalable, qui prévoient que l'organisme notifié ou le fabricant envoie des échantillons des dispositifs ou des lots de dispositifs fabriqués à un laboratoire de référence de l'UE, lorsqu'un tel laboratoire a été désigné conformément à l'article 100, afin que les essais en laboratoire appropriés soient effectués. Le laboratoire de référence de l'UE informe l'organisme notifié des résultats. |
||||||||||
5.2. |
Le fabricant peut mettre les dispositifs sur le marché à moins que, dans le délai convenu, qui ne peut dépasser trente jours à compter de la réception des échantillons, l'organisme notifié ne lui communique toute autre décision, notamment toute condition de validité des certificats délivrés. |
||||||||||
6. |
Dispositions administratives Le fabricant ou, lorsque le fabricant ne dispose pas d'un siège social dans un État membre, son mandataire, tient à la disposition des autorités compétentes, pendant une période expirant au plus tôt dix ans après la mise sur le marché du dernier dispositif:
L'annexe IX, section 7, s'applique. |
ANNEXE XII
CERTIFICATS DÉLIVRÉS PAR UN ORGANISME NOTIFIÉ
CHAPITRE I
EXIGENCES GÉNÉRALES
1. |
Les certificats sont établis dans une des langues officielles de l'Union. |
||||
2. |
Chaque certificat ne se réfère qu'à une seule procédure d'évaluation de la conformité. |
||||
3. |
Les certificats ne sont délivrés qu'à un seul fabricant. Le nom et l'adresse du fabricant figurant sur le certificat sont les mêmes que ceux enregistrés dans le système électronique visé à l'article 27. |
||||
4. |
Le champ d'application des certificats identifie sans ambiguïté le ou les dispositifs auxquels ils se rapportent:
|
||||
5. |
L'organisme notifié est en mesure de démontrer, sur demande, quels sont les (différents) dispositifs auxquels le certificat se rapporte. L'organisme notifié met en place un système permettant de déterminer quels sont les dispositifs, y compris leur classe, auxquels le certificat se rapporte. |
||||
6. |
Les certificats contiennent, s'il y a lieu, une note indiquant que, aux fins d'une mise sur le marché du ou des dispositifs auxquels le certificat se rapporte, un autre certificat délivré conformément aux dispositions du présent règlement est requis. |
||||
7. |
Les certificats UE concernant le système de gestion de la qualité et les certificats UE d'assurance de la qualité de la production pour les dispositifs stériles de classe A comprennent une déclaration selon laquelle l'audit réalisé par l'organisme notifié était limité aux aspects de la fabrication liés à l'obtention et au maintien de l'état stérile. |
||||
8. |
Lorsqu'un certificat est complété, modifié ou délivré à nouveau, le nouveau certificat comporte une référence au certificat précédent et à sa date de délivrance et précise les modifications apportées. |
CHAPITRE II
CONTENU MINIMAL DES CERTIFICATS
1. |
Le nom, l'adresse et le numéro d'identification de l'organisme notifié. |
2. |
Le nom et l'adresse du fabricant et, le cas échéant, du mandataire. |
3. |
Le numéro unique permettant d'identifier le certificat. |
4. |
S'il a déjà été délivré, le numéro d'enregistrement unique du fabricant visé à l'article 28, paragraphe 2. |
5. |
La date de délivrance. |
6. |
La date d'expiration. |
7. |
Les données nécessaires pour l'identification non ambiguë du ou des dispositifs, le cas échéant, comme indiqué à la section 4 de la présente annexe. |
8. |
Le cas échéant, la référence à tout certificat précédent, comme indiqué au chapitre I, section 8. |
9. |
Une référence au présent règlement et à l'annexe correspondante conformément à laquelle l'évaluation de la conformité a été effectuée. |
10. |
Les contrôles et les essais effectués, par exemple une référence aux spécifications communes, aux normes harmonisées, aux rapports d'essais et au(x) rapport(s) d'audit correspondants. |
11. |
Le cas échéant, une référence aux parties correspondantes de la documentation technique ou d'autres certificats requis pour la mise sur le marché du ou des dispositifs concernés. |
12. |
Le cas échéant, les informations relatives à la surveillance par l'organisme notifié. |
13. |
Les conclusions de l'évaluation de la conformité par l'organisme notifié, compte tenu de l'annexe applicable. |
14. |
Les conditions ou les limitations de la validité du certificat. |
15. |
La signature autorisée de l'organisme notifié conformément à la législation nationale applicable. |
ANNEXE XIII
ÉVALUATION DES PERFORMANCES, ÉTUDES DES PERFORMANCES ET SUIVI DES PERFORMANCES APRÈS COMMERCIALISATION
PARTIE A
ÉVALUATION DES PERFORMANCES ET ÉTUDES DES PERFORMANCES
1. |
ÉVALUATION DES PERFORMANCES L'évaluation des performances d'un dispositif est un processus continu par lequel des données sont évaluées et analysées pour démontrer la validité scientifique, les performances analytiques et les performances cliniques de ce dispositif au regard de la destination définie par le fabricant. Pour planifier, effectuer en continu et documenter une évaluation des performances, le fabricant établit et met à jour un plan d'évaluation des performances. Le plan d'évaluation des performances précise les caractéristiques et les performances du dispositif ainsi que le processus et les critères appliqués pour obtenir les preuves cliniques nécessaires. L'évaluation des performances est approfondie et objective et il est tenu compte des données aussi bien favorables que défavorables. Son ampleur et sa portée sont proportionnées et adaptées aux caractéristiques du dispositif, notamment les risques qu'il présente, sa classe de risque, ses performances et sa destination. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1.1. |
Plan d'évaluation des performances En règle générale et au minimum, le plan d'évaluation des performances:
Lorsque l'un des éléments énumérés ci-dessus n'est pas jugé approprié dans le plan d'évaluation des performances en raison des caractéristiques d'un dispositif donné, une justification est fournie dans le plan. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1.2. |
Démonstration de la validité scientifique et des performances analytiques et cliniques À titre de principe méthodologique général, le fabricant:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1.2.1. |
Démonstration de la validité scientifique Le fabricant démontre la validité scientifique sur la base d'une ou de plusieurs des sources suivantes:
La validité scientifique de l'analyte ou marqueur est démontrée et documentée dans le rapport sur la validité scientifique. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1.2.2. |
Démonstration des performances analytiques Le fabricant démontre les performances analytiques du dispositif au regard de tous les paramètres visés à l'annexe I, section 9.1, point a), sauf paramètre non applicable. En règle générale, les performances analytiques sont toujours démontrées sur la base des études des performances analytiques. Pour les marqueurs nouveaux ou d'autres marqueurs sans matériaux de référence certifiés ou procédures de mesure de référence disponibles, il est possible que la justesse ne puisse pas être démontrée. S'il n'existe pas de méthodes comparatives, différentes démarches peuvent être suivies si la preuve de leur adéquation est faite, comme la comparaison avec d'autres méthodes bien documentées ou la méthode de référence composite. En l'absence de telles démarches, une étude des performances cliniques comparant les performances du dispositif nouveau à la pratique clinique standard en vigueur est requise. Les performances analytiques sont démontrées et documentées dans le rapport sur les performances analytiques. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1.2.3. |
Démonstration des performances cliniques Le fabricant démontre les performances cliniques du dispositif au regard de tous les paramètres visés à l'annexe I, section 9.1, point b), sauf paramètre non applicable. Les performances cliniques d'un dispositif sont démontrées sur la base d'une ou de plusieurs des sources suivantes:
Les études des performances cliniques sont réalisées sauf s'il est dûment justifié de s'en tenir à d'autres sources de données sur les performances cliniques. Les performances cliniques sont démontrées et documentées dans le rapport sur les performances cliniques. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1.3. |
Preuves cliniques et rapport sur l'évaluation des performances |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1.3.1. |
Le fabricant évalue l'ensemble des données pertinentes concernant la validité scientifique et les performances analytiques et cliniques afin de vérifier que son dispositif est conforme aux exigences générales en matière de sécurité et de performances visées à l'annexe I. Le volume et la qualité de ces données permettent au fabricant d'évaluer, en connaissance de cause, si le dispositif offrira le ou les bénéfices cliniques et la sécurité attendus lorsqu'il est utilisé comme prévu par le fabricant. Les données et conclusions issues de cette évaluation constituent les preuves cliniques pour le dispositif. Les preuves cliniques démontrent de manière scientifique que le ou les bénéfices cliniques et la sécurité attendus seront atteints conformément à l'état de l'art dans le domaine médical. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1.3.2. |
Rapport sur l'évaluation des performances Les preuves cliniques sont documentées dans un rapport sur l'évaluation des performances. Ce rapport comprend le rapport sur la validité scientifique, le rapport sur les performances analytiques et le rapport sur les performances cliniques, ainsi qu'une évaluation de ces rapports permettant d'étayer les preuves cliniques. Le rapport sur l'évaluation des performances comprend notamment:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1.3.3. |
Les preuves cliniques et leur évaluation figurant dans le rapport sur l'évaluation des performances sont actualisées tout au long du cycle de vie du dispositif concerné à l'aide des données obtenues par le fabricant à la suite de l'application de son plan de SPAC conformément à la partie B de la présente annexe, dans le cadre de l'évaluation des performances et du système de surveillance après commercialisation visé à l'article 10, paragraphe 9. Le rapport sur l'évaluation des performances fait partie de la documentation technique. Les données favorables et défavorables prises en compte dans l'évaluation des performances figurent dans la documentation technique. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2. |
ÉTUDES DES PERFORMANCES CLINIQUES |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2.1. |
But des études des performances cliniques Le but des études des performances cliniques est d'établir ou de confirmer des aspects des performances du dispositif qui ne peuvent être déterminés par les études des performances analytiques, la documentation et/ou l'expérience préalable acquise grâce aux tests de diagnostic de routine. Ces informations sont utilisées pour démontrer la conformité avec les exigences générales applicables en matière de sécurité et de performances relatives aux performances cliniques. Lorsque des études des performances cliniques sont effectuées, les données obtenues sont utilisées dans le processus d'évaluation des performances et font partie des preuves cliniques pour le dispositif. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2.2. |
Considérations éthiques pour les études des performances cliniques Chaque étape de l'étude des performances cliniques, depuis la première réflexion sur la nécessité et la justification de l'étude jusqu'à la publication des résultats, respecte des principes éthiques reconnus. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2.3. |
Méthodes pour les études des performances cliniques |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2.3.1. |
Type de conception de l'étude des performances cliniques Les études des performances cliniques sont conçues de manière à maximiser la pertinence des données et à réduire au minimum les biais éventuels. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2.3.2. |
Plan d'étude des performances cliniques Les études des performances cliniques sont effectuées sur la base d'un plan d'étude des performances cliniques. Le plan d'étude des performances cliniques énonce la justification, les objectifs, la conception et l'analyse proposée, les méthodes, le contrôle, la réalisation de l'étude des performances cliniques et la documentation de ses résultats. Il contient en particulier les informations ci-après.
Si une partie des informations visées au deuxième alinéa est fournie dans un document distinct, le plan en fait état. Les points u), x), y) et z) ne s'appliquent pas dans le cas des études utilisant des échantillons restants. Lorsque l'un des éléments visés au deuxième alinéa n'est pas jugé approprié dans le plan d'étude des performances cliniques en raison du modèle d'étude spécifique choisi (par exemple utilisation d'échantillons restants ou études interventionnelles des performances cliniques), une justification est fournie. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2.3.3. |
Rapport sur l'étude des performances cliniques Un rapport sur l'étude des performances cliniques, signé par un médecin ou toute autre personne autorisée, contient des informations documentées sur le plan d'étude des performances cliniques, les résultats et les conclusions de l'étude des performances cliniques, y compris les résultats négatifs. Les résultats et les conclusions sont transparents, exempts de biais et cliniquement pertinents. Le rapport contient suffisamment d'informations pour être compris par une partie indépendante sans qu'il soit nécessaire de se référer à d'autres documents. Le rapport mentionne également, si nécessaire, toute modification du protocole ou tout écart par rapport à celui-ci, ainsi que toute exclusion de données, et en fournit la justification appropriée. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
3. |
AUTRES ÉTUDES DES PERFORMANCES Par analogie, le plan d'étude des performances visé à la section 2.3.2 et le rapport sur l'étude des performances visé à la section 2.3.3 sont documentés pour d'autres études des performances que les études des performances cliniques. |
PARTIE B
SUIVI DES PERFORMANCES APRÈS COMMERCIALISATION
4. |
Le SPAC s'entend comme un processus continu de mise à jour de l'évaluation des performances visée à l'article 56 et à la partie A de la présente annexe et il s'inscrit, en particulier, dans le plan de surveillance après commercialisation établi par le fabricant. Dans le cadre du SPAC, le fabricant collecte et évalue de manière proactive des données relatives aux performances et des données scientifiques pertinentes résultant de l'utilisation d'un dispositif qui porte le marquage CE et est mis sur le marché ou mis en service conformément à sa destination, comme prévu dans la procédure d'évaluation de la conformité correspondante, dans le but de confirmer la sécurité, les performances et la validité scientifique pendant toute la durée de vie prévue du dispositif, de garantir le caractère constamment acceptable du rapport /bénéfice/risque et de détecter les risques émergents sur la base d'éléments de preuve concrets. |
||||||||||||||||
5. |
Le SPAC est effectué conformément à une méthode documentée exposée dans un plan de SPAC. |
||||||||||||||||
5.1. |
Le plan de SPAC précise les méthodes et les procédures à suivre pour collecter et évaluer de manière proactive des données relatives à la sécurité et aux performances et des données scientifiques dans le but:
|
||||||||||||||||
5.2. |
Le plan de SPAC comprend au moins:
|
||||||||||||||||
6. |
Le fabricant analyse les résultats du SPAC et les documente dans un rapport d'évaluation du SPAC, qui met à jour le rapport sur l'évaluation des performances et fait partie de la documentation technique. |
||||||||||||||||
7. |
Les conclusions du rapport d'évaluation du SPAC sont prises en compte pour l'évaluation des performances visée à l'article 56 et à la partie A de la présente annexe ainsi que pour la gestion des risques visée à l'annexe I, section 3. Si le SPAC met en évidence la nécessité de mesures préventives et/ou correctives, le fabricant met en place de telles mesures. |
||||||||||||||||
8. |
Si le SPAC n'est pas jugé approprié pour un dispositif donné, une justification est fournie et documentée dans le rapport sur l'évaluation des performances. |
ANNEXE XIV
ÉTUDES INTERVENTIONNELLES DES PERFORMANCES CLINIQUES ET CERTAINES AUTRES ÉTUDES DES PERFORMANCES
CHAPITRE I
DOCUMENTATION CONCERNANT LA DEMANDE RELATIVE AUX ÉTUDES INTERVENTIONNELLES DES PERFORMANCES CLINIQUES ET AUX AUTRES ÉTUDES DES PERFORMANCES PRÉSENTANT DES RISQUES POUR LES PARTICIPANTS AUX ÉTUDES
Pour les dispositifs qui sont destinés à être utilisés dans le cadre d'études interventionnelles des performances cliniques ou d'autres études des performances présentant des risques pour les participants aux études, le promoteur élabore et présente la demande, conformément à l'article 58, accompagnée des documents suivants:
1. |
Formulaire de demande Le formulaire de demande est dûment complété et contient ce qui suit: |
||||||
1.1. |
le nom, l'adresse et les coordonnées du promoteur et, s'il y a lieu, ceux de sa personne de contact ou de son représentant légal conformément à l'article 58, paragraphe 4, qui est établi dans l'Union; |
||||||
1.2. |
s'ils sont différents de ceux de la section 1.1, le nom, l'adresse et les coordonnées du fabricant du dispositif dont les performances doivent être évaluées et, s'il y a lieu, ceux de son mandataire; |
||||||
1.3. |
l'intitulé de l'étude des performances; |
||||||
1.4. |
le numéro d'identification unique visé à l'article 66, paragraphe 1; |
||||||
1.5. |
le statut de l'étude des performances, par exemple première demande, réintroduction de la demande, modification significative; |
||||||
1.6. |
les détails et/ou références du plan d'étude des performances, comprenant par exemple des détails relatifs à la phase de conception de l'étude des performances; |
||||||
1.7. |
si la demande est réintroduite pour un dispositif ayant déjà fait l'objet d'une demande, la ou les dates et le ou les numéros de référence de la demande précédente ou, en cas de modification significative, la référence de la demande initiale. Le promoteur met en évidence toutes les modifications par rapport à la demande précédente, en les justifiant, et indique par exemple si ces modifications donnent suite aux conclusions d'examens antérieurs de l'autorité compétente ou du comité d'éthique; |
||||||
1.8. |
si la demande est introduite parallèlement à une demande d'essai clinique conformément au règlement (UE) no 536/2014, la référence au numéro d'enregistrement officiel de l'essai clinique; |
||||||
1.9. |
la mention des États membres et des pays tiers dans lesquels l'étude des performances cliniques sera menée dans le cadre d'une étude multicentrique ou multinationale au moment de la demande; |
||||||
1.10. |
une description succincte du dispositif devant faire l'objet d'une étude des performances, sa classification et d'autres informations nécessaires aux fins de l'identification du dispositif et du type de dispositif; |
||||||
1.11. |
un résumé du plan d'étude des performances; |
||||||
1.12. |
le cas échéant, des informations sur un dispositif comparateur, sa classification et d'autres informations nécessaires aux fins de l'identification du dispositif comparateur; |
||||||
1.13. |
des éléments de preuve fournis par le promoteur, indiquant que l'investigateur et le site d'investigation sont aptes à la réalisation de l'étude des performances cliniques selon le plan d'étude des performances; |
||||||
1.14. |
des indications concernant la date prévue pour le début de l'étude des performances et sa durée envisagée; |
||||||
1.15. |
des informations permettant d'identifier l'organisme notifié si celui-ci est déjà impliqué au stade de la demande d'étude des performances; |
||||||
1.16. |
la confirmation que le promoteur est conscient que l'autorité compétente peut contacter le comité d'éthique qui évalue ou a évalué la demande; |
||||||
1.17. |
la déclaration visée à la section 4.1. |
||||||
2. |
Brochure pour l'investigateur La brochure pour l'investigateur contient les informations sur le dispositif devant faire l'objet d'une étude des performances qui sont utiles à l'étude et disponibles au moment de la demande. Toute mise à jour de la brochure pour l'investigateur ou toute autre information utile ultérieure est portée en temps voulu à l'attention des investigateurs. La brochure est clairement identifiée et contient notamment ce qui suit: |
||||||
2.1. |
les données d'identification et la description du dispositif, et notamment des informations sur la destination, la classification en fonction des risques et la règle de classification applicable en vertu de l'annexe VIII, la conception et la fabrication du dispositif et la référence aux générations précédentes et similaires du dispositif; |
||||||
2.2. |
les instructions du fabricant concernant l'installation, la maintenance, le maintien des normes d'hygiène et l'utilisation, notamment les conditions de stockage et de manipulation, ainsi que, dans la mesure où ces informations sont disponibles, les données devant figurer sur l'étiquette et la notice d'utilisation devant être fournie avec le dispositif lors de sa mise sur le marché; en outre, des informations sur toute formation requise; |
||||||
2.3. |
les performances analytiques; |
||||||
2.4. |
les données cliniques existantes, notamment:
|
||||||
2.5. |
un résumé de l'analyse bénéfice/risque et de la gestion des risques, et notamment des informations sur les risques connus ou prévisibles et sur les mises en garde; |
||||||
2.6. |
dans le cas des dispositifs contenant des tissus, des cellules et des substances d'origine humaine, animale ou microbienne, des informations détaillées sur ces tissus, ces cellules et ces substances, et sur le respect des exigences générales en matière de sécurité et de performances et la gestion des risques particuliers posés par ces tissus, ces cellules et ces substances; |
||||||
2.7. |
une liste détaillant le respect des exigences générales applicables en matière de sécurité et de performances énoncées à l'annexe I, y compris des normes et des spécifications communes appliquées, en totalité ou en partie, ainsi qu'une description des solutions retenues pour satisfaire aux exigences générales applicables en matière de sécurité et de performances, dans la mesure où ces normes et spécifications communes n'ont pas été respectées, ou ne l'ont été que partiellement, ou en l'absence de normes et spécifications; |
||||||
2.8. |
une description détaillée des procédures cliniques et des essais diagnostiques utilisés au cours de l'étude des performances et, notamment, des informations sur tout écart par rapport à la pratique clinique normale. |
||||||
3. |
Plan d'étude des performances visé à l'annexe XIII, sections 2 et 3 |
||||||
4. |
Autres informations |
||||||
4.1. |
Déclaration signée par la personne physique ou morale responsable de la fabrication du dispositif devant faire l'objet d'une étude des performances, selon laquelle le dispositif en question est conforme aux exigences générales en matière de sécurité et de performances énoncées à l'annexe I indépendamment des aspects relevant de l'étude des performances cliniques et selon laquelle, en ce qui concerne ces aspects, toutes les précautions ont été prises pour protéger la santé et la sécurité du participant. |
||||||
4.2. |
Lorsque le droit national le prévoit, copie du ou des avis du ou des comités d'éthique concernés. Lorsqu'en vertu de la législation nationale, l'avis ou les avis du ou des comités d'éthique ne sont pas exigés au moment de la présentation de la demande, une copie du ou des avis du ou des comités d'éthique est transmise dès qu'elle est disponible. |
||||||
4.3. |
Preuve de la souscription d'une assurance ou de l'affiliation à un régime d'indemnisation des participants en cas de blessure, en vertu de l'article 65 et du droit national correspondant. |
||||||
4.4. |
Documents à utiliser aux fins de l'obtention d'un consentement éclairé, y compris la fiche d'information du patient et le document relatif au consentement éclairé. |
||||||
4.5. |
Description des dispositions prises pour respecter les règles applicables en matière de protection et de confidentialité des données à caractère personnel, notamment:
|
||||||
4.6. |
Description complète de la documentation technique disponible, par exemple celle relative à la gestion/l'analyse des risques ou des rapports d'essais spécifiques, à présenter sur demande à l'autorité compétente chargée de l'examen d'une demande. |
CHAPITRE II
AUTRES OBLIGATIONS DU PROMOTEUR
1. |
Le promoteur s'emploie à tenir à la disposition des autorités nationales compétentes toutes les pièces justificatives des documents visés à la section I de la présente annexe. Si le promoteur n'est pas la personne physique ou morale responsable de la fabrication du dispositif devant faire l'objet d'une étude des performances, cette obligation peut être remplie par ladite personne au nom du promoteur. |
2. |
Le promoteur a conclu un accord garantissant que tout événement indésirable grave ou tout autre événement visé à l'article 76, paragraphe 2, lui est signalé en temps utile par le ou les investigateurs. |
3. |
Les documents mentionnés dans la présente annexe sont conservés pour une durée d'au moins dix ans après la fin de l'étude des performances cliniques du dispositif en question ou, lorsque le dispositif est ensuite mis sur le marché, d'au moins dix ans après la mise sur le marché du dernier dispositif. Chaque État membre exige que les documents visés dans la présente annexe soient tenus à la disposition des autorités compétentes pour la durée indiquée au premier alinéa au cas où le promoteur, ou sa personne de contact, établi sur son territoire fait faillite ou met fin à ses activités avant la fin de cette période. |
4. |
Le promoteur nomme un contrôleur indépendant du site d'investigation, chargé de veiller à ce que l'étude des performances cliniques soit réalisée conformément au plan d'étude des performances cliniques, aux principes des bonnes pratiques cliniques et au présent règlement. |
5. |
Le promoteur achève le suivi des participants. |
ANNEXE XV
TABLEAU DE CORRESPONDANCE
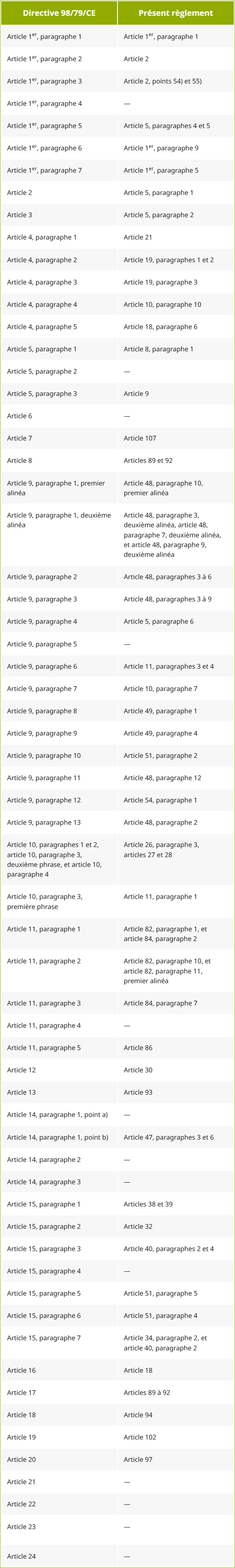
| Directive 98/79/CE | Présent règlement |
|---|---|
| Article 1er, paragraphe 1 | Article 1er, paragraphe 1 |
| Article 1er, paragraphe 2 | Article 2 |
| Article 1er, paragraphe 3 | Article 2, points 54) et 55) |
| Article 1er, paragraphe 4 | — |
| Article 1er, paragraphe 5 | Article 5, paragraphes 4 et 5 |
| Article 1er, paragraphe 6 | Article 1er, paragraphe 9 |
| Article 1er, paragraphe 7 | Article 1er, paragraphe 5 |
| Article 2 | Article 5, paragraphe 1 |
| Article 3 | Article 5, paragraphe 2 |
| Article 4, paragraphe 1 | Article 21 |
| Article 4, paragraphe 2 | Article 19, paragraphes 1 et 2 |
| Article 4, paragraphe 3 | Article 19, paragraphe 3 |
| Article 4, paragraphe 4 | Article 10, paragraphe 10 |
| Article 4, paragraphe 5 | Article 18, paragraphe 6 |
| Article 5, paragraphe 1 | Article 8, paragraphe 1 |
| Article 5, paragraphe 2 | — |
| Article 5, paragraphe 3 | Article 9 |
| Article 6 | — |
| Article 7 | Article 107 |
| Article 8 | Articles 89 et 92 |
| Article 9, paragraphe 1, premier alinéa | Article 48, paragraphe 10, premier alinéa |
| Article 9, paragraphe 1, deuxième alinéa | Article 48, paragraphe 3, deuxième alinéa, article 48, paragraphe 7, deuxième alinéa, et article 48, paragraphe 9, deuxième alinéa |
| Article 9, paragraphe 2 | Article 48, paragraphes 3 à 6 |
| Article 9, paragraphe 3 | Article 48, paragraphes 3 à 9 |
| Article 9, paragraphe 4 | Article 5, paragraphe 6 |
| Article 9, paragraphe 5 | — |
| Article 9, paragraphe 6 | Article 11, paragraphes 3 et 4 |
| Article 9, paragraphe 7 | Article 10, paragraphe 7 |
| Article 9, paragraphe 8 | Article 49, paragraphe 1 |
| Article 9, paragraphe 9 | Article 49, paragraphe 4 |
| Article 9, paragraphe 10 | Article 51, paragraphe 2 |
| Article 9, paragraphe 11 | Article 48, paragraphe 12 |
| Article 9, paragraphe 12 | Article 54, paragraphe 1 |
| Article 9, paragraphe 13 | Article 48, paragraphe 2 |
| Article 10, paragraphes 1 et 2, article 10, paragraphe 3, deuxième phrase, et article 10, paragraphe 4 | Article 26, paragraphe 3, articles 27 et 28 |
| Article 10, paragraphe 3, première phrase | Article 11, paragraphe 1 |
| Article 11, paragraphe 1 | Article 82, paragraphe 1, et article 84, paragraphe 2 |
| Article 11, paragraphe 2 | Article 82, paragraphe 10, et article 82, paragraphe 11, premier alinéa |
| Article 11, paragraphe 3 | Article 84, paragraphe 7 |
| Article 11, paragraphe 4 | — |
| Article 11, paragraphe 5 | Article 86 |
| Article 12 | Article 30 |
| Article 13 | Article 93 |
| Article 14, paragraphe 1, point a) | — |
| Article 14, paragraphe 1, point b) | Article 47, paragraphes 3 et 6 |
| Article 14, paragraphe 2 | — |
| Article 14, paragraphe 3 | — |
| Article 15, paragraphe 1 | Articles 38 et 39 |
| Article 15, paragraphe 2 | Article 32 |
| Article 15, paragraphe 3 | Article 40, paragraphes 2 et 4 |
| Article 15, paragraphe 4 | — |
| Article 15, paragraphe 5 | Article 51, paragraphe 5 |
| Article 15, paragraphe 6 | Article 51, paragraphe 4 |
| Article 15, paragraphe 7 | Article 34, paragraphe 2, et article 40, paragraphe 2 |
| Article 16 | Article 18 |
| Article 17 | Articles 89 à 92 |
| Article 18 | Article 94 |
| Article 19 | Article 102 |
| Article 20 | Article 97 |
| Article 21 | — |
| Article 22 | — |
Article 23 |
— |
| Article 24 | — |